Clear Sky Science · sv
Nanopartiklar med dubbel styvhet för fackspecifik läkemedelsleverans vid stroke
Att angripa stroke på två fronter
Stroke beskrivs ofta som en hjärnattack, men denna forskning visar att skadorna inte stannar vid hjärnan. När en större artär i hjärnan blockeras utbryter en inflammationsstorm både i blodet och inne i hjärnan. Denna studie presenterar en smart nanomedicinsk strategi som skickar en typ av små partiklar för att lugna immunsystemet i blodomloppet medan en annan typ smyger in i hjärnan för att hjälpa skadade nervceller återhämta sig — allt från en enda injektion.
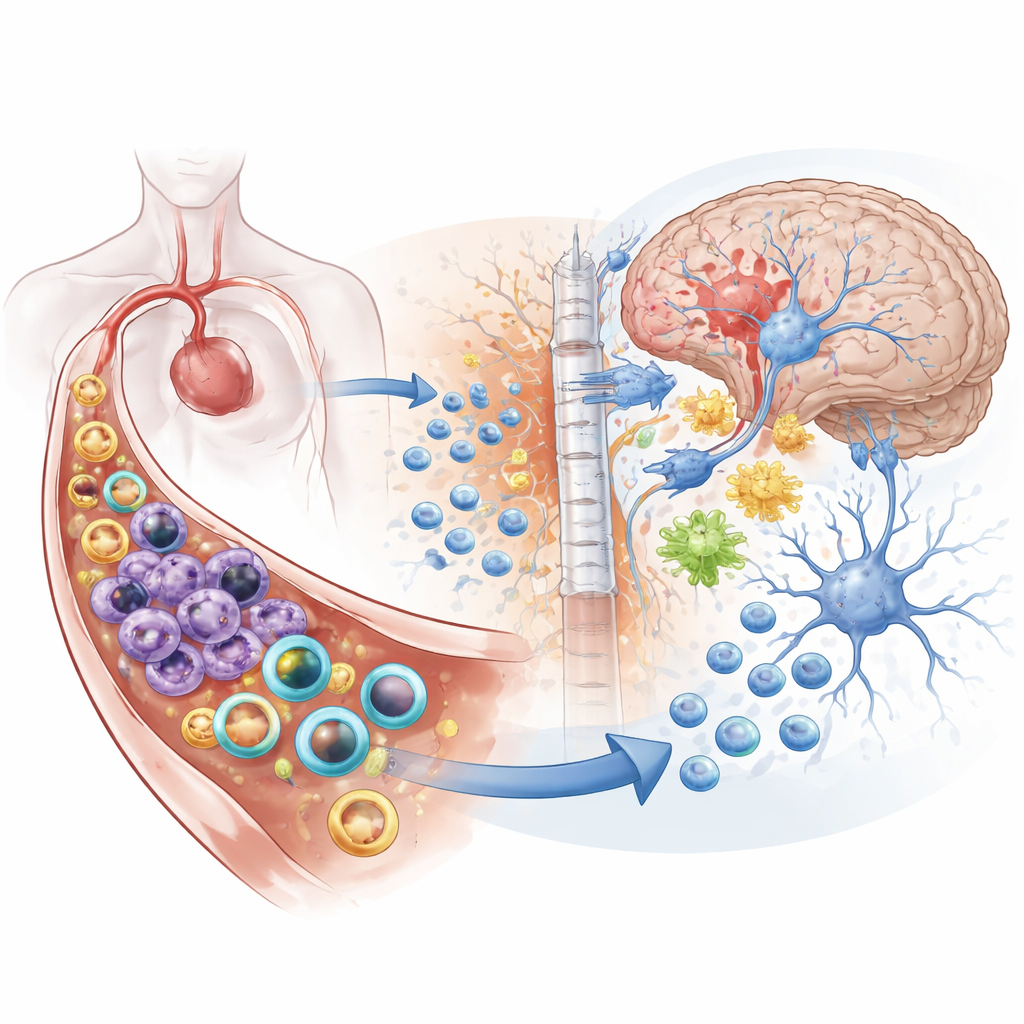
Varför stroke är mer än en lokal skada
Ischemisk stroke, orsakad av en blodpropp som blockerar blodflödet till hjärnan, är den vanligaste formen av stroke och en ledande orsak till död och funktionsnedsättning världen över. När hjärnvävnad förlorar syre dör nervceller, giftiga molekyler frigörs och blod–hjärnbarriären — den skyddande väggen mellan blod och hjärna — börjar läcka. Stresssignaler sipprar ut i blodbanan och kallar på arméer av immunceller som neutrofiler och monocyter. Dessa celler skyndar mot hjärnan, pressar sig genom blodkärlen och förvärrar svullnad och vävnadsskada. Många nuvarande behandlingar fokuserar antingen på att dämpa immunsystemet överallt eller försöka skydda neuroner direkt, men sällan båda på ett samordnat sätt.
Utformning av två sorters helande partiklar
Forskargruppen resonerade att en nanopartikels fysiska ”känsla” — hur styv eller mjuk den är — kan avgöra vilka celler som tar upp den. De byggde två nästan identiska partiklar av godkända material: mjuka, kramvänliga liposomer och styvare partiklar skapade genom att placera en solid polymerkärna i ett liknande lipidskal. Båda typerna hade liknande storlek, laddning och ytkemin, men mycket olika styvhet. I cellexperiment sögs de styva partiklarna girigt upp av immunceller, medan neuroner visade en tydlig preferens för de mjukare. När båda gavs samtidigt fokuserade immuncellerna ännu mer på de styva partiklarna och ignorerade till stor del de mjuka, vilket tillät de senare att passera i större antal.
Hur mekanik och blodproteiner styr partiklarna
Datorsimuleringar och biokemiska tester hjälpte till att förklara detta delade beteende. Styva partiklar krävde mindre energi för att cellerna skulle linda sina membran runt dem, vilket gjorde dem lättare att omsluta. Mjuka partiklar fastnade väl vid membranet men var svårare att dra helt in, särskilt för styva, högaktiva immunceller. Samtidigt täckte blodet partiklarna med ett lager proteiner kallat en ”korona”. Styva partiklar drog till sig fler komplementproteiner — molekylära markörer som flaggar objekt för immunangrepp — medan mjuka partiklar plockade upp färre av dessa markörer. När båda typerna fanns närvarande snodde de styva partiklarna åt sig flest komplementproteiner och lämnade de mjuka relativt omärkta. Denna kombination av enklare omslutning och tyngre märkning drog de styva partiklarna in i immunceller och skyddade de mjuka från rensning, vilket hjälpte dem att stanna i cirkulationen och nå hjärnan.
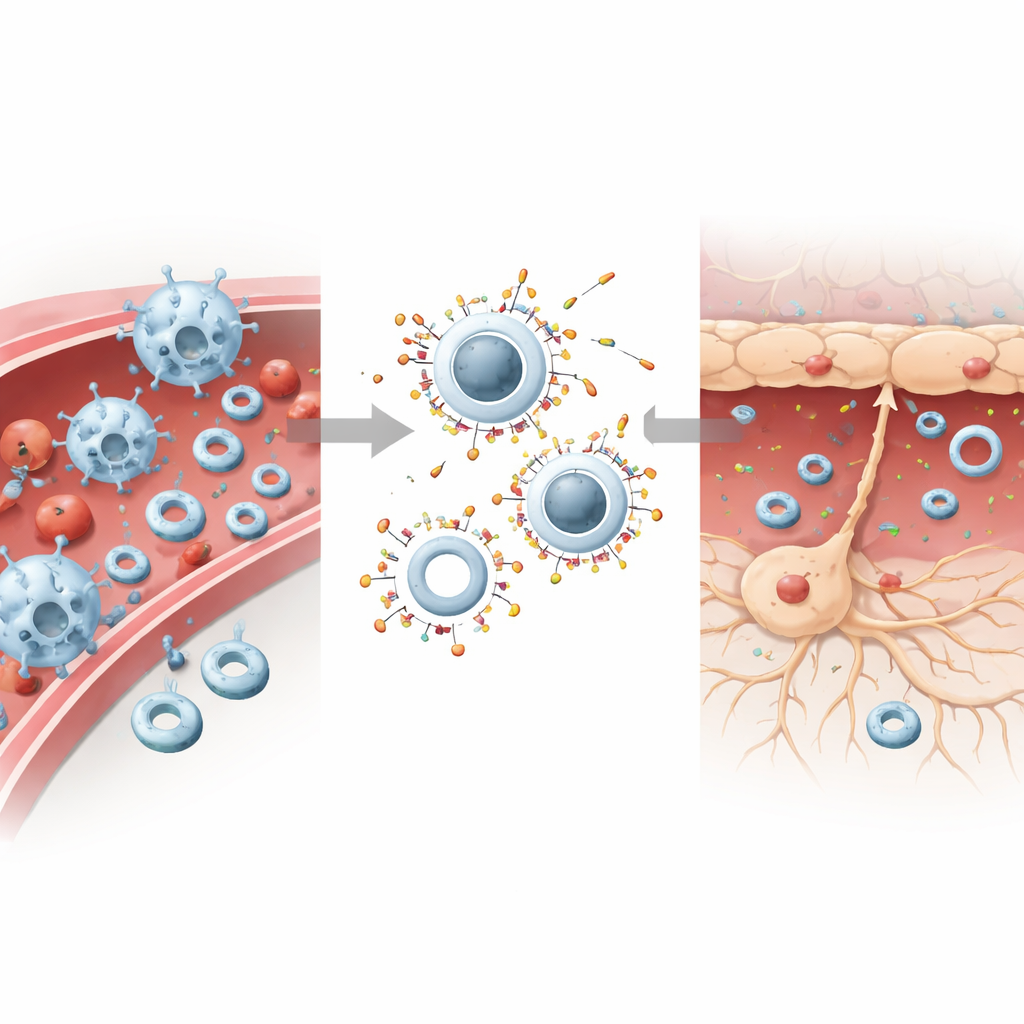
Att dela upp uppgiften: lugna blodet, hela hjärnan
För att omvandla detta beteende till terapi lastade forskarna de styva partiklarna med piceatannol, ett läkemedel som dämpar signaler som driver immuncellernas vidhäftning och invasion, och de mjuka partiklarna med DL-3-n-butylftalid, en neuroprotektiv förening som används för att motverka oxidativ stress och celldöd. I musmodeller för stroke ansamlades de styva läkemedelsladdade partiklarna i levern och immuncellsrika områden, sänkte nivåerna av nyckeladhesionsmolekyler och minskade kraftigt antalet immunceller som trängde in i den skadade hjärnan. De mjuka, läkemedelsladdade partiklarna, nu mindre benägna att bli uppslukade av immunceller, korsade den skadade blod–hjärnbarriären mer effektivt och frigjorde sitt innehåll till stressade neuroner, förbättrade cellöverlevnad och lindrade lokal inflammation.
Från möss till en ny typ av precisionsmedicin
När detta testades under 28 dagar i möss med svår stroke reducerade denna kombination med dubbel styvhet i hög grad hjärnsvullnad och infarktstorlek, bevarade blod–hjärnbarriärens integritet och sänkte markörer för inflammation och celldöd. Mest slående ökade överlevnaden från ungefär en av nio möss till nästan åtta av nio, och neurologisk funktion återhämtade sig mycket bättre än med någon enkelpartikel- eller fri-läkemedelsbehandling. För icke-specialister är huvudbudskapet att matcha läkemedelsbärare till rätt kroppsrum genom att ställa in deras mjukhet eller styvhet kan samordna en tvådelad attack: en i blodet för att stoppa skadliga immunövereaktioner, och en i hjärnan för att främja reparation. Detta ”mekaniskt styrda” leveranskoncept kan sträcka sig bortom stroke till andra sjukdomar där immunsystemet och hjärnan — eller andra organ — är inlåsta i en skadlig dialog.
Citering: Liu, H., Zheng, J., Li, Y. et al. Dual-stiffness nanoparticles for compartment-specific drug delivery in stroke. Nat Commun 17, 3837 (2026). https://doi.org/10.1038/s41467-026-70340-3
Nyckelord: ischemisk stroke, nanopartiklar, läkemedelsleverans, neuroinflammation, precisionsmedicin