Clear Sky Science · de
Nanopartikel mit doppelter Steifigkeit für kompartment-spezifische Medikamentenabgabe beim Schlaganfall
Den Schlaganfall an zwei Fronten angehen
Ein Schlaganfall wird oft als ein „Hirnangriff“ bezeichnet, doch diese Forschung zeigt, dass der Schaden nicht am Gehirn haltmacht. Wenn eine größere Arterie im Gehirn verstopft wird, bricht ein Entzündungssturm sowohl im Blut als auch innerhalb des Gehirns aus. Diese Studie stellt eine clevere Nanomedizin-Strategie vor, bei der eine Partikelart das Immunsystem im Blut beruhigt, während eine andere Art ins Gehirn eindringt, um geschädigte Nervenzellen zur Heilung zu unterstützen — alles aus einer einzigen Injektion.
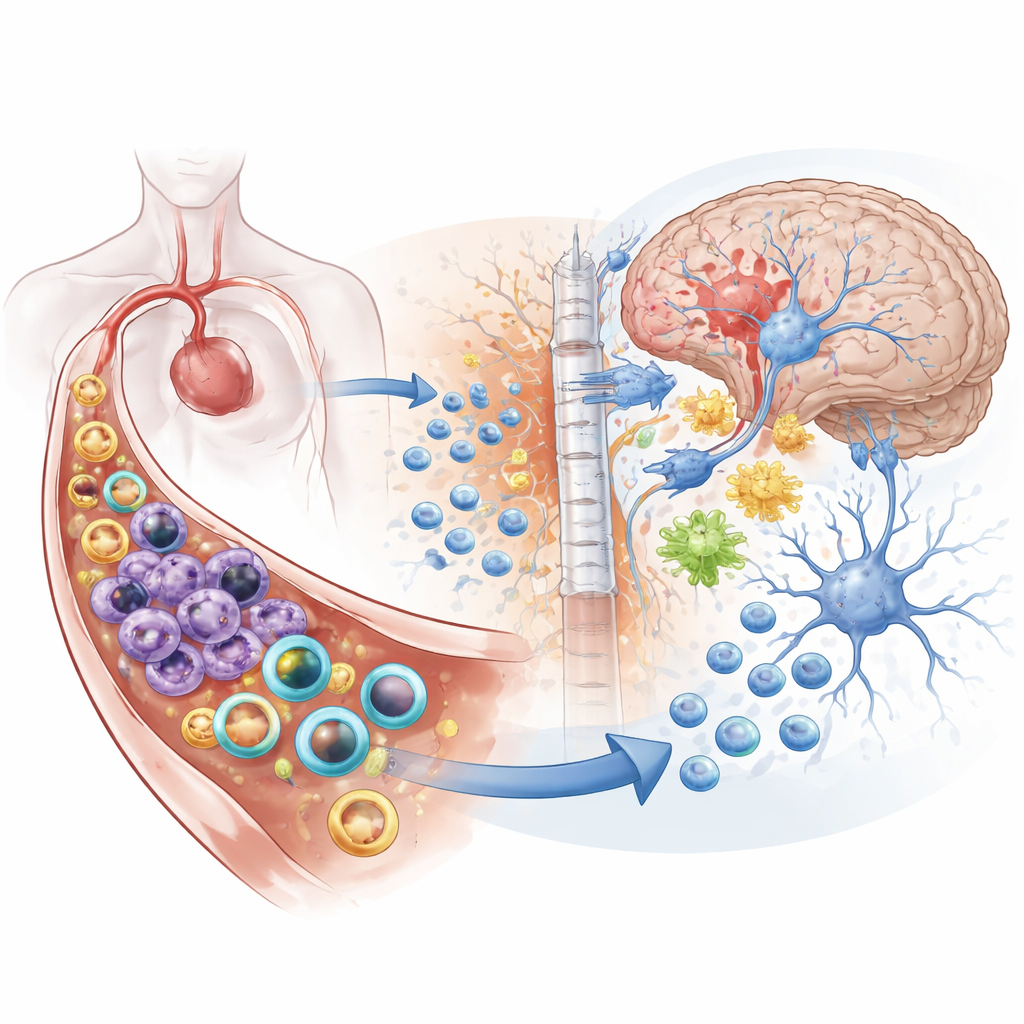
Warum Schlaganfall mehr ist als eine lokale Verletzung
Der ischämische Schlaganfall, verursacht durch ein Blutgerinnsel, das die Durchblutung des Gehirns blockiert, ist die häufigste Form des Schlaganfalls und eine führende Ursache für Tod und Behinderung weltweit. Wenn Hirngewebe Sauerstoff verliert, sterben Nervenzellen, toxische Moleküle werden freigesetzt und die Blut‑Hirn‑Schranke — die Schutzbarriere zwischen Blut und Gehirn — beginnt undicht zu werden. Notrufe gelangen ins Blut und rufen Armeen von Immunzellen wie Neutrophilen und Monozyten herbei. Diese Zellen strömen zum Gehirn, quetschen sich durch Blutgefäße und verschlimmern Schwellungen und Gewebeschäden. Viele heutige Behandlungen zielen entweder darauf ab, das Immunsystem allgemein zu dämpfen oder direkt Neuronen zu schützen, selten jedoch beides koordiniert.
Zwei Arten heilender Partikel entwerfen
Das Forscherteam vermutete, dass das physikalische „Gefühl“ eines Nanopartikels — wie steif oder weich er ist — bestimmen könnte, in welche Zellen er gelangt. Sie bauten zwei nahezu identische Partikel aus zugelassenen Materialien: weiche, nachgiebige Liposomen und steifere Partikel, die durch Einbringen eines festen Polymerkerns in eine ähnliche Lipidhülle entstanden. Beide Typen hatten ähnliche Größe, Ladung und äußere Chemie, aber deutlich unterschiedliche Steifigkeit. In Zellversuchen wurden steife Partikel gierig von Immunzellen aufgenommen, während Neuronen eine klare Vorliebe für die weicheren zeigten. Wurden beide gleichzeitig verabreicht, konzentrierten sich die Immunzellen noch stärker auf die steifen Partikel und ignorierten größtenteils die weichen, sodass letztere in größerer Zahl passieren konnten.
Wie Mechanik und Blutproteine die Partikel lenken
Computersimulationen und biochemische Tests halfen, dieses gespaltene Verhalten zu erklären. Für Zellen erforderte das Umwickeln steifer Partikel weniger Energie, was das Verschlingen erleichterte. Weiche Partikel hafteten zwar gut an der Membran, waren aber schwerer vollständig ins Zellinnere zu ziehen, insbesondere für steife, hochaktive Immunzellen. Gleichzeitig überzog das Blut die Partikel mit einer Proteinschicht, der sogenannten „Korona“. Steife Partikel zogen mehr Komplementproteine an — molekulare Markierungen, die Objekte für einen Immunangriff kennzeichnen — während weiche Partikel weniger dieser Markierungen aufnahmen. Wenn beide Typen gleichzeitig vorhanden waren, beanspruchten die steifen Partikel die Komplementproteine und ließen die weichen relativ unmarkiert. Diese Kombination aus leichterer Aufnahme und stärkerer Markierung zog steife Partikel in Immunzellen und schützte weiche Partikel vor dem Abbau, sodass sie länger zirkulierten und das Gehirn erreichen konnten.
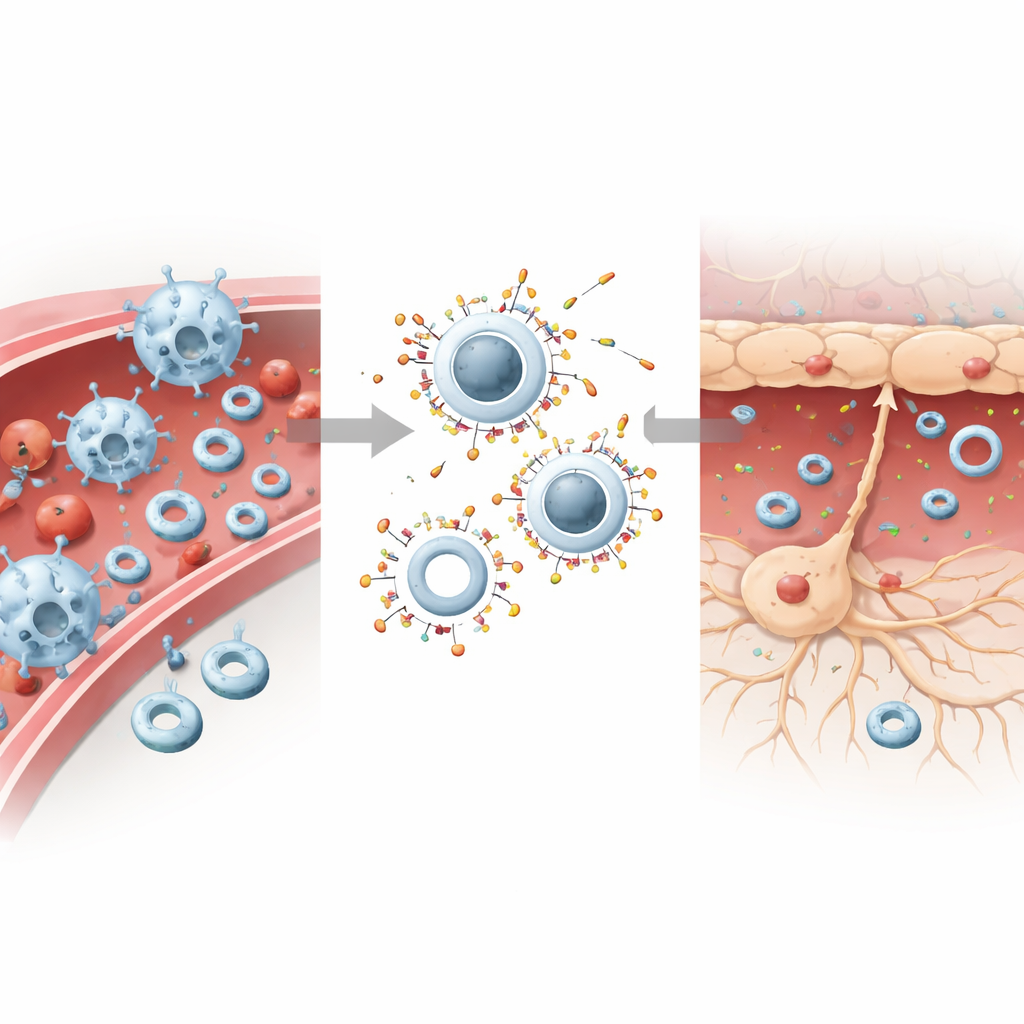
Aufgabenteilung: Blut beruhigen, Gehirn heilen
Um dieses Verhalten therapeutisch zu nutzen, luden die Wissenschaftler die steifen Partikel mit Piceatannol, einem Wirkstoff, der Signale dämpft, die die Adhäsion und Invasion von Immunzellen antreiben, und die weichen Partikel mit DL-3-n-Butylphthalid, einer neuroprotektiven Verbindung, die gegen oxidativen Stress und Zelltod wirkt. In Mausmodellen des Schlaganfalls reichten die steifen, mit Medikament beladenen Partikel in Leber und immunzellreichen Bereichen an und senkten die Werte zentraler Adhäsionsmoleküle, wodurch die Zahl der Immunzellen, die ins verletzte Gehirn eindringen, deutlich reduziert wurde. Die weichen, medikamentbeladenen Partikel, die nun weniger wahrscheinlich von Immunzellen aufgenommen wurden, überquerten die geschädigte Blut‑Hirn‑Schranke effizienter und setzten ihren Wirkstoff an gestressten Neuronen frei, was das Überleben der Zellen verbesserte und lokale Entzündungen linderte.
Von Mäusen zu einer neuen Form der Präzisionsmedizin
Bei Tests über 28 Tage in Mäusen mit schwerem Schlaganfall verringerte diese Doppelsteifigkeits‑Kombination deutlich Hirnschwellungen und Infarktgröße, bewahrte die Integrität der Blut‑Hirn‑Schranke und senkte Marker für Entzündung und Zelltod. Am auffälligsten stieg die Überlebensrate von etwa einer von neun Mäusen auf nahezu acht von neun, und die neurologische Funktion erholte sich deutlich besser als bei Behandlungen mit nur einem Partikeltyp oder freien Medikamenten. Für Laien ist die Kernbotschaft, dass das Anpassen von Wirkstoffträgern an das richtige Körperkompartment durch Feinabstimmung ihrer Weichheit oder Steifigkeit einen zweigleisigen Angriff orchestrieren kann: einen im Blut, um schädliche Immunüberreaktionen zu stoppen, und einen im Gehirn, um die Reparatur zu fördern. Dieses „mechanisch gesteuerte“ Abgabekonzept könnte über Schlaganfall hinaus auf andere Erkrankungen ausgeweitet werden, bei denen Immunsystem und Gehirn — oder andere Organe — in einem schädlichen Dialog stehen.
Zitation: Liu, H., Zheng, J., Li, Y. et al. Dual-stiffness nanoparticles for compartment-specific drug delivery in stroke. Nat Commun 17, 3837 (2026). https://doi.org/10.1038/s41467-026-70340-3
Schlüsselwörter: ischämischer Schlaganfall, Nanopartikel, Arzneimittelabgabe, Neuroinflammation, präzisionsmedizin