Clear Sky Science · it
Nanoparticelle a rigidità doppia per somministrazione di farmaci specifica per compartimento nell’ictus
Colpire l’ictus su due fronti
L’ictus è spesso descritto come un attacco al cervello, ma questa ricerca dimostra che il danno non si limita al cervello. Quando un’arteria cerebrale principale viene bloccata, esplode una tempesta infiammatoria sia nel sangue sia all’interno del cervello stesso. Questo studio introduce una strategia nanomedica intelligente che invia un tipo di particelle piccolissime a calmare il sistema immunitario nel circolo sanguigno mentre un altro tipo si insinua nel cervello per assistere i neuroni danneggiati verso la guarigione — tutto con una singola iniezione.
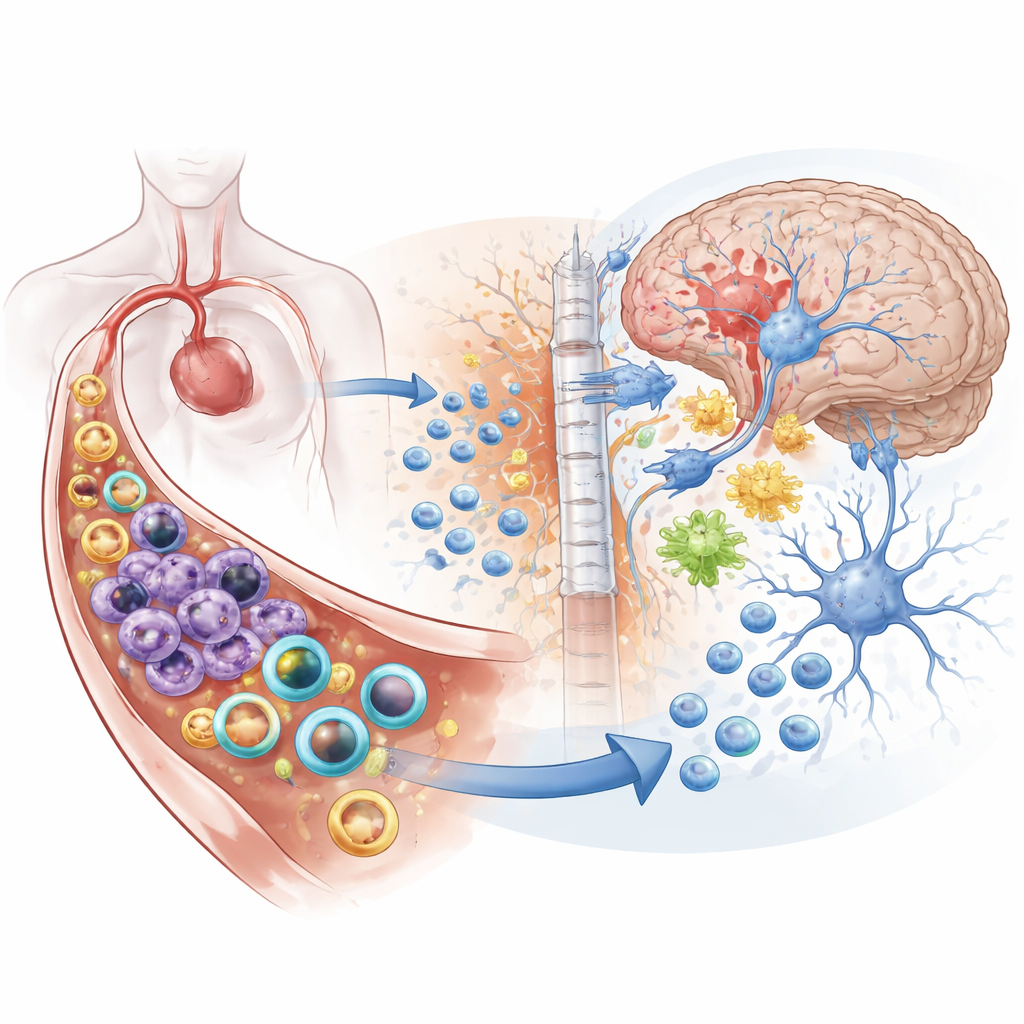
Perché l’ictus è più di una lesione locale
L’ictus ischemico, causato da un coagulo che blocca il flusso sanguigno al cervello, è la forma più comune di ictus e una delle principali cause di morte e disabilità a livello globale. Quando il tessuto cerebrale perde ossigeno, i neuroni muoiono, vengono rilasciate molecole tossiche e la barriera emato-encefalica — la parete protettiva tra sangue e cervello — comincia a diventare permeabile. Segnali di distress si riversano nel flusso sanguigno, richiamando eserciti di cellule immunitarie come neutrofili e monociti. Queste cellule si precipitano verso il cervello, attraversano i vasi e aggravano il rigonfiamento e il danno tissutale. Molti trattamenti attuali si concentrano o sul calmare il sistema immunitario ovunque o sul proteggere direttamente i neuroni, ma raramente fanno entrambe le cose in modo coordinato.
Progettare due tipi di particelle terapeutiche
Il team di ricerca ha ipotizzato che la «sensazione» fisica di una nanoparticella — quanto è rigida o morbida — potesse determinare in quali cellule finisse. Hanno costruito due particelle quasi identiche con materiali approvati: liposomi morbidi e deformabili e particelle più rigide ottenute inserendo un nucleo polimerico solido in un guscio lipidico simile. Entrambi i tipi avevano dimensioni, carica e chimica superficiale simili, ma una rigidità molto diversa. Negli esperimenti cellulari, le particelle rigide venivano avidamente ingerite dalle cellule immunitarie, mentre i neuroni mostravano una chiara preferenza per quelle più morbide. Quando somministrate insieme, le cellule immunitarie si concentravano ancora di più sulle particelle rigide ignorando in larga parte quelle morbide, permettendo a queste ultime di attraversare il circolo in numero maggiore.
Come meccanica e proteine del sangue guidano le particelle
Simulazioni al computer e test biochimici hanno aiutato a spiegare questo comportamento divergente. Le particelle rigide richiedevano meno energia perché le cellule potessero avvolgere la loro membrana attorno a esse, rendendo più facile la fagocitosi. Le particelle morbide aderivano bene alla membrana ma erano più difficili da estrarre completamente all’interno della cellula, specialmente per cellule immunitarie rigide e altamente attive. Allo stesso tempo, il sangue rivestiva le particelle con uno strato proteico noto come «corona». Le particelle rigide attiravano più proteine del complemento — marcatori molecolari che segnalano gli oggetti per l’attacco immunitario — mentre le particelle morbide ne raccoglievano di meno. Quando erano presenti entrambi i tipi, le particelle rigide monopolizzavano le proteine del complemento, lasciando quelle morbide relativamente non marcate. Questa combinazione di più facile ingestione e marcatura maggiore attirava le particelle rigide nelle cellule immunitarie e schermava le particelle morbide dalla clearance, aiutandole a rimanere in circolazione e a raggiungere il cervello.
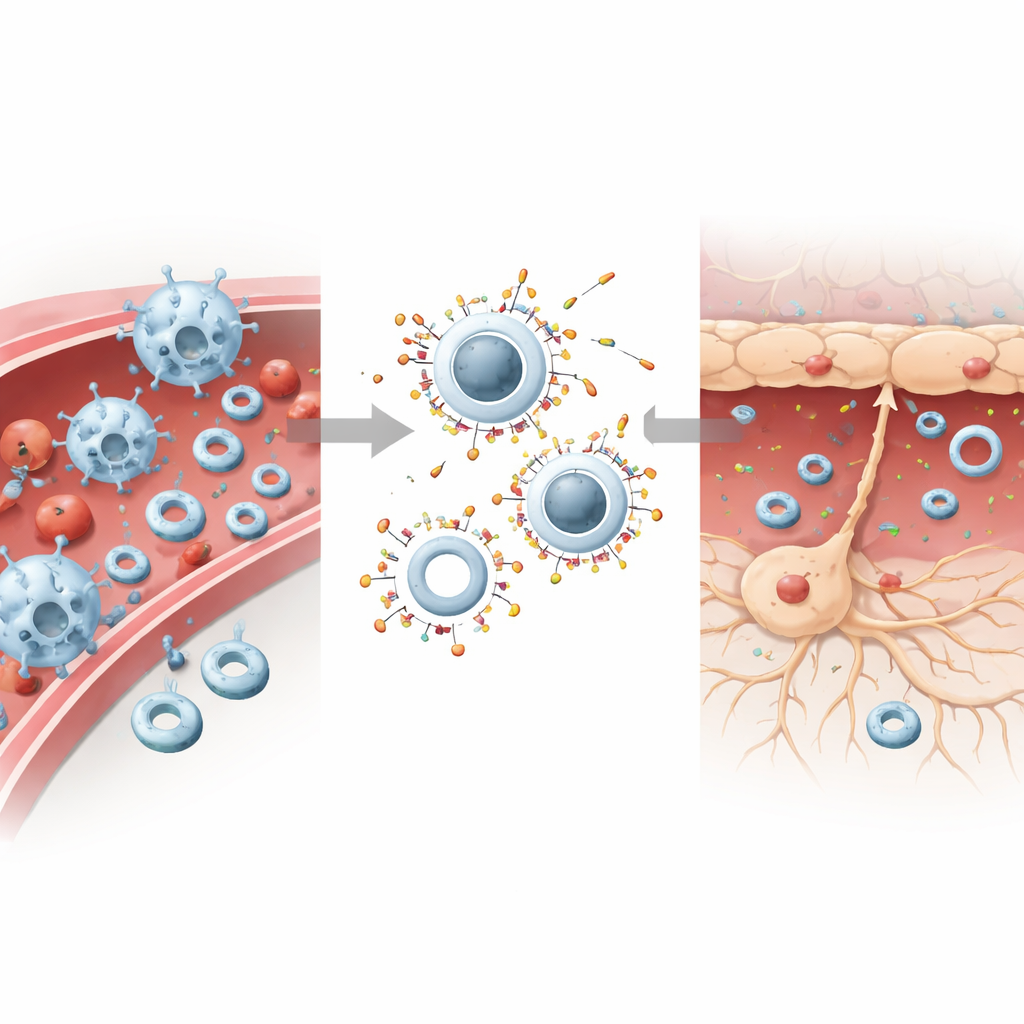
Dividere il compito: calmare il sangue, curare il cervello
Per trasformare questo comportamento in terapia, gli scienziati hanno caricato le particelle rigide con piceatannolo, un farmaco che attenua i segnali che guidano l’adesione e l’invasione delle cellule immunitarie, e hanno caricato le particelle morbide con DL-3-n-butilftalide, un composto neuroprotettivo usato per contrastare lo stress ossidativo e la morte cellulare. Nei modelli murini di ictus, le particelle rigide caricate di farmaco si accumulavano nel fegato e nelle aree ricche di cellule immunitarie, riducendo i livelli di molecole chiave di adesione e diminuendo nettamente il numero di cellule immunitarie che entravano nel cervello danneggiato. Le particelle morbide caricate di farmaco, meno soggette a essere ingerite dalle cellule immunitarie, attraversavano più efficacemente la barriera emato-encefalica danneggiata e rilasciavano il loro carico ai neuroni stressati, migliorando la sopravvivenza cellulare e attenuando l’infiammazione locale.
Dai topi a una nuova forma di medicina di precisione
Sperimentata per 28 giorni in topi con ictus severo, questa combinazione a doppia rigidità ha ridotto notevolmente il rigonfiamento cerebrale e la dimensione dell’infarto, preservato l’integrità della barriera emato-encefalica e abbassato i marker di infiammazione e morte cellulare. Ciò che colpisce di più è che la sopravvivenza è salita da circa uno su nove topi a quasi otto su nove, e la funzione neurologica si è ripresa molto meglio rispetto a qualsiasi trattamento con una singola particella o con farmaco libero. Per il pubblico non specialista, il messaggio chiave è che abbinare i vettori dei farmaci al compartimento corporeo giusto regolando la loro morbidezza o rigidità può orchestrare un attacco a due punte: uno nel sangue per fermare la sovrareazione immunitaria dannosa e uno nel cervello per favorire la riparazione. Questo concetto di somministrazione «guidata meccanicamente» potrebbe estendersi oltre l’ictus ad altre malattie in cui il sistema immunitario e il cervello — o altri organi — sono intrappolati in un dialogo dannoso.
Citazione: Liu, H., Zheng, J., Li, Y. et al. Dual-stiffness nanoparticles for compartment-specific drug delivery in stroke. Nat Commun 17, 3837 (2026). https://doi.org/10.1038/s41467-026-70340-3
Parole chiave: ictus ischemico, nanoparticelle, somministrazione di farmaci, neuroinfiammazione, medicina di precisione