Clear Sky Science · pt
Nanopartículas de dupla rigidez para entrega de fármacos específica por compartimento no AVC
Alvejando o AVC em Dois Frentes
O AVC costuma ser descrito como um ataque ao cérebro, mas esta pesquisa mostra que o dano não se limita ao tecido cerebral. Quando uma artéria importante no cérebro fica bloqueada, uma tempestade inflamatória irrompe tanto no sangue quanto dentro do próprio cérebro. Este estudo apresenta uma estratégia engenhosa de nanomedicina que envia um tipo de partícula minúscula para acalmar o sistema imunológico na corrente sanguínea enquanto outro tipo penetra no cérebro para ajudar neurônios danificados a se recuperar — tudo a partir de uma única injeção.
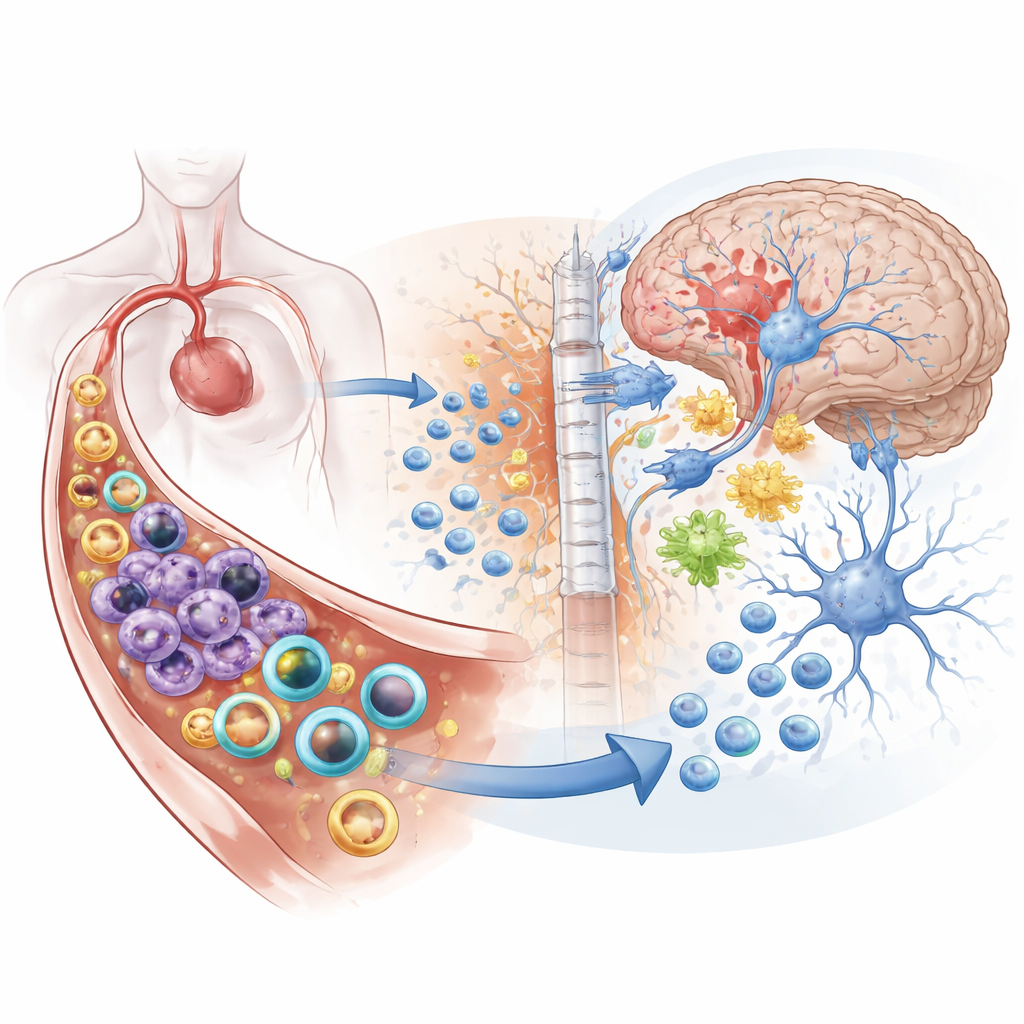
Por que o AVC é Mais do que uma Lesão Local
O AVC isquêmico, causado por um coágulo que bloqueia o fluxo sanguíneo ao cérebro, é a forma mais comum de AVC e uma das principais causas de morte e incapacidade no mundo. Quando o tecido cerebral perde oxigênio, neurônios morrem, moléculas tóxicas são liberadas e a barreira hematoencefálica — a parede protetora entre sangue e cérebro — começa a vazar. Sinais de estresse se derramam na corrente sanguínea, convocando exércitos de células imunes como neutrófilos e monócitos. Essas células correm em direção ao cérebro, atravessam os vasos e agravam o inchaço e o dano tecidual. Muitos tratamentos atuais focam ou em silenciar o sistema imunológico de forma ampla ou em proteger diretamente os neurônios, raramente fazendo os dois de maneira coordenada.
Projetando Dois Tipos de Partículas Reparadoras
A equipe de pesquisa supôs que a "sensação" física de uma nanopartícula — quão rígida ou macia ela é — poderia determinar em quais células ela acaba sendo internalizada. Eles construíram duas partículas quase idênticas a partir de materiais aprovados: lipossomas macios e flexíveis e partículas mais rígidas formadas por um núcleo polimérico sólido dentro de uma concha lipídica semelhante. Ambos os tipos tinham tamanho, carga e química superficial semelhantes, mas rigidez drasticamente diferente. Em experimentos celulares, as partículas rígidas eram avidamente engolidas por células imunes, enquanto os neurônios mostraram preferência clara pelas mais macias. Quando administradas juntas, as células imunes concentraram-se ainda mais nas partículas rígidas e em grande parte ignoraram as macias, permitindo que estas últimas passassem em maior número.
Como a Mecânica e as Proteínas Sanguíneas Guiam as Partículas
Simulações computacionais e testes bioquímicos ajudaram a explicar esse comportamento dividido. Partículas rígidas exigiam menos energia para que as células envolvessem suas membranas ao redor delas, tornando-as mais fáceis de englobar. Partículas macias aderiam bem à membrana, mas eram mais difíceis de puxar totalmente para dentro, especialmente para células imunes rígidas e altamente ativas. Ao mesmo tempo, o sangue revestia as partículas com uma camada de proteínas conhecida como "coroa". Partículas rígidas atraíam mais proteínas do complemento — marcadores moleculares que sinalizam objetos para ataque imune — enquanto partículas macias captavam menos dessas marcas. Quando ambos os tipos estavam presentes, as rígidas monopolizavam as proteínas do complemento, deixando as macias relativamente sem marcação. Essa combinação de englobamento facilitado e marcação mais intensa puxou as partículas rígidas para dentro das células imunes e protegeu as partículas macias da depuração, ajudando-as a permanecer na circulação e alcançar o cérebro.
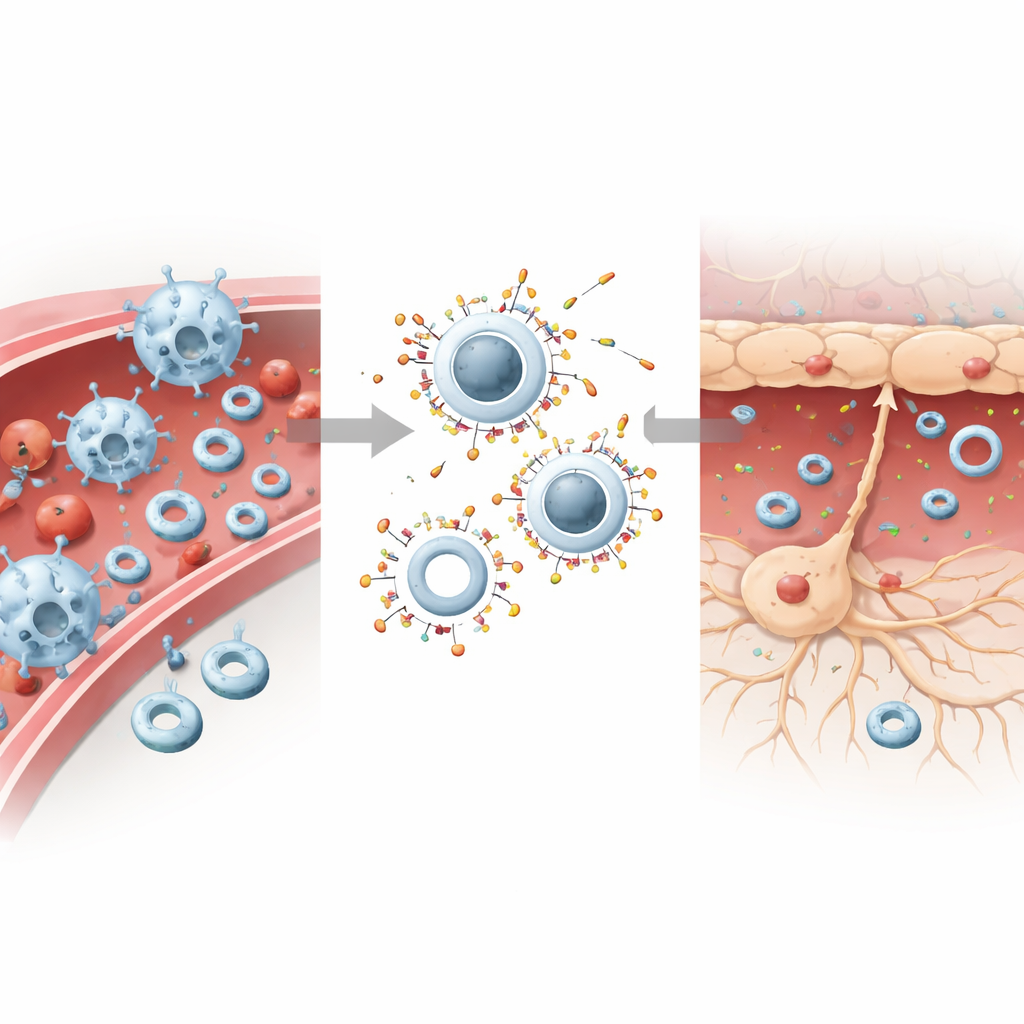
Dividindo a Tarefa: Acalmar o Sangue, Curar o Cérebro
Para transformar esse comportamento em terapia, os cientistas carregaram as partículas rígidas com piceatannol, um fármaco que reduz sinais que impulsionam a adesão e invasão de células imunes, e carregaram as partículas macias com DL-3-n-butilftalida, um composto neuroprotetor usado para combater o estresse oxidativo e a morte celular. Em modelos murinos de AVC, as partículas rígidas carregadas com fármaco se acumularam no fígado e em áreas ricas em células imunes, reduzindo os níveis de moléculas de adesão-chave e diminuindo drasticamente o número de células imunes que entravam no cérebro lesionado. As partículas macias carregadas com fármaco, agora menos propensas a serem engolidas por células imunes, atravessaram mais eficientemente a barreira hematoencefálica danificada e liberaram seu conteúdo em neurônios estressados, melhorando a sobrevivência celular e aliviando a inflamação local.
De Camundongos a um Novo Tipo de Medicina de Precisão
Quando testada por 28 dias em camundongos com AVC severo, essa combinação de dupla rigidez reduziu muito o inchaço cerebral e o tamanho do infarto, preservou a integridade da barreira hematoencefálica e diminuiu marcadores de inflamação e morte celular. O mais notável foi que a sobrevida aumentou de cerca de um em nove camundongos para quase oito em nove, e a recuperação da função neurológica foi muito melhor do que com qualquer tratamento de partícula única ou droga livre. Para não especialistas, a mensagem central é que emparelhar transportadores de fármacos ao compartimento corporal certo ajustando sua maciez ou rigidez pode orquestrar um ataque em duas frentes: um no sangue para deter reações imunes nocivas e outro no cérebro para promover a reparação. Esse conceito de entrega "guiada mecanicamente" poderia se estender além do AVC para outras doenças nas quais o sistema imunológico e o cérebro — ou outros órgãos — estão presos em um diálogo prejudicial.
Citação: Liu, H., Zheng, J., Li, Y. et al. Dual-stiffness nanoparticles for compartment-specific drug delivery in stroke. Nat Commun 17, 3837 (2026). https://doi.org/10.1038/s41467-026-70340-3
Palavras-chave: acidente isquêmico, nanopartículas, entrega de fármacos, neuroinflamação, medicina de precisão