Clear Sky Science · es
Nanopartículas de doble rigidez para la administración de fármacos específica por compartimento en el ictus
Atacar el ictus en dos frentes
El ictus suele describirse como un ataque al cerebro, pero esta investigación muestra que el daño no se limita a él. Cuando una arteria cerebral importante queda obstruida, se desencadena una tormenta inflamatoria tanto en la sangre como dentro del propio cerebro. Este estudio presenta una estrategia ingeniosa de nanomedicina que envía un tipo de partículas diminutas para calmar al sistema inmunitario en el torrente sanguíneo mientras que otro tipo se desliza hacia el cerebro para atender las neuronas dañadas y promover su recuperación —todo a partir de una única inyección.
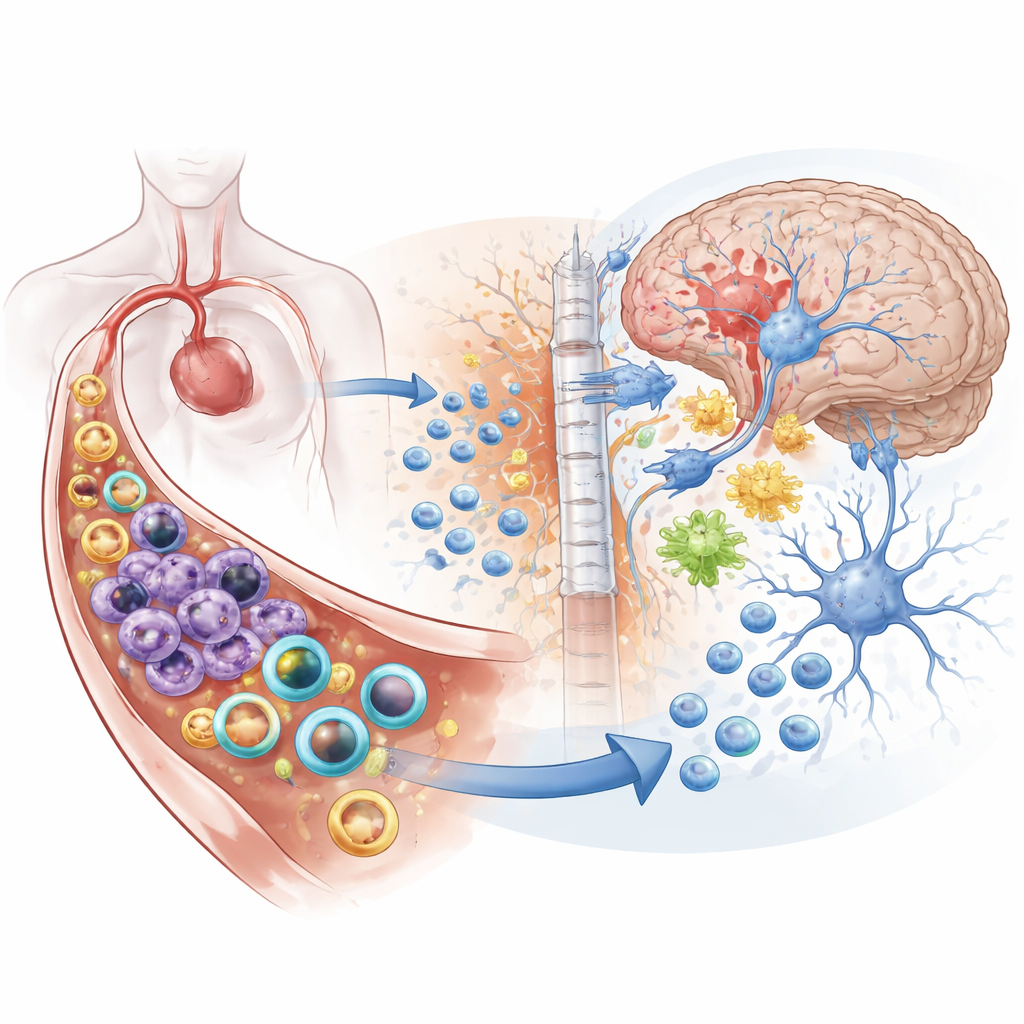
Por qué el ictus es más que una lesión local
El ictus isquémico, causado por un coágulo que bloquea el flujo sanguíneo al cerebro, es la forma más común de ictus y una de las principales causas de muerte y discapacidad en todo el mundo. Cuando el tejido cerebral pierde oxígeno, las neuronas mueren, se liberan moléculas tóxicas y la barrera hematoencefálica —la pared protectora entre la sangre y el cerebro— empieza a filtrarse. Señales de alarma llegan al torrente sanguíneo, reclutando ejércitos de células inmunitarias como neutrófilos y monocitos. Estas células se dirigen al cerebro, atraviesan los vasos sanguíneos y empeoran la inflamación y el daño tisular. Muchos tratamientos actuales se centran o bien en calmar el sistema inmunitario de forma general o en proteger directamente a las neuronas, pero rara vez lo hacen de forma coordinada.
Diseñando dos tipos de partículas reparadoras
El equipo de investigación razonó que la “sensación” física de una nanopartícula —qué tan rígida o blanda es— podría determinar en qué células termina. Construyeron dos partículas casi idénticas a partir de materiales aprobados: liposomas blandos y flexibles y partículas más rígidas formadas al colocar un núcleo polimérico sólido dentro de una envoltura lipídica similar. Ambos tipos tenían tamaño, carga y química superficial semejantes, pero una rigidez muy distinta. En experimentos celulares, las partículas rígidas fueron devoradas vorazmente por las células inmunitarias, mientras que las neuronas mostraron una clara preferencia por las más blandas. Cuando se administraron juntas, las células inmunitarias se enfocaron aún más en las rígidas e ignoraron en gran medida las blandas, permitiendo que estas últimas circularan en mayor número.
Cómo la mecánica y las proteínas plasmáticas dirigen a las partículas
Simulaciones por ordenador y pruebas bioquímicas ayudaron a explicar este comportamiento divergente. Las partículas rígidas requerían menos energía para que las células envolvieran sus membranas alrededor de ellas, facilitando su ingestión. Las partículas blandas se adherían bien a la membrana pero eran más difíciles de introducir completamente, especialmente para células inmunitarias rígidas y altamente activas. Al mismo tiempo, la sangre recubrió las partículas con una capa de proteínas conocida como “corona”. Las partículas rígidas atrajeron más proteínas del complemento —etiquetas moleculares que marcan objetos para el ataque inmunitario—, mientras que las blandas recogieron menos de estas señales. Cuando ambos tipos estaban presentes, las rígidas acaparaban las proteínas del complemento, dejando a las blandas relativamente sin etiquetar. Esta combinación de una ingestión más fácil y un etiquetado más intenso arrastró a las partículas rígidas hacia las células inmunitarias y protegió a las blandas de la eliminación, ayudándolas a permanecer en circulación y alcanzar el cerebro.
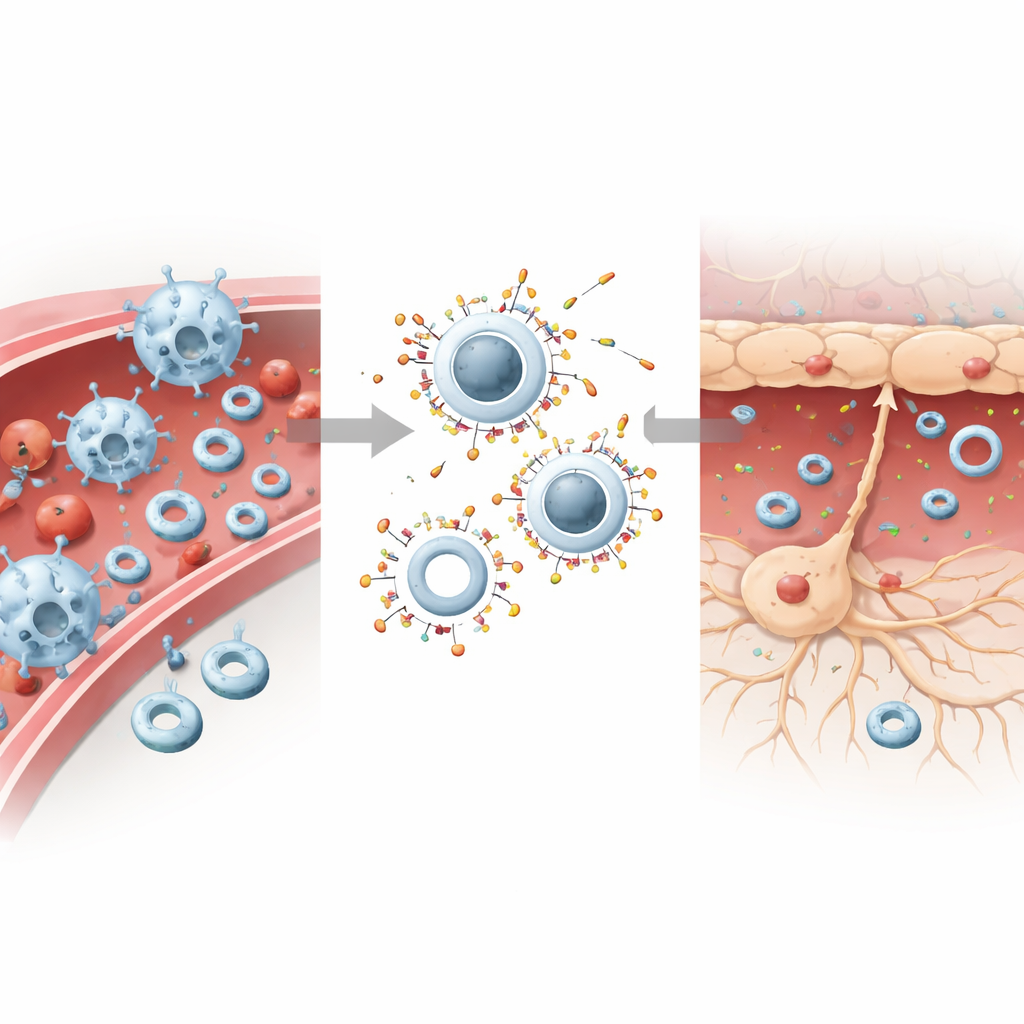
Dividir la tarea: calmar la sangre, sanar el cerebro
Para convertir este comportamiento en terapia, los científicos cargaron las partículas rígidas con piceatannol, un fármaco que atenúa las señales que impulsan la adhesión e invasión de las células inmunitarias, y cargaron las partículas blandas con DL-3-n-butilftalido, un compuesto neuroprotector usado para contrarrestar el estrés oxidativo y la muerte celular. En modelos murinos de ictus, las partículas rígidas cargadas con el fármaco se acumularon en el hígado y en áreas ricas en células inmunitarias, reduciendo los niveles de moléculas de adhesión clave y disminuyendo drásticamente el número de células inmunitarias que entraban en el cerebro lesionado. Las partículas blandas cargadas con fármaco, ahora menos propensas a ser engullidas por las células inmunitarias, cruzaron con mayor eficacia la barrera hematoencefálica dañada y liberaron su carga en las neuronas estresadas, mejorando la supervivencia celular y aliviando la inflamación local.
De los ratones a un nuevo tipo de medicina de precisión
Cuando se probó durante 28 días en ratones con ictus severo, esta combinación de doble rigidez redujo considerablemente la hinchazón cerebral y el tamaño del infarto, preservó la integridad de la barrera hematoencefálica y disminuyó los marcadores de inflamación y muerte celular. Lo más llamativo fue que la supervivencia pasó de aproximadamente uno de cada nueve ratones a casi ocho de cada nueve, y la función neurológica se recuperó mucho mejor que con cualquier tratamiento de partícula única o fármaco libre. Para el público no especializado, el mensaje clave es que adaptar los portadores de fármacos al compartimento corporal correcto ajustando su blandura o rigidez puede orquestar un ataque en dos frentes: uno en la sangre para detener la sobrerreacción inmunitaria nociva, y otro en el cerebro para favorecer la reparación. Este concepto de entrega “guiada mecánicamente” podría aplicarse más allá del ictus a otras enfermedades en las que el sistema inmunitario y el cerebro —u otros órganos— mantienen un diálogo dañino.
Cita: Liu, H., Zheng, J., Li, Y. et al. Dual-stiffness nanoparticles for compartment-specific drug delivery in stroke. Nat Commun 17, 3837 (2026). https://doi.org/10.1038/s41467-026-70340-3
Palabras clave: ictus isquémico, nanopartículas, administración de fármacos, neuroinflamación, medicina de precisión