Clear Sky Science · fr
Nanoparticules à rigidité double pour une délivrance de médicaments spécifique aux compartiments dans l’AVC
Cibler l’AVC sur deux fronts
L’accident vasculaire cérébral est souvent décrit comme une attaque du cerveau, mais cette recherche montre que les dégâts ne se limitent pas à l’organe. Lorsqu’une grosse artère cérébrale est obstruée, une tempête inflammatoire éclate à la fois dans le sang et à l’intérieur du cerveau. Cette étude présente une stratégie nanomédicale ingénieuse qui envoie un type de particules miniatures pour calmer le système immunitaire dans la circulation sanguine tandis qu’un autre type se faufile dans le cerveau pour aider les neurones endommagés à retrouver la santé — le tout à partir d’une seule injection.
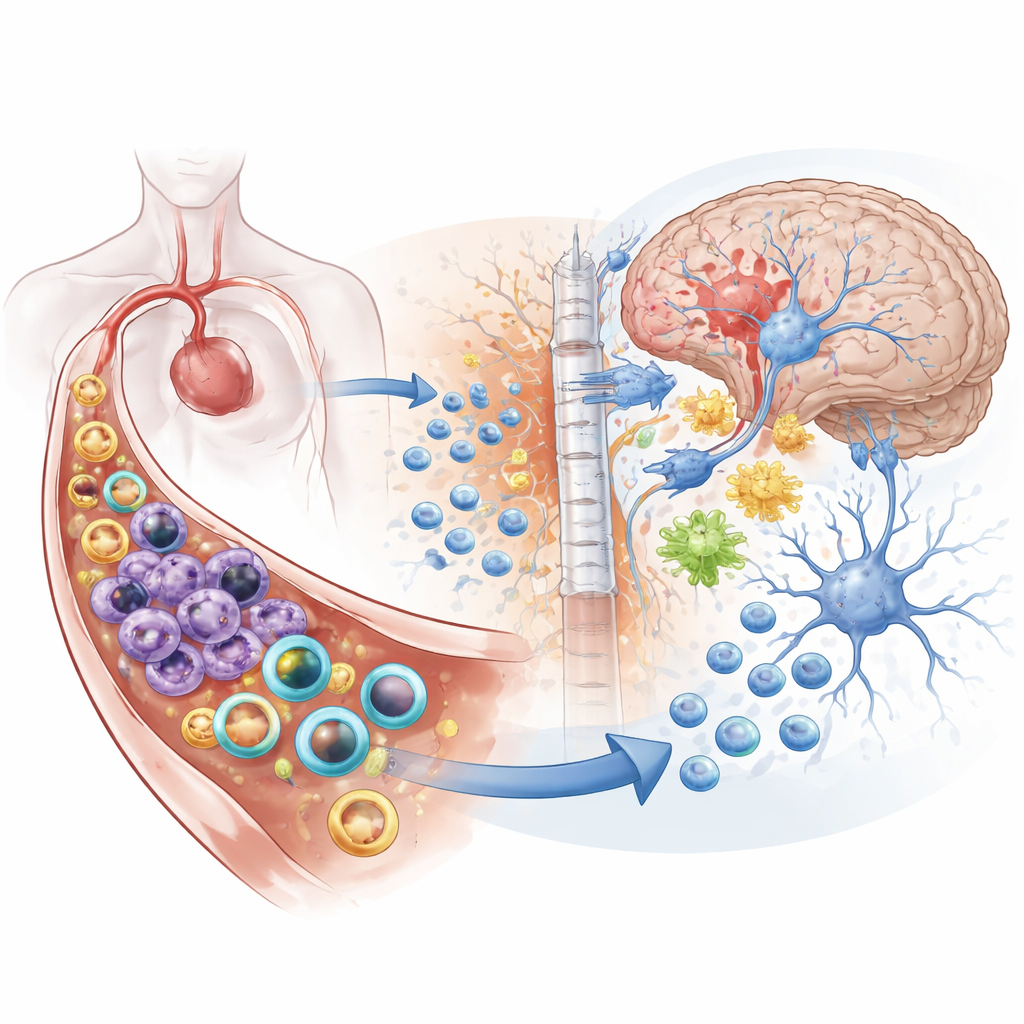
Pourquoi l’AVC dépasse une lésion locale
L’accident ischémique cérébral, causé par un caillot qui bloque l’apport sanguin au cerveau, est la forme la plus fréquente d’AVC et une cause majeure de décès et de handicap dans le monde. Lorsque le tissu cérébral manque d’oxygène, les neurones meurent, des molécules toxiques sont libérées et la barrière hémato‑encéphalique — la paroi protectrice entre le sang et le cerveau — commence à fuir. Des signaux de détresse se répandent dans la circulation, appelant des armées de cellules immunitaires comme les neutrophiles et les monocytes. Ces cellules affluent vers le cerveau, traversent les vaisseaux sanguins et aggravent œdème et lésions tissulaires. De nombreux traitements actuels visent soit à inhiber globalement le système immunitaire, soit à protéger directement les neurones, mais rarement les deux de façon coordonnée.
Concevoir deux types de particules réparatrices
L’équipe de recherche a émis l’hypothèse que la « sensation » physique d’une nanoparticule — sa rigidité ou sa souplesse — pourrait déterminer quelles cellules l’engloutissent. Ils ont construit deux particules presque identiques à partir de matériaux approuvés : des liposomes mous et déformables et des particules plus rigides obtenues en plaçant un cœur polymère solide dans une enveloppe lipidique similaire. Les deux types avaient des tailles, charges et chimie de surface comparables, mais une rigidité très différente. Dans des expériences cellulaires, les particules rigides étaient avidement phagocytées par les cellules immunitaires, tandis que les neurones montraient une nette préférence pour les particules plus souples. Lorsqu’on administrait les deux ensembles, les cellules immunitaires se focalisaient encore davantage sur les particules rigides et ignoraient en grande partie les particules souples, permettant à ces dernières de circuler en plus grand nombre.
Comment la mécanique et les protéines sanguines dirigent les particules
Des simulations informatiques et des tests biochimiques ont aidé à expliquer ce comportement différencié. Les particules rigides nécessitaient moins d’énergie pour que la membrane cellulaire s’enroule autour d’elles, ce qui les rendait plus faciles à engloutir. Les particules souples adhéraient bien à la membrane mais étaient plus difficiles à extraire entièrement à l’intérieur de la cellule, en particulier pour des cellules immunitaires rigides et très actives. Parallèlement, le sang recouvrait les particules d’une couche de protéines appelée « couronne ». Les particules rigides attiraient davantage de protéines du complément — des marquages moléculaires qui signalent un objet pour attaque immunitaire — tandis que les particules souples en capturaient moins. Lorsque les deux types étaient présents, les particules rigides accaparaient les protéines du complément, laissant les particules souples relativement non marquées. Cette combinaison d’une internalisation facilitée et d’un marquage plus important entraînait les particules rigides vers les cellules immunitaires et protégeait les particules souples de l’élimination, leur permettant de rester en circulation et d’atteindre le cerveau.
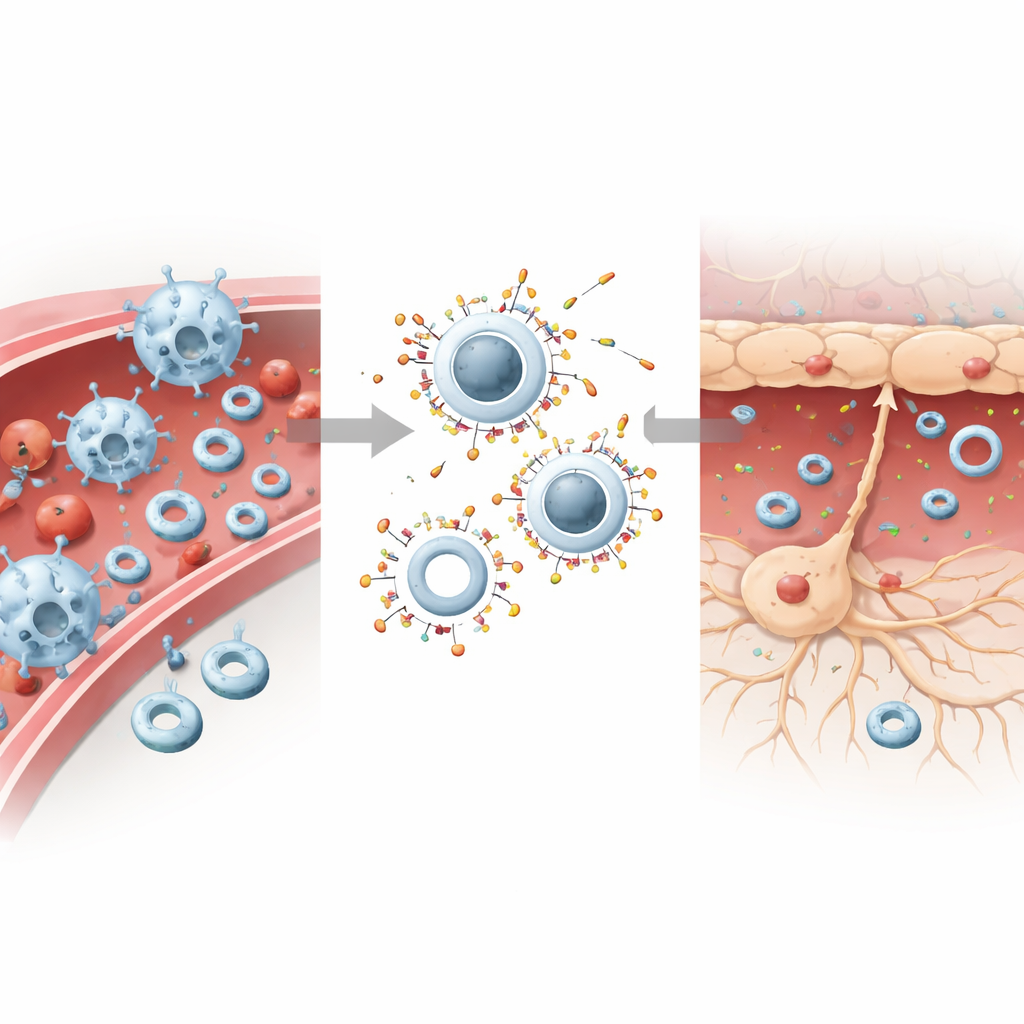
Répartir la tâche : calmer le sang, soigner le cerveau
Pour transformer ce comportement en thérapie, les scientifiques ont chargé les particules rigides avec du piceatannol, un médicament qui atténue les signaux favorisant l’adhésion et l’invasion des cellules immunitaires, et ont chargé les particules souples avec du DL‑3‑n‑butylphthalide, un composé neuroprotecteur utilisé pour contrer le stress oxydatif et la mort cellulaire. Chez des souris modèles d’AVC, les particules rigides chargées se sont accumulées dans le foie et les zones riches en cellules immunitaires, réduisant les niveaux de molécules d’adhésion clés et diminuant fortement le nombre de cellules immunitaires pénétrant dans le cerveau blessé. Les particules souples chargées, désormais moins susceptibles d’être phagocytées, ont franchi plus efficacement la barrière hémato‑encéphalique endommagée et libéré leur cargaison aux neurones stressés, améliorant la survie cellulaire et atténuant l’inflammation locale.
Des souris vers une nouvelle forme de médecine de précision
Testée sur 28 jours chez des souris victimes d’un AVC sévère, cette combinaison à rigidité double a fortement réduit l’œdème cérébral et la taille de l’infarctus, préservé l’intégrité de la barrière hémato‑encéphalique et abaissé les marqueurs d’inflammation et de mort cellulaire. Fait le plus marquant : la survie est passée d’environ une souris sur neuf à près de huit sur neuf, et la récupération neurologique a été bien meilleure qu’avec un traitement à particule unique ou un médicament libre. Pour les non‑spécialistes, le message clé est que l’adaptation des vecteurs médicamenteux au compartiment corporel approprié en ajustant leur souplesse ou rigidité peut orchestrer une attaque en deux temps : une dans le sang pour stopper la réaction immunitaire nocive, et une dans le cerveau pour favoriser la réparation. Ce concept de délivrance « guidée mécaniquement » pourrait s’étendre au‑delà de l’AVC à d’autres maladies où le système immunitaire et le cerveau — ou d’autres organes — sont engagés dans un dialogue délétère.
Citation: Liu, H., Zheng, J., Li, Y. et al. Dual-stiffness nanoparticles for compartment-specific drug delivery in stroke. Nat Commun 17, 3837 (2026). https://doi.org/10.1038/s41467-026-70340-3
Mots-clés: accident ischémique cérébral, nanoparticules, <keyword>neuroinflammation, médecine de précision