Clear Sky Science · nl
Nanodeeltjes met dubbele stijfheid voor compartimentspecifieke medicijnafgifte bij beroerte
De beroerte op twee fronten aanpakken
Beroerte wordt vaak omschreven als een aanval op de hersenen, maar dit onderzoek toont aan dat de schade niet bij de hersenen stopt. Wanneer een grote slagader in de hersenen wordt geblokkeerd, breekt er een storm van ontsteking los, zowel in het bloed als binnenin de hersenen zelf. Deze studie introduceert een slimme nanomedicijnstrategie die één type deeltje inzet om het immuunsysteem in de bloedbaan te kalmeren, terwijl een ander type de hersenen binnendringt om beschadigde zenuwcellen te helpen herstellen — allemaal vanuit één injectie.
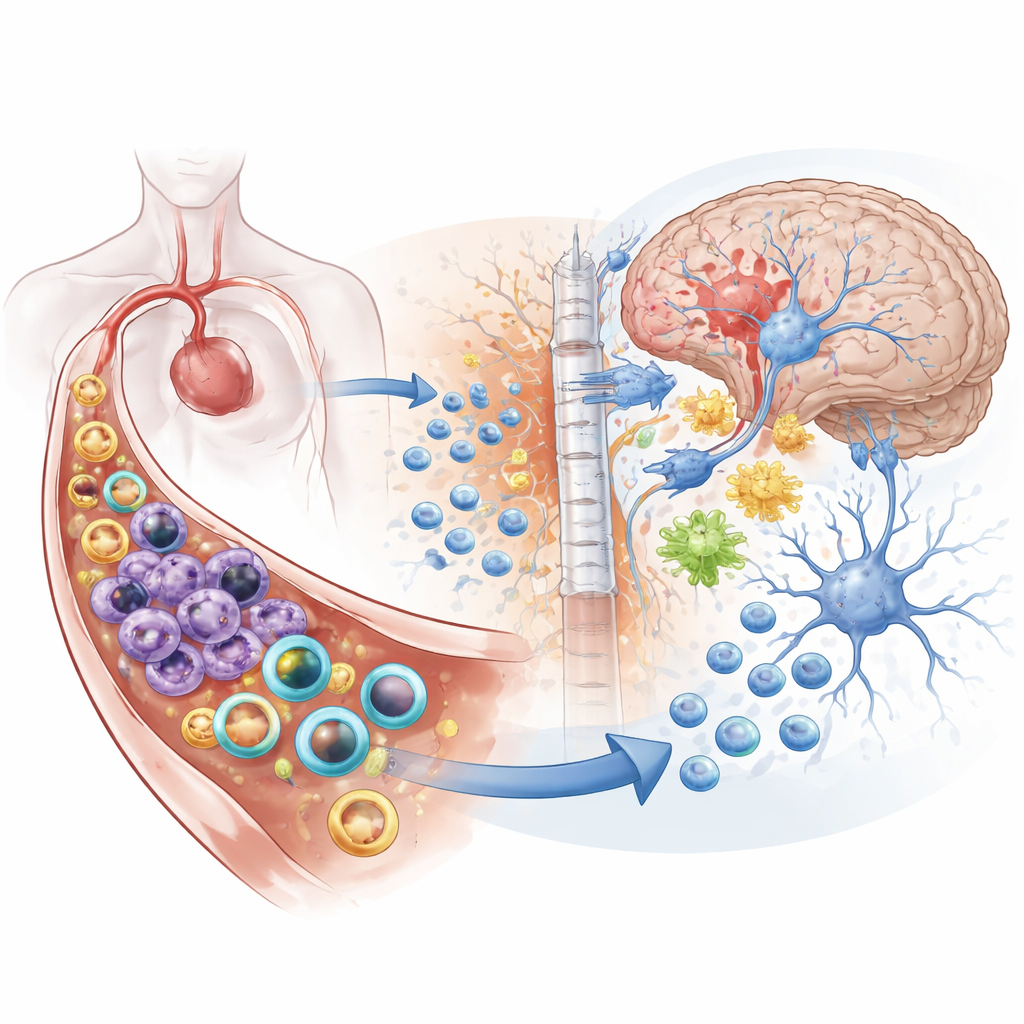
Waarom een beroerte meer is dan een lokale verwonding
Ischemische beroerte, veroorzaakt door een stolsel dat de bloedtoevoer naar de hersenen blokkeert, is de meest voorkomende vorm van beroerte en een belangrijke oorzaak van overlijden en invaliditeit wereldwijd. Wanneer hersenweefsel zuurstof verliest, sterven zenuwcellen, komen toxische moleculen vrij en begint de bloed-hersenbarrière — de beschermende wand tussen bloed en hersenen — te lekken. Noodsignalen stromen het bloed in en roepen legers van immuuncellen op, zoals neutrofielen en monocyten. Deze cellen schieten naar de hersenen, persen zich door bloedvaten en verergeren zwelling en weefselschade. Veel huidige behandelingen richten zich ofwel op het dempen van het immuunsysteem overal, of op het direct beschermen van neuronen, maar zelden beide op een gecoördineerde manier.
Ontwerpen van twee soorten helende deeltjes
Het onderzoeksteam bedacht dat het fysieke “gevoel” van een nanodeeltje — hoe stijf of zacht het is — zou kunnen bepalen in welke cellen het terechtkomt. Ze bouwden twee bijna identieke deeltjes van goedgekeurde materialen: zachte, veerkrachtige liposomen en stijvere deeltjes gemaakt door een vaste polymeerkernt binnen een vergelijkbare lipideomhulling te plaatsen. Beide types hadden vergelijkbare grootte, lading en buitenchemie, maar een drastisch verschillende stijfheid. In celexperimenten werden stijve deeltjes gretig opgenomen door immuuncellen, terwijl neuronen een duidelijke voorkeur toonden voor de zachtere deeltjes. Wanneer beide tegelijk werden toegediend, concentreerden immuuncellen zich nog meer op de stijve deeltjes en negeerden grotendeels de zachte, waardoor die in grotere aantallen konden passeren.
Hoe mechanica en bloedproteïnen de deeltjes sturen
Computersimulaties en biochemische tests hielpen dit verdeelde gedrag verklaren. Voor stijve deeltjes was minder energie nodig om cellen hun membranen eromheen te laten vouwen, waardoor ze makkelijker werden ingesloten. Zachte deeltjes hechtten goed aan het membraan maar waren moeilijker volledig naar binnen te trekken, vooral voor stijve, zeer actieve immuuncellen. Tegelijkertijd bedekte het bloed de deeltjes met een laag eiwitten, bekend als een “corona.” Stijve deeltjes trokken meer complementproteïnen aan — moleculaire labels die objecten markeren voor immuunaanval — terwijl zachte deeltjes minder van deze labels oppikten. Wanneer beide types aanwezig waren, kapten de stijve deeltjes de complementproteïnen weg, waardoor de zachte relatief ongetagd bleven. Deze combinatie van makkelijkere insluiting en zwaardere labeling trok stijve deeltjes naar immuuncellen en beschermde zachte deeltjes tegen clearance, waardoor ze langer in de circulatie bleven en de hersenen bereikten.
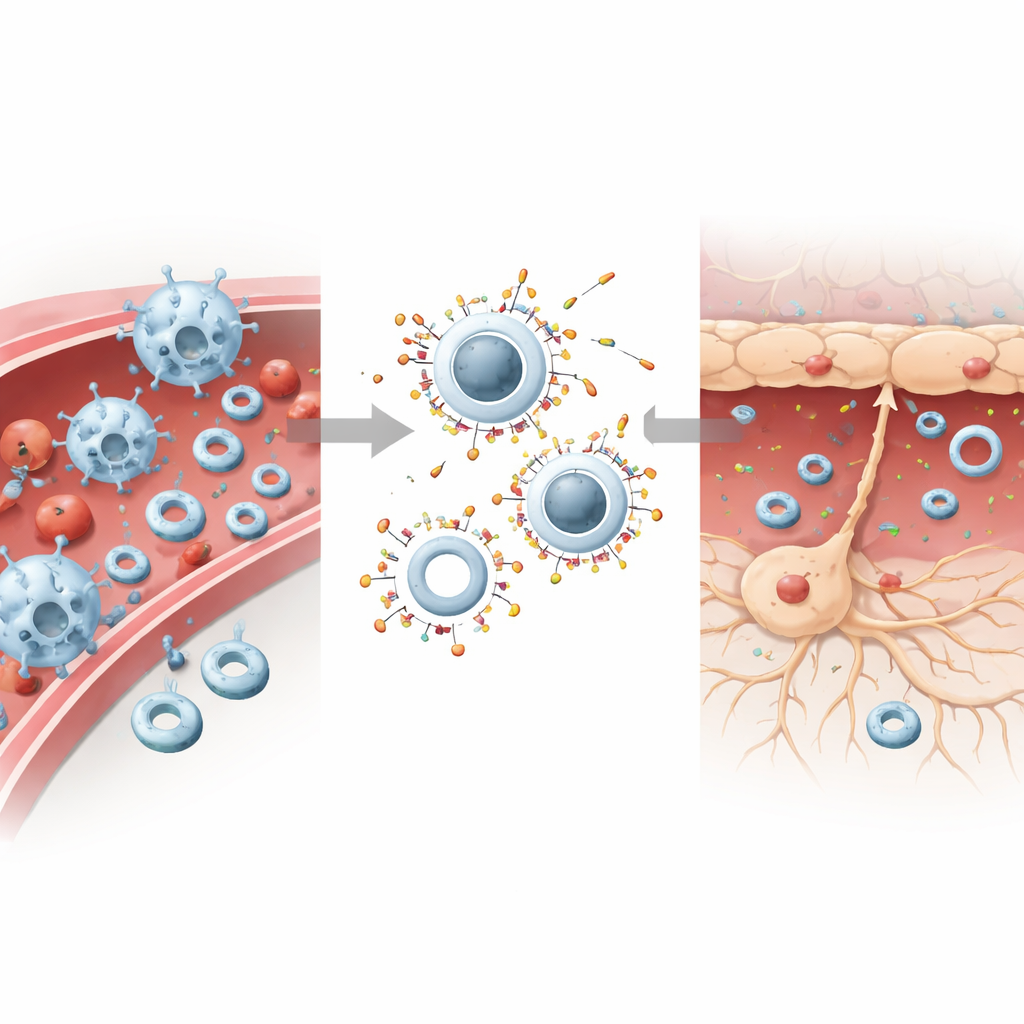
Taakverdeling: bloed kalmeren, hersenen genezen
Om dit gedrag therapeutisch te benutten, laadden de wetenschappers de stijve deeltjes met piceatannol, een middel dat signalen dempt die immuuncel‑hechting en invasie aansturen, en vulden de zachte deeltjes met DL-3-n-butylftalide, een neuroprotectieve verbinding die wordt gebruikt tegen oxidatieve stress en celdood. In muismodellen van beroerte stapelden de stijve, geneesmiddelgevulde deeltjes zich op in de lever en immuuncelrijke gebieden, verlaagden de niveaus van cruciale adhesiemoleculen en reduceerden scherp het aantal immuuncellen dat de beschadigde hersenen binnendrong. De zachte, geneesmiddelgevulde deeltjes, nu minder vatbaar voor opname door immuuncellen, passeerden de beschadigde bloed-hersenbarrière efficiënter en gaven hun lading vrij aan gestreste neuronen, wat de overleving van cellen verbeterde en lokale ontsteking verminderde.
Van muizen naar een nieuw soort precisiegeneeskunde
Bij tests over 28 dagen in muizen met ernstige beroerte verminderde deze combinatie van dubbele stijfheid de hersenzwelling en de infarctgrootte sterk, behield de integriteit van de bloed-hersenbarrière en verlaagde markers van ontsteking en celdood. Het meest opvallend was dat de overleving toenam van ongeveer één op negen muizen naar bijna acht op negen, en het neurologische herstel veel beter was dan bij enige behandeling met één type deeltje of met vrij geneesmiddel. Voor niet‑specialisten is de kernboodschap dat het afstemmen van draagstoffen op het juiste lichaamscompartiment door hun zachtheid of stijfheid te tunen een tweezijdige aanpak kan orkestreren: één in het bloed om schadelijke immuunoverreactie te stoppen, en één in de hersenen om herstel te bevorderen. Dit ‘mechanisch geleide’ afleveringsconcept zou zich kunnen uitstrekken voorbij beroerte naar andere ziekten waarin het immuunsysteem en de hersenen — of andere organen — verstrengeld zijn in een schadelijke dialoog.
Bronvermelding: Liu, H., Zheng, J., Li, Y. et al. Dual-stiffness nanoparticles for compartment-specific drug delivery in stroke. Nat Commun 17, 3837 (2026). https://doi.org/10.1038/s41467-026-70340-3
Trefwoorden: ischemische beroerte, nanodeeltjes, medicijnafgifte, neuroinflammatie, precisiemedicine