Clear Sky Science · sv
Trifluoperazin orsakar mastcellsapoptos genom en sekretorisk granulmedierad väg
Att omvandla ett läkemedel för mental hälsa till en allergikämpe
Personer med allergier, astma eller vissa inflammatoriska sjukdomar plågas ofta av en enda typ av immuncell: mastcellen. Denna studie undersöker en oväntad idé—att återanvända ett gammalt antipsykotiskt läkemedel, trifluoperazin, för att selektivt avlägsna skadliga mastceller samtidigt som de flesta andra celler sparas. Genom att klarlägga exakt hur detta läkemedel får mastceller att självförstöras öppnar arbetet en potentiellt ny väg för behandling av allergiska och mastcellsdrivna tillstånd.
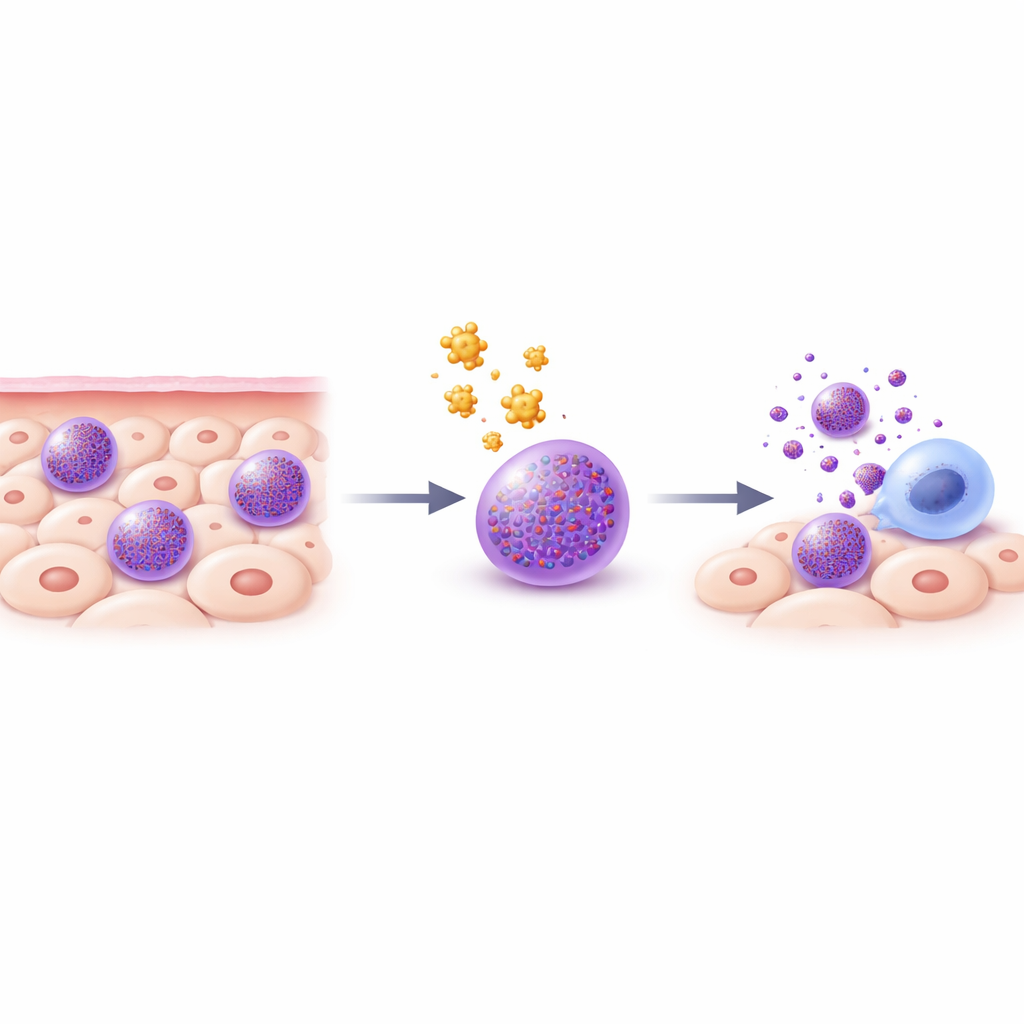
Den ställa besvärliga immuncellen
Mastceller är immunsensorer som finns i vävnader som hud, lungor och tarm. De är fyllda med små sura lagringsblåsor kallade granula, som innehåller potenta substanser såsom histamin, enzymer och inflammatoriska molekyler. När mastceller aktiveras—till exempel vid en allergisk reaktion—tömmer de snabbt dessa granula och utlöser svullnad, klåda och andra symtom. Befintliga behandlingar, som antihistaminer eller mastcellsstabiliserande läkemedel, blockerar bara en del av de många kemikalier mastceller kan frisätta. Eftersom sjukdom ofta beror på kombinerad verkan av flera mastcellsmediatorer övervägde författarna en djärvare strategi: att selektivt utlösa kontrollerad celldöd i mastcellerna själva.
En oväntad kandidat från psykiatrin
Teamet fokuserade på »lysosomotropa« läkemedel—små, svagt basiska molekyler som ansamlas i sura kompartment såsom lysosomer och mastcellsgranula. Vid tillräckligt höga nivåer kan dessa läkemedel försvaga granulamembran och få dem att läcka, vilket ibland leder till celldöd. Trifluoperazin, som länge använts för behandling av schizofreni och ångest, tillhör en läkemedelsfamilj som redan är känd för att ackumuleras i sådana sura kompartment. Forskarna testade trifluoperazin på en rad mus- och människoceller, inklusive glatta muskelceller i luftvägarna, fibroblaster, epitelceller, neutrofiler, eosinofiler och flera mastcellspopulationer. De fann att kliniskt relevanta doser var påfallande toxiska för mastceller, men lämnade de flesta andra celltyper stort sett opåverkade; endast eosinofiler, en annan granulrik immuncellstyp, visade viss känslighet vid högre doser.

Hur läkemedlet utlöser självförstörelse
För att förstå vad som händer inne i mastceller exponerade för trifluoperazin följde forskarna förändringar i granula och cellhälsa över tid. Strax efter behandling visade många mastceller klassiska kännetecken för apoptos, en prydlig, icke-inflammatorisk form av programmerad celldöd: de band Annexin V, visade DNA-fragmentering, krympte i storlek och utvecklade membranblåsor samtidigt som deras yttre membran förblev intakt. Mätningar med pH-känsliga färgämnen avslöjade att trifluoperazin gjorde granula mindre sura och samtidigt gjorde den omgivande cellvätskan surare—bevis på att protoner och annat innehåll läckte ut ur granula. Ett nyckelenzym i mastceller, tryptas, som normalt är inneslutet i granula, detekterades i cellens cytosol strax efter läkemedelsexponering, vilket bekräftade att granulamembranen blivit permeabla.
Granula i centrum för händelserna
Mikroskopi gav en visuell inblick i denna process. I elektronmikroskop visade obehandlade mastceller täta, välstrukturerade granula. Efter behandling med trifluoperazin svällde dessa granula, förlorade mycket av sitt inre innehåll och visade ibland synliga brott i sina membran, förenligt med läckage in i cellen. När forskarna blockerade den protonpumpande V‑ATPase, som normalt håller granula sura, kunde trifluoperazin inte längre effektivt avsura granula, flytta tryptas till cytosolen, fragmentera DNA eller döda mastcellerna. Detta starka skydd visade att granulasyra är avgörande för läkemedlets destruktiva effekt. Överraskande nog spelade enzymer kallade kaspaser—centrala bödlar i många former av apoptos—endast en mindre roll här. Istället påverkade andra proteaser, särskilt en undergrupp av serinproteaser, om cellerna dog på ett ordnat apoptotiskt sätt eller på ett mer skadligt nekrosliknande vis.
Vad detta kan innebära för framtida behandlingar
Sammanfattningsvis visar studien att trifluoperazin selektivt kan döda mastceller genom att destabilisera deras sura granula, vilket får deras egna toxiska innehåll att läcka ut och driva en i stor utsträckning kaspasoberoende, apoptosliknande död. Eftersom mastceller är nyckelaktörer i många allergiska och inflammatoriska sjukdomar, och eftersom trifluoperazin redan är ett godkänt läkemedel, pekar denna granulamedierade väg mot en lovande strategi för att återanvända eller förfina sådana föreningar för klinisk användning. I princip kan noggrant riktad dosering minska antalet mastceller i drabbade vävnader—såsom luftvägarna vid astma eller vid näspolyper—utan att i hög grad skada intilliggande celler, vilket erbjuder en ny strategi för att dämpa mastcellsdrivna sjukdomar.
Citering: Vraila, M., Hu Frisk, J.M., Mayavannan, A. et al. Trifluoperazine causes mast cell apoptosis through a secretory granule-mediated pathway. Cell Death Discov. 12, 185 (2026). https://doi.org/10.1038/s41420-026-03122-x
Nyckelord: mastceller, trifluoperazin, allergibehandling, granulmedierad apoptos, lysosomotrofa läkemedel