Clear Sky Science · he
טריפלואופרזין גורם לאפופטוזה של תאי פיטום דרך מסלול מתווך על ידי גרנולות מופרשות
להפוך תרופת בריאות נפש למלחמה באלרגיה
אנשים עם אלרגיות, אסתמה או מחלות דלקתיות מסוימות סובלים לעתים קרובות בגלל סוג אחד של תא חיסון: תא הפיטום. המחקר הזה בוחן רעיון בלתי צפוי — השמת תרופה אנטי־פסיכוטית ישנה, טריפלואופרזין, לשימוש מחדש כדי להסיר בצורה סלקטיבית תאי פיטום מזיקים תוך שמירה על רוב התאים האחרים. על ידי חשיפת המנגנון המדויק שבו התרופה גורמת לתאי הפיטום להשמיד את עצמם, העבודה פותחת מסלול פוטנציאלי חדש לטיפול במצבי אלרגיה ומחלות מונעות על ידי תאי פיטום.
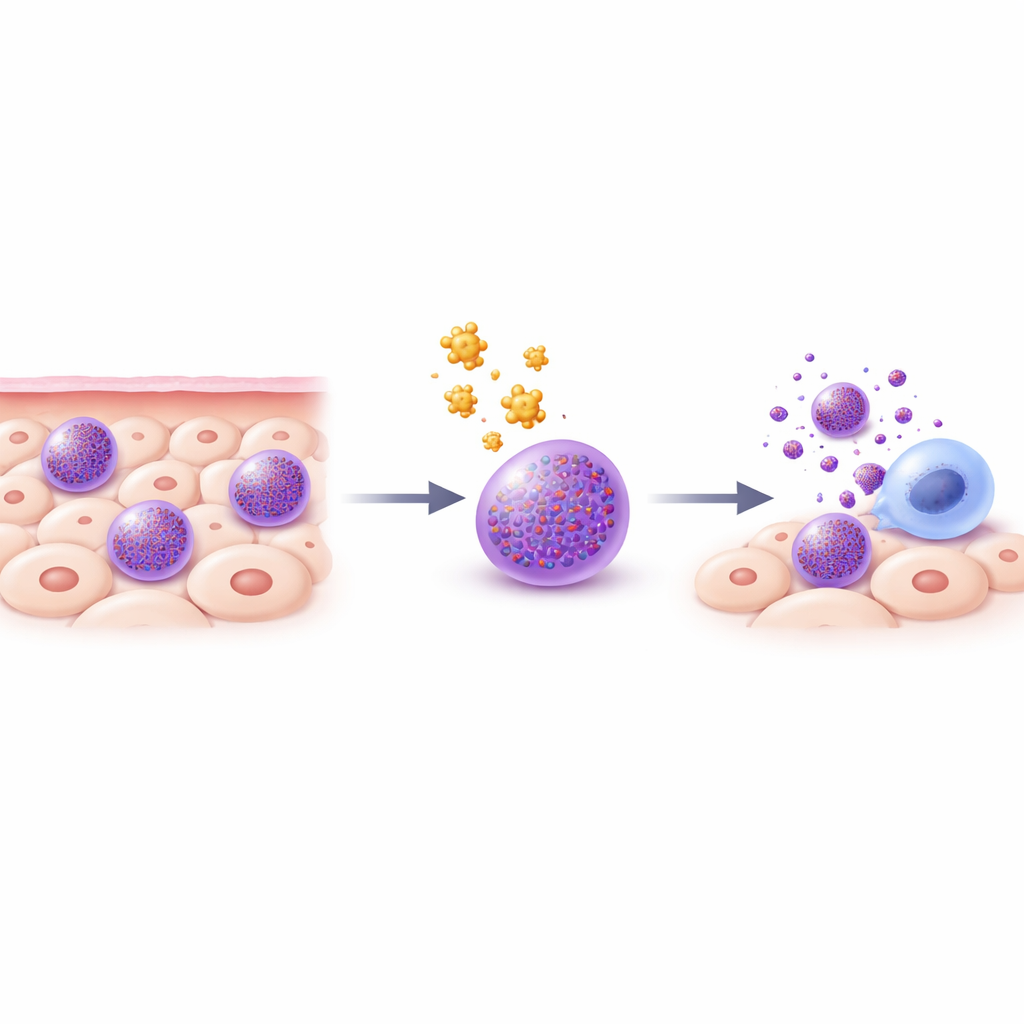
תא החיסון שגורם לבעיות
תאי הפיטום הם סנטינלים חיסוניים היושבים ברקמות כמו העור, הריאות והמעי. הם מלאים בשקיות אחסון חומציות זעירות שנקראות גרנולות, ובהן חומרים עוצמתיים כגון היסטמין, אנזימים ומולקולות דלקתיות. כאשר תאי הפיטום מופעלים — לדוגמה במהלך תגובה אלרגית — הם מרוקנים במהירות את הגרנולות, מה שגורם לנפיחות, גירוד ותסמינים אחרים. טיפולים קיימים, כמו אנטיהיסטמינים או תרופות המייצבות תאי פיטום, חוסמים רק חלק מהחומרים הרבים שתאי הפיטום יכולים לשחרר. מאחר שמחלה נובעת לעתים משילוב הפעולה של מספר מתווכים של תאי הפיטום, החוקרים שקלו אסטרטגיה נועזת יותר: לגרום באופן סלקטיבי למוות מתוכנן מבוקר בתאי הפיטום עצמם.
מועמד מפתיע מתחום הפסיכיאטריה
הקבוצה התמקדה ב«תרופות ליזוסומוטרופיות» — מולקולות קטנות, בסיסיות בחולשה, שנוטות להצטבר בתאים בת compartments חומציים כגון ליזוזומים וגרנולות של תאי פיטום. בריכוזים גבוהים דיים, תרופות אלה יכולות להחליש את ממברנות הגרנולות ולגרום לדליפה, שלעיתים מובילה למוות תאי. טריפלואופרזין, ששימש זמן רב לטיפול בסכיזופרניה ובחרדות, שייך למשפחה של תרופות שכבר ידועות כי מצטברות באותם compartments חומציים. החוקרים בדקו את הטריפלואופרזין על מגוון תאים של עכבר ובני אדם, כולל תאי שריר חלק של דרכי הנשימה, פיברובלסטים, תאים אפיתליאליים, נויטרופילים, אאוזינופילים וכמה אוכלוסיות של תאי פיטום. הם מצאו שמינונים קליניים היו רעילים באופן בולט לתאי פיטום, אך השאירו את רוב סוגי התאים האחרים כמעט ללא פגע; רק אאוזינופילים, תא חיסון עשיר בגרנולות אחר, הראו רגישות מסוימת במינונים גבוהים יותר.

כיצד התרופה מעוררת השמדה עצמית
כדי להבין מה קורה בתוך תאי הפיטום החשופים לטריפלואופרזין, המדענים עקבו אחר שינויים בגרנולות ובמצב התא לאורך זמן. זמן קצר אחרי הטיפול, רבים מתאי הפיטום הציגו סימנים קלאסיים של אפופטוזה, צורת מוות תאי מתוכננת נקייה ולא דלקתית: קישור ל־Annexin V, שבירת DNA, הצטמצמות בגודל ופיתוח בליטות ממברנלית בעוד שהממברנה החיצונית נשמרת שלמה. מדידות בעזרת צבעים רגישי pH הראו שטריפלואופרזין הפך את הגרנולות לפחות חומציות ובאותו זמן החמיץ את הנוזל התוך־תא חיובי החומציות — ראיה שחלבונים אחרים ופרוטונים דולפים מהגרנולות. אנזים מרכזי של תאי הפיטום, טריפטאז, שנעול בדרך כלל בתוך הגרנולות, זוהה בנוזל התוך־תאי זמן קצר לאחר החשיפה לתרופה, ואשרר שממברנות הגרנולות הפכו לפרמיאביליות.
גרנולות במרכז הפעולה
מיקרוסקופיה סיפקה חלון חזותי לתהליך זה. תחת מיקרוסקופ אלקטרוני, תאי פיטום שלא טופלו הציגו גרנולות צפופות ומסודרות היטב. לאחר טיפול בטריפלואופרזין, גרנולות אלה התנפחו, איבדו חלק גדול מהחומר הפנימי ולעתים הציגו קרעים נראים בממברנותיהן, תואם לדליפה לתוך התא. כאשר החוקרים חסמו את משאבת החומציות V‑ATPase, שאחראית לשימור החומציות בגרנולות, הטריפלואופרזין כבר לא יכול היה להפחית ביעילות את חומציות הגרנולות, להעביר את הטריפטאז לציטוזול, לשבור DNA או להרוג את תאי הפיטום. ההגנה החזקה הזו הראתה שחומציות הגרנולות חיונית להשפעה ההרסנית של התרופה. באופן מפתיע, אנזימים הקרויים קספאזות — מבצעים מרכזיים בצורות רבות של אפופטוזה — שיחקו כאן רק תפקיד משני. במקום זאת, פרוטאזות אחרות, ובמיוחד תת‑קבוצה של פרוטאזות serine, נראו כמחוללות השפעה על כך שהתאים ימותו באופן אפופטוטי מסודר או בדרך יותר מזיקה הדומה לנקרוזה.
מה זה עשוי להצביע לגבי טיפולים עתידיים
בסך הכל, הממצאים מראים שטריפלואופרזין יכול להרוג תאי פיטום בצורה סלקטיבית על ידי יצירת חוסר יציבות בגרנולות החומציות שלהם, מה שגורם לתכולה הרעילה להיחשף ולהוביל למוות דמוי‑אפופטוזה ברובו שאינו תלוי מאוד בקספרות. מאחר שתאי הפיטום הם גורם מרכזי בהרבה מחלות אלרגיות ודלקתיות, ומאחר שטריפלואופרזין כבר מאושר כתרופה, המסלול המתווך על ידי הגרנולות מציע נתיב מבטיח להטמעת שימוש מחדש או לשכלול תרכובות כאלה לשימוש קליני. בעקרון, מתן מדוד וממוקד יכול להפחית את מספר תאי הפיטום ברקמות מושפעות — כמו דרכי הנשימה באסתמה או פוליפים באף — מבלי לפגוע באופן נרחב בתאים מסביב, וכך להציע אסטרטגיה חדשה להגביל מחלות מונעות־פיטום.
ציטוט: Vraila, M., Hu Frisk, J.M., Mayavannan, A. et al. Trifluoperazine causes mast cell apoptosis through a secretory granule-mediated pathway. Cell Death Discov. 12, 185 (2026). https://doi.org/10.1038/s41420-026-03122-x
מילות מפתח: תאי פיטום, טריפלואופרזין, טיפול באלרגיה, אפופטוזה מתווכת־גרנולות, תרופות ליזוסומוטרופיות