Clear Sky Science · nl
Trifluoperazine veroorzaakt apoptose van mestcellen via een secretorisch granula-gemedieerde route
Een psychofarmacon omvormen tot allergiebestrijder
Mensen met allergieën, astma of bepaalde ontstekingsziekten hebben vaak last van één type immuuncel: de mestcel. Deze studie verkent een onverwacht idee: een oud antipsychoticum, trifluoperazine, herbestemmen om schadelijke mestcellen selectief te verwijderen terwijl de meeste andere cellen gespaard blijven. Door precies te ontrafelen hoe dit middel mestcellen zelfdestructie laat ondergaan, opent het werk een mogelijke nieuwe weg voor de behandeling van allergische en mestcel‑gedreven aandoeningen.
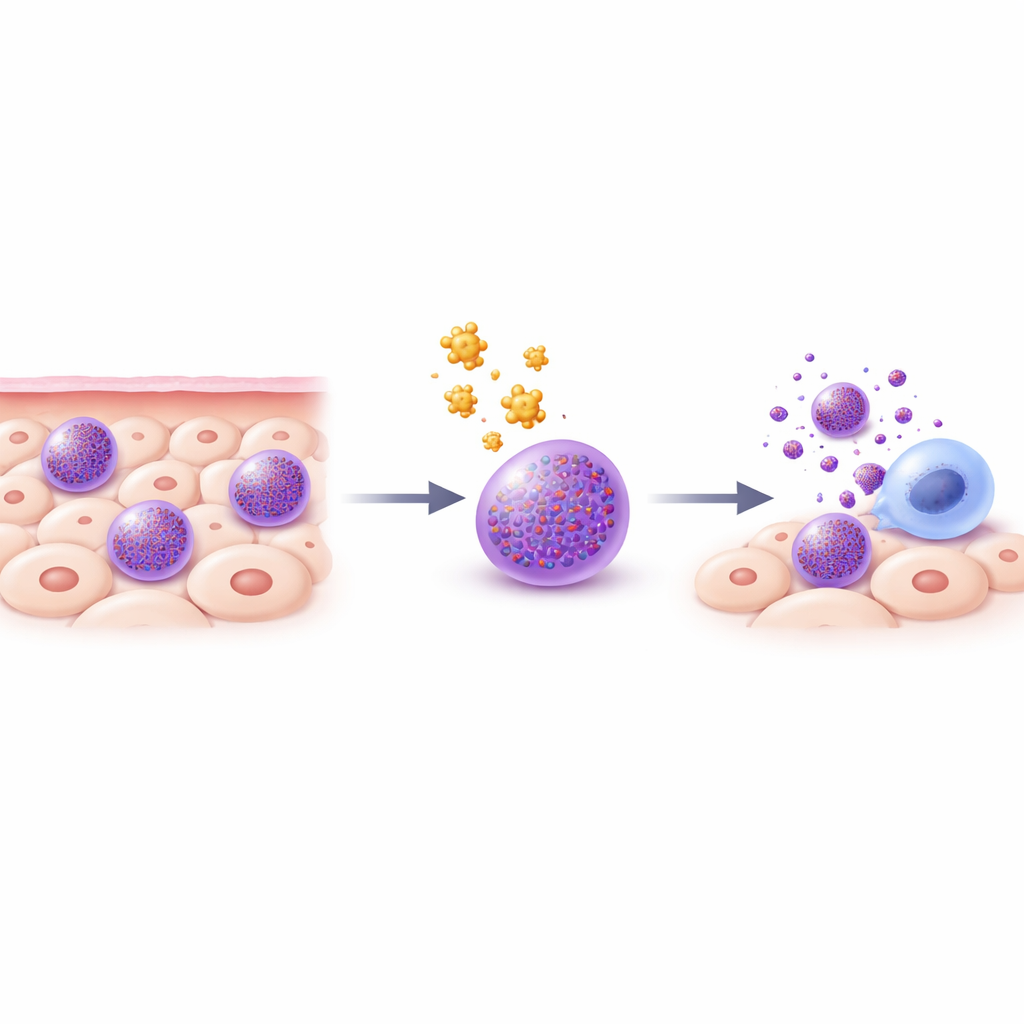
De probleem veroorzakende immuuncel
Mestcellen zijn immuunwachters die in weefsels zoals de huid, longen en darmen zitten. Ze zitten vol met kleine zure opslagblaasjes, granula genoemd, die krachtige stoffen bevatten zoals histamine, enzymen en ontstekingsmoleculen. Wanneer mestcellen geactiveerd worden—bijvoorbeeld tijdens een allergische reactie—ledigen ze snel deze granula, wat zwelling, jeuk en andere symptomen veroorzaakt. Bestaande behandelingen, zoals antihistaminica of mestcel‑stabilisatoren, blokkeren slechts een deel van de vele chemicaliën die mestcellen kunnen vrijgeven. Omdat ziekte vaak het gevolg is van de gecombineerde werking van meerdere mestcelmediatoren, overwegen de auteurs een gedurfder strategie: gecontroleerde celdood in de mestcellen zelf opwekken.
Een verrassende kandidaat uit de psychiatrie
Het team richtte zich op “lysosomotrope” geneesmiddelen—kleine, zwak basische moleculen die zich ophopen in zure compartimenten zoals lysosomen en mestcelgranula. Bij voldoende hoge concentraties kunnen deze middelen de granula‑membranen verzwakken en lekkage veroorzaken, wat soms leidt tot celdood. Trifluoperazine, dat lange tijd gebruikt wordt voor de behandeling van schizofrenie en angst, behoort tot een geneesmiddelengroep die bekendstaat om zich in zulke zure compartimenten op te hopen. De onderzoekers testten trifluoperazine op verschillende muis‑ en menselijke cellen, waaronder luchtwegspierspieren, fibroblasten, epitheelcellen, neutrofielen, eosinofielen en meerdere mestcelpopulaties. Ze vonden dat klinisch relevante doses opvallend toxisch waren voor mestcellen, maar de meeste andere celtypen grotendeels ongemoeid lieten; alleen eosinofielen, een ander granula‑rijk immuunceltype, toonden bij hogere doses enige gevoeligheid.

Hoe het middel zelfvernietiging veroorzaakt
Om te begrijpen wat er binnenin mestcellen gebeurt na blootstelling aan trifluoperazine, volgden de wetenschappers veranderingen in granula en celgezondheid in de tijd. Kort na behandeling vertoonden veel mestcellen klassieke kenmerken van apoptose, een nette, niet‑ontstekingsbevorderende vorm van geprogrammeerde celdood: ze binden Annexine V, vertonen DNA‑fragmentatie, krimpen in omvang en ontwikkelen membraanblaasjes terwijl de buitenste membraan intact blijft. Metingen met pH‑gevoelige kleurstoffen toonden aan dat trifluoperazine de granula minder zuur maakte en tegelijkertijd het omringende celvocht zuurder maakte—bewijs dat protonen en andere inhoudsstoffen uit de granula lekten. Een belangrijk mestcelenzym, tryptase, dat normaal in de granula opgesloten zit, werd kort na blootstelling aan het middel in het cytosol gedetecteerd, wat bevestigt dat granula‑membranen permeabel waren geworden.
Granula in het hart van de werking
Microscopie bood een visueel venster op dit proces. Onder de elektronenmicroscoop toonden onbehandelde mestcellen dichte, goed gestructureerde granula. Na behandeling met trifluoperazine zwollen deze granula op, verloren veel van hun binnenmateriaal en vertoonden soms zichtbare scheuren in hun membranen, wat consistent is met lekkage in de cel. Wanneer de onderzoekers de zuurpomp V‑ATPase blokkeerden, die normaal granula zuur houdt, kon trifluoperazine de granula niet meer efficiënt deacidifiëren, tryptase naar het cytosol verplaatsen, DNA fragmenteren of de mestcellen doden. Deze sterke bescherming toont aan dat de zuurheid van granula cruciaal is voor het destructieve effect van het middel. Verrassend genoeg speelden enzymen die caspases heten—centrale uitvoerders in veel vormen van apoptose—hier slechts een kleine rol. In plaats daarvan leken andere proteasen, met name een subset van serineproteasen, te bepalen of de cellen op een ordelijke apoptotische manier stierven of op een meer schadelijke, necrose‑achtige wijze.
Wat dit kan betekenen voor toekomstige behandelingen
Al met al laat de studie zien dat trifluoperazine mestcellen selectief kan doden door hun zure granula te destabiliseren, waardoor hun eigen toxische inhoud lekt en een grotendeels caspase‑onafhankelijke, apoptose‑achtige dood in gang zet. Omdat mestcellen belangrijke boosdoeners zijn bij veel allergische en ontstekingsziekten, en trifluoperazine al een goedgekeurd geneesmiddel is, suggereert deze granula‑gemedieerde route een veelbelovende mogelijkheid om zulke verbindingen voor klinisch gebruik te herbestemmen of te verfijnen. In principe kan een zorgvuldig gerichte dosering het aantal mestcellen in aangedane weefsels—zoals de luchtwegen bij astma of neuspoliepen—verminderen zonder omliggende cellen veel te schaden, wat een nieuwe strategie biedt om mestcel‑gedreven ziekte af te zwakken.
Bronvermelding: Vraila, M., Hu Frisk, J.M., Mayavannan, A. et al. Trifluoperazine causes mast cell apoptosis through a secretory granule-mediated pathway. Cell Death Discov. 12, 185 (2026). https://doi.org/10.1038/s41420-026-03122-x
Trefwoorden: mestcellen, trifluoperazine, allergiebehandeling, granula-gemedieerde apoptose, lysosomotrope geneesmiddelen