Clear Sky Science · ja
トリフルオペラジンは分泌顆粒依存経路を介して肥満細胞のアポトーシスを引き起こす
精神科薬をアレルギー治療薬に転用する試み
アレルギー、喘息、ある種の炎症性疾患の患者は、しばしば単一の免疫細胞、肥満細胞の作用によって症状を招かれます。本研究は予想外の発想を探ります――古くからある抗精神病薬トリフルオペラジンを再利用し、有害な肥満細胞のみを選択的に除去して他の多くの細胞を保護するというものです。この薬が肥満細胞の自己破壊をどのように引き起こすかを詳述することで、アレルギーや肥満細胞駆動性疾患の新たな治療経路を開く可能性が示されます。
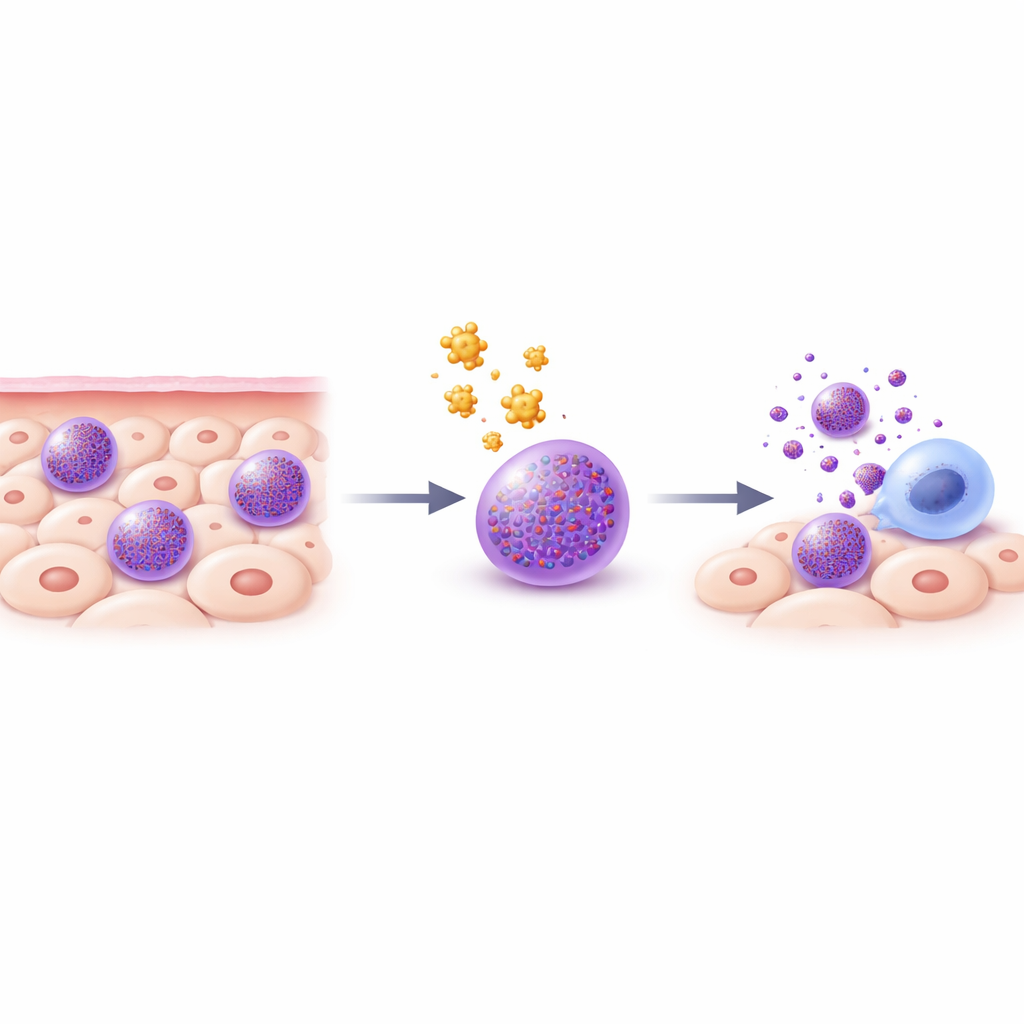
厄介な免疫細胞
肥満細胞は皮膚、肺、腸などの組織に存在する免疫の見張り役です。これらの細胞は顆粒と呼ばれる小さな酸性の貯蔵袋を多数含み、ヒスタミンや酵素、炎症性分子など強力な物質を蓄えています。アレルギー反応のように肥満細胞が活性化されると、これらの顆粒が急速に放出され、腫れ、かゆみなどの症状を引き起こします。抗ヒスタミンや肥満細胞安定化薬のような既存治療は、肥満細胞が放出する多数の化学物質のごく一部しか遮断できません。疾患はしばしば複数の肥満細胞メディエーターの結合作用から生じるため、著者らはより大胆な戦略、すなわち肥満細胞自身に制御された細胞死を選択的に誘導することを検討しました。
精神医学からの意外な候補
研究チームは「リソソモトロピック」薬剤に注目しました。これはリソソームや肥満細胞顆粒のような酸性コンパートメントに蓄積する小さく弱塩基性の分子群です。高濃度では、これらの薬剤は顆粒膜を弱めリークを引き起こし、場合によっては細胞死に至らせることがあります。統合失調症や不安障害の治療に長く用いられてきたトリフルオペラジンは、こうした酸性コンパートメントに蓄積することが既知の薬剤群に属します。研究者らは気道平滑筋細胞、線維芽細胞、上皮細胞、好中球、好酸球、そして複数の肥満細胞集団を含むマウスおよびヒトの細胞群にトリフルオペラジンを投与して試験しました。その結果、臨床的に関連する濃度で肥満細胞に対して著しい毒性を示した一方で、ほとんどの他の細胞種にはほぼ影響が見られませんでした。例外として、別の顆粒豊富な免疫細胞である好酸球は、より高濃度で感受性を示しました。

薬が自己破壊を誘導する仕組み
トリフルオペラジンに暴露された肥満細胞内で何が起きるかを理解するため、科学者らは時間経過に伴う顆粒と細胞の変化を追跡しました。処理後まもなく、多くの肥満細胞はアポトーシスの古典的な特徴を示しました。アネキシンV結合、DNA断片化、細胞の縮小、膜ブレブの形成が観察されつつ外膜は保たれており、これは非炎症性で整然としたプログラム細胞死を示します。pH感受性蛍光色素による計測は、トリフルオペラジンが顆粒内を脱酸性化すると同時に細胞質側の液相を酸性化していることを示し、プロトンや顆粒内容物が漏出していることを示す証拠となりました。本来顆粒内に封じ込められている主要な肥満細胞酵素であるトリプターゼが、薬剤暴露後まもなく細胞質液内で検出されたことは、顆粒膜が透過性を獲得したことを裏付けます。
中心にあるのは顆粒の変化
顕微鏡観察はこの過程を視覚的に示しました。電子顕微鏡下で未処理の肥満細胞は濃密で構造の整った顆粒を示しましたが、トリフルオペラジン処理後には顆粒が膨張し内部物質を失い、時に膜の断裂が見られるなど細胞内への漏出と一致する変化が観察されました。顆粒を酸性に保つV‑ATPaseを阻害すると、トリフルオペラジンは顆粒を効率的に脱酸性化できず、トリプターゼを細胞質へ移動させることも、DNAを断片化することも、肥満細胞を死に至らしめることもできなくなりました。この強い保護効果は、顆粒の酸性化が薬剤の破壊的作用にとって重要であることを示しています。驚くべきことに、多くのアポトーシスで中心的役割を果たすカスパーゼはここでは小さな寄与しか示しませんでした。代わりに、特に一部のセリンプロテアーゼなど他のプロテアーゼ群が、細胞が秩序だったアポトーシス様死を迎えるか、より損傷的な壊死様の経路をとるかに影響を与えているようでした。
将来の治療にとっての意義
総じて、本研究はトリフルオペラジンが肥満細胞の酸性顆粒を不安定化させ、自らの有毒な内容物を漏出させることで、主にカスパーゼ非依存のアポトーシス様死を誘導し肥満細胞を選択的に死滅させることを明らかにしました。肥満細胞は多くのアレルギー性および炎症性疾患の主要な加害因子であり、トリフルオペラジンはすでに承認薬であることから、この顆粒依存経路はこうした化合物を臨床利用に転用・改良する有望な手がかりを示唆します。原理的には、慎重に標的化された用量設定により、喘息の気道や鼻ポリープなど影響を受けた組織の肥満細胞数を減らしつつ、周囲の細胞に広く有害な影響を及ぼさないことで、肥満細胞駆動性疾患の活動を抑える新たな戦略となり得ます。
引用: Vraila, M., Hu Frisk, J.M., Mayavannan, A. et al. Trifluoperazine causes mast cell apoptosis through a secretory granule-mediated pathway. Cell Death Discov. 12, 185 (2026). https://doi.org/10.1038/s41420-026-03122-x
キーワード: 肥満細胞, トリフルオペラジン, アレルギー治療, 顆粒依存性アポトーシス, リソソモトロピック薬