Clear Sky Science · fr
La trifluopérazine induit l’apoptose des mastocytes via une voie médiée par les granules sécrétoires
Transformer un médicament de santé mentale en arme contre les allergies
Les personnes souffrant d’allergies, d’asthme ou de certaines maladies inflammatoires pâtissent souvent à cause d’un seul type de cellule immunitaire : le mastocyte. Cette étude examine une idée inattendue — recycler un ancien antipsychotique, la trifluopérazine, pour éliminer sélectivement les mastocytes nocifs tout en épargnant la plupart des autres cellules. En révélant précisément comment ce médicament provoque l’autodestruction des mastocytes, le travail ouvre une voie potentielle pour traiter les affections allergiques et celles induites par les mastocytes.
La cellule immunitaire à l’origine des ennuis
Les mastocytes sont des sentinelles immunitaires présentes dans les tissus comme la peau, les poumons et l’intestin. Ils sont remplis de petits sacs de stockage acides appelés granules, qui contiennent des substances puissantes telles que l’histamine, des enzymes et des molécules inflammatoires. Lorsque les mastocytes sont activés — par exemple lors d’une réaction allergique — ils vident rapidement ces granules, déclenchant gonflement, démangeaisons et autres symptômes. Les traitements existants, comme les antihistaminiques ou les stabilisateurs de mastocytes, ne bloquent qu’une fraction des nombreux médiateurs que ces cellules peuvent libérer. Parce que la maladie résulte souvent de l’action combinée de plusieurs médiateurs des mastocytes, les auteurs ont envisagé une stratégie plus audacieuse : déclencher sélectivement la mort cellulaire programmée des mastocytes eux‑mêmes.
Un candidat surprenant venu de la psychiatrie
L’équipe s’est intéressée aux médicaments « lysosomotropes » — de petites molécules faiblement basiques qui s’accumulent dans des compartiments acides comme les lysosomes et les granules des mastocytes. À des concentrations suffisantes, ces médicaments peuvent affaiblir les membranes des granules et provoquer des fuites, conduisant parfois à la mort cellulaire. La trifluopérazine, utilisée depuis longtemps pour traiter la schizophrénie et l’anxiété, appartient à une famille de médicaments déjà connue pour s’accumuler dans ces compartiments acides. Les chercheurs ont testé la trifluopérazine sur une gamme de cellules de souris et humaines, y compris des cellules musculaires lisses des voies aériennes, des fibroblastes, des cellules épithéliales, des neutrophiles, des éosinophiles et plusieurs populations de mastocytes. Ils ont constaté que des doses cliniquement pertinentes étaient remarquablement toxiques pour les mastocytes, tout en épargnant la plupart des autres types cellulaires ; seuls les éosinophiles, un autre type de cellule immunitaire riche en granules, ont montré une certaine sensibilité à doses plus élevées.

Comment le médicament déclenche l’autodestruction
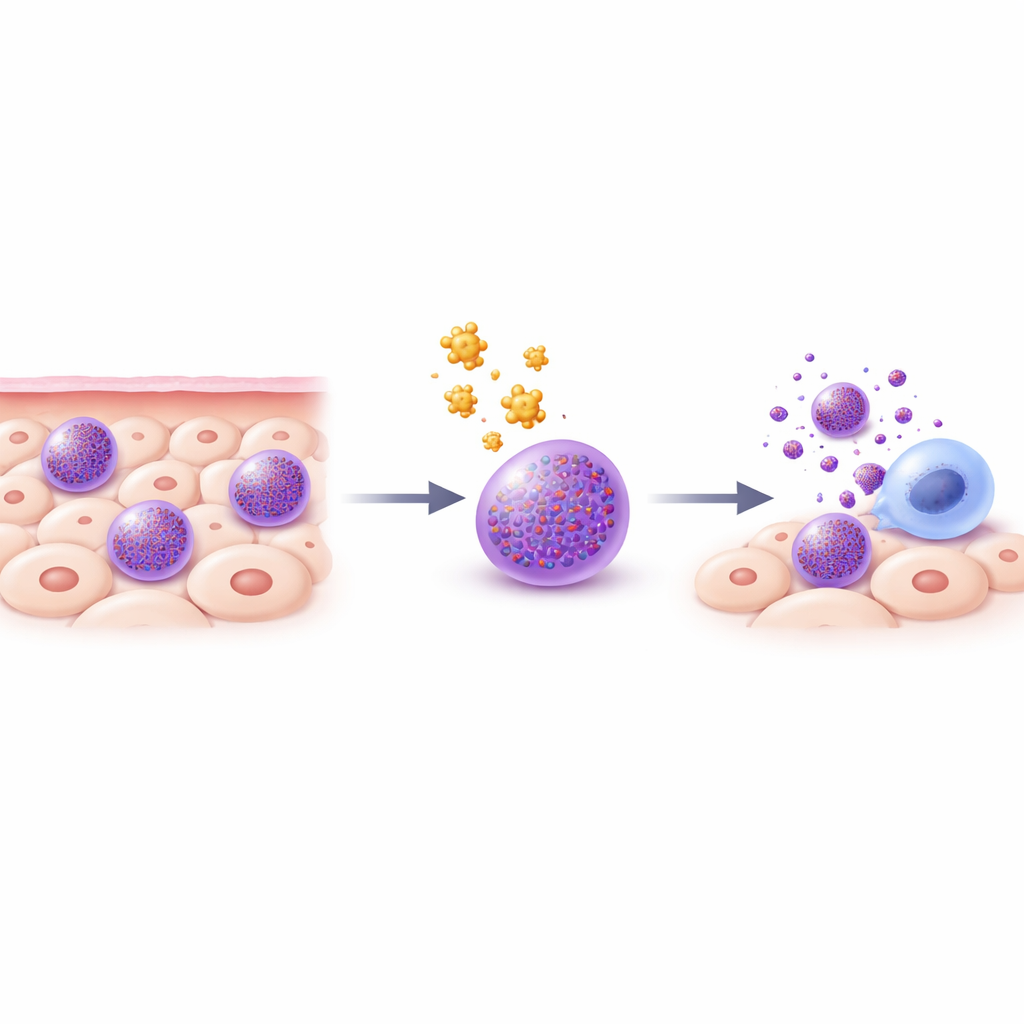
Pour comprendre ce qui se passe à l’intérieur des mastocytes exposés à la trifluopérazine, les scientifiques ont suivi l’évolution des granules et de l’état cellulaire au fil du temps. Peu après le traitement, de nombreux mastocytes présentaient les signes classiques de l’apoptose, une forme ordonnée et non inflammatoire de mort cellulaire programmée : fixation de l’Annexine V, fragmentation de l’ADN, réduction du volume cellulaire et apparition de boursouflures de membrane tout en conservant une membrane plasmique intacte. Des mesures avec des sondes sensibles au pH ont montré que la trifluopérazine rendait les granules moins acides et, simultanément, acidifiait davantage le fluide environnant de la cellule — preuve que des protons et d’autres contenus fuyaient hors des granules. Une enzyme clé des mastocytes, la tryptase, normalement enfermée dans les granules, a été détectée dans le fluide intracellulaire peu après l’exposition au médicament, confirmant que les membranes des granules étaient devenues perméables.
Les granules au cœur du mécanisme
La microscopie a offert une fenêtre visuelle sur ce processus. Au microscope électronique, les mastocytes non traités présentaient des granules denses et bien structurés. Après traitement par la trifluopérazine, ces granules gonflaient, perdaient une grande partie de leur contenu intérieur et montraient parfois des ruptures visibles de leurs membranes, compatibles avec des fuites dans la cellule. Lorsque les chercheurs ont bloqué la V‑ATPase, la pompe à protons qui maintient normalement l’acidité des granules, la trifluopérazine n’a plus pu déacidifier efficacement les granules, déplacer la tryptase dans le cytosol, fragmenter l’ADN ni tuer les mastocytes. Cette forte protection montrait que l’acidité des granules est cruciale pour l’effet destructeur du médicament. De manière surprenante, les caspases — exécuteurs centraux de nombreuses formes d’apoptose — jouaient ici un rôle mineur. À la place, d’autres protéases, en particulier un sous‑ensemble de protéases sérine, semblaient influencer si les cellules mouraient de façon ordonnée par apoptose ou de manière plus dommageable ressemblant à la nécrose.
Ce que cela pourrait signifier pour les traitements futurs
Dans l’ensemble, l’étude révèle que la trifluopérazine peut tuer sélectivement les mastocytes en déstabilisant leurs granules acides, provoquant la fuite de leur contenu toxique et entraînant une mort de type apoptotique largement indépendante des caspases. Parce que les mastocytes sont des acteurs clés de nombreuses maladies allergiques et inflammatoires, et parce que la trifluopérazine est déjà un médicament approuvé, cette voie médiée par les granules suggère une piste prometteuse pour réorienter ou affiner de tels composés en vue d’un usage clinique. En principe, un dosage ciblé avec précaution pourrait réduire le nombre de mastocytes dans les tissus affectés — comme les voies aériennes dans l’asthme ou les polypes nasaux — sans nuire largement aux cellules voisines, offrant une nouvelle stratégie pour atténuer les maladies induites par les mastocytes.
Citation: Vraila, M., Hu Frisk, J.M., Mayavannan, A. et al. Trifluoperazine causes mast cell apoptosis through a secretory granule-mediated pathway. Cell Death Discov. 12, 185 (2026). https://doi.org/10.1038/s41420-026-03122-x
Mots-clés: mastocytes, trifluopérazine, thérapie des allergies, apoptose médiée par les granules, médicaments lysosomotropes