Clear Sky Science · de
Trifluoperazin verursacht Mastzell-Apoptose durch einen von sekretorischen Granula vermittelten Weg
Ein Psychopharmakon als Angriffspunkt gegen Allergien
Menschen mit Allergien, Asthma oder bestimmten entzündlichen Erkrankungen leiden oft wegen einer einzigen Art von Immunzellen: den Mastzellen. Diese Studie untersucht eine unerwartete Idee — die Umwidmung eines alten Antipsychotikums, Trifluoperazin, um schädliche Mastzellen selektiv zu entfernen und dabei die meisten anderen Zellen zu verschonen. Indem sie genau aufdecken, wie dieses Medikament Mastzellen zur Selbstzerstörung bringt, öffnet die Arbeit einen potenziellen neuen Weg zur Behandlung allergischer und mastzellgetriebener Erkrankungen.
Die problematische Immunzelle
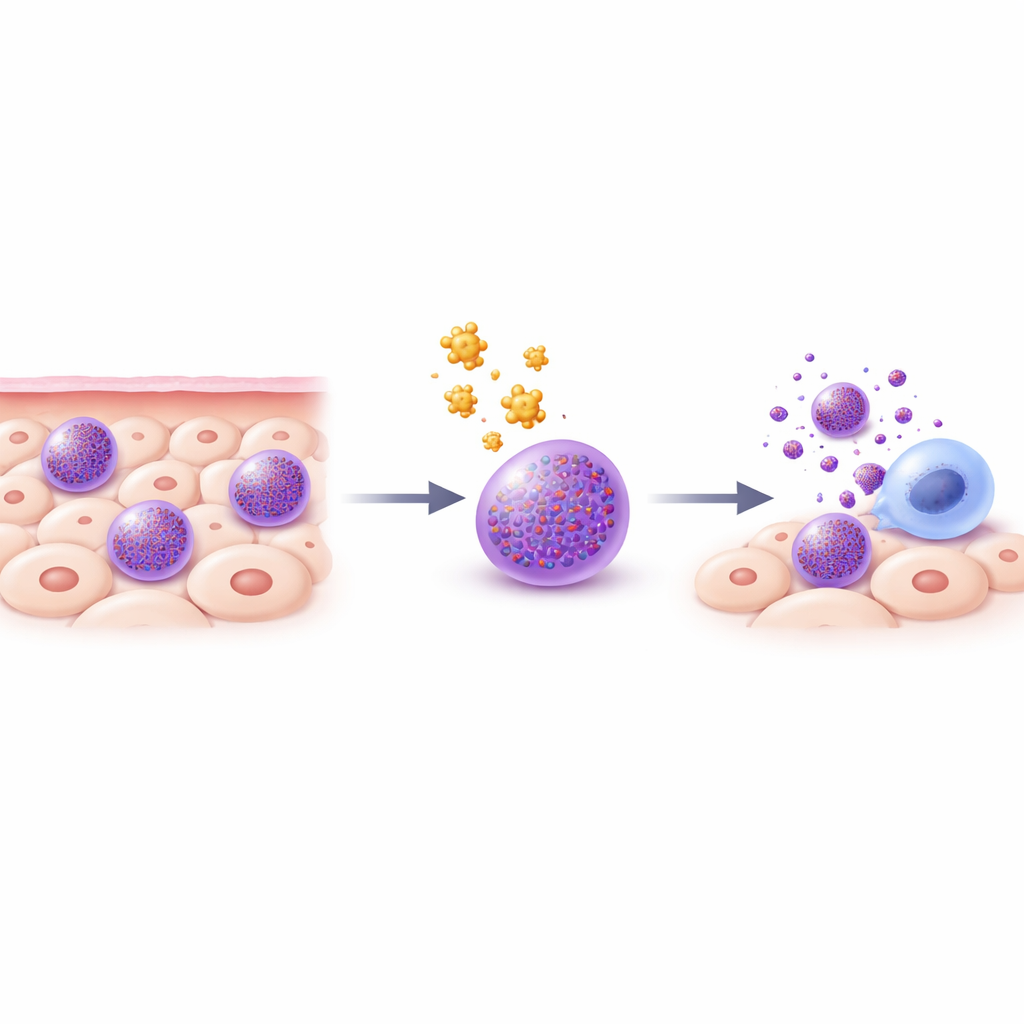
Mastzellen sind Immunwächter, die in Geweben wie Haut, Lunge und Darm sitzen. Sie sind vollgepackt mit winzigen, sauren Speichersäckchen, den Granula, die potente Substanzen wie Histamin, Enzyme und entzündungsfördernde Moleküle enthalten. Wenn Mastzellen aktiviert werden — zum Beispiel bei einer allergischen Reaktion — entleeren sie diese Granula schnell, was Schwellung, Juckreiz und andere Symptome auslöst. Bestehende Behandlungen, wie Antihistaminika oder Mastzell-stabilisierende Medikamente, blockieren nur einen Teil der zahlreichen Chemikalien, die Mastzellen freisetzen können. Da Krankheiten oft aus der kombinierten Wirkung mehrerer Mastzellmediatoren resultieren, verfolgten die Autoren eine mutigere Strategie: gezielt den kontrollierten Zelltod in Mastzellen selbst auszulösen.
Ein überraschender Kandidat aus der Psychiatrie
Das Team konzentrierte sich auf „lysosomotrope“ Wirkstoffe — kleine, schwach basische Moleküle, die sich in sauren Kompartimenten wie Lysosomen und Mastzellgranula anreichern. In hohen Konzentrationen können diese Wirkstoffe die Granulamembranen schwächen und zum Auslaufen bringen, was manchmal zum Zelltod führt. Trifluoperazin, das lange zur Behandlung von Schizophrenie und Angststörungen eingesetzt wurde, gehört zu einer Wirkstoffklasse, die dafür bekannt ist, sich in solchen sauren Kompartimenten anzusammeln. Die Forscher testeten Trifluoperazin an verschiedenen Maus- und menschlichen Zellen, darunter glatte Atemwegsmuskulaturzellen, Fibroblasten, Epithelzellen, Neutrophile, Eosinophile und mehrere Mastzellpopulationen. Sie fanden heraus, dass klinisch relevante Dosen für Mastzellen auffallend toxisch waren, während die meisten anderen Zelltypen weitgehend verschont blieben; lediglich Eosinophile, eine weitere granuläre Immunzellart, zeigten bei höheren Dosen eine gewisse Empfindlichkeit.

Wie das Medikament die Selbstzerstörung auslöst
Um zu verstehen, was in Mastzellen nach Trifluoperazin-Exposition geschieht, verfolgten die Wissenschaftler zeitlich die Veränderungen in Granula und Zellgesundheit. Kurz nach der Behandlung zeigten viele Mastzellen klassische Anzeichen der Apoptose, einer ordentlichen, nicht-entzündlichen Form des programmierten Zelltods: Sie banden Annexin V, zeigten DNA-Fragmentierung, schrumpften und bildeten Membranausstülpungen, während ihre äußere Membran intakt blieb. Messungen mit pHsensitiven Farbstoffen zeigten, dass Trifluoperazin die Granula weniger sauer machte und gleichzeitig die umgebende Zellflüssigkeit saurer werden ließ — ein Hinweis darauf, dass Protonen und andere Inhaltsstoffe aus den Granula ausliefen. Eine wichtige Mastzellenzyme, Tryptase, die normalerweise in den Granula eingeschlossen ist, wurde kurz nach der Medikamentenexposition im Zellinnenraum nachgewiesen, was bestätigt, dass Granulamembranen durchlässig geworden waren.
Granula im Zentrum der Wirkung
Mikroskopie bot ein visuelles Fenster für diesen Prozess. Unter dem Elektronenmikroskop zeigten unbehandelte Mastzellen dichte, gut strukturierte Granula. Nach Trifluoperazin-Behandlung schwollen diese Granula an, verloren einen Großteil ihres inneren Materials und zeigten manchmal sichtbare Brüche in ihren Membranen, konsistent mit Auslaufen in das Zellinnere. Als die Forscher die säurepumpende V-ATPase blockierten, die normalerweise die Granula sauer hält, konnte Trifluoperazin die Granula nicht mehr effizient deacidifizieren, Tryptase nicht in das Zytosol verlagern, keine DNA-Fragmentierung auslösen und die Mastzellen nicht mehr töten. Dieser starke Schutz zeigte, dass die Granulasäure entscheidend für die zerstörerische Wirkung des Wirkstoffs ist. Überraschenderweise spielten Enzyme namens Caspasen — zentrale Vollstrecker vieler Apoptoseformen — hier nur eine kleine Rolle. Stattdessen schienen andere Proteasen, insbesondere eine Untergruppe von Serinproteasen, zu beeinflussen, ob die Zellen in einer geordneten apoptotischen Weise oder eher in einer schädlicheren nekroseähnlichen Weise starben.
Was das für künftige Behandlungen bedeuten könnte
Insgesamt zeigt die Studie, dass Trifluoperazin Mastzellen selektiv töten kann, indem es ihre sauren Granula destabilisiert, sodass deren eigene toxische Inhaltsstoffe auslaufen und einen weitgehend caspaseunabhängigen, apoptoseähnlichen Tod antreiben. Da Mastzellen Schlüsselfiguren in vielen allergischen und entzündlichen Erkrankungen sind und Trifluoperazin bereits ein zugelassenes Medikament ist, legt dieser granulavermittelte Weg nahe, dass es vielversprechend sein könnte, solche Verbindungen für den klinischen Einsatz umzunutzen oder zu verfeinern. Prinzipiell könnte eine sorgfältig gezielte Dosierung die Mastzellzahlen in betroffenen Geweben — etwa in den Atemwegen bei Asthma oder in Nasenpolypen — reduzieren, ohne benachbarte Zellen breit zu schädigen, und so eine neue Strategie bieten, mastzellgetriebene Erkrankungen abzuschwächen.
Zitation: Vraila, M., Hu Frisk, J.M., Mayavannan, A. et al. Trifluoperazine causes mast cell apoptosis through a secretory granule-mediated pathway. Cell Death Discov. 12, 185 (2026). https://doi.org/10.1038/s41420-026-03122-x
Schlüsselwörter: Mastzellen, Trifluoperazin, Allergietherapie, granula-vermittelte Apoptose, lysosomotrope Wirkstoffe