Clear Sky Science · ru
Трифлуоперазин вызывает апоптоз тучных клеток через путь, опосредованный секреторными гранулами
Превращение психиатрического препарата в средство против аллергии
Люди с аллергиями, астмой или некоторыми воспалительными заболеваниями часто страдают из‑за одного типа иммунных клеток — тучных клеток. В этом исследовании рассматривается неожиданный подход: перепрофилирование старого антипсихотического препарата трифлуоперазина для избирательного удаления вредных тучных клеток при щадящем отношении к большинству других клеток. Раскрывая точный механизм, по которому препарат вызывает самоуничтожение тучных клеток, работа открывает потенциально новый путь лечения аллергических и тучноклеточно‑опосредованных состояний.
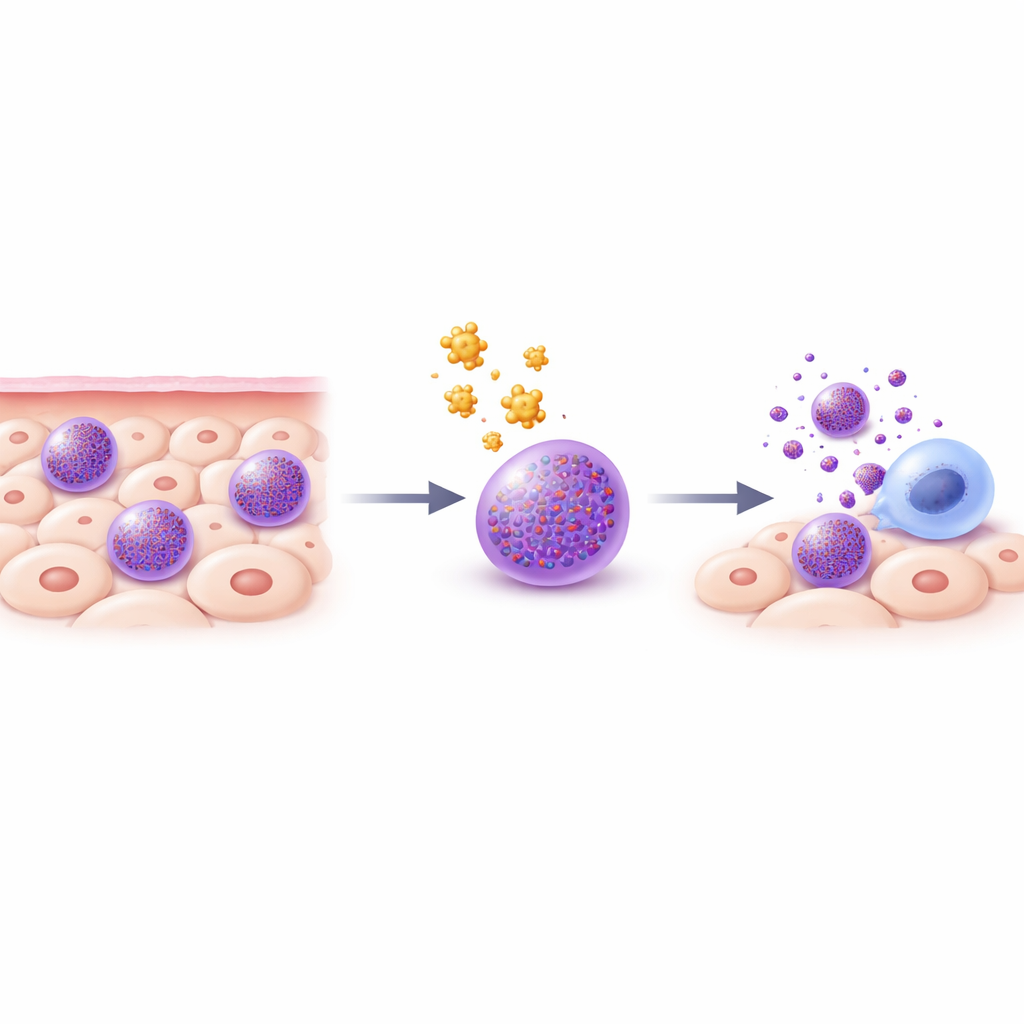
Клетка, создающая проблему
Тучные клетки — это иммунные сторожа, расположенные в тканях, таких как кожа, легкие и кишечник. Они заполнены крошечными кислыми хранилищами — гранулами, содержащими мощные вещества, такие как гистамин, ферменты и провоспалительные молекулы. При активации тучных клеток — например во время аллергической реакции — гранулы быстро освобождают содержимое, что вызывает отек, зуд и другие симптомы. Существующие методы лечения, такие как антигистаминные или стабилизирующие тучные клетки препараты, блокируют лишь часть многочисленных медиаторов, которые могут выделять тучные клетки. Поскольку заболевания часто обусловлены совместным действием нескольких медиаторов, авторы предложили более решительную стратегию: избирательно вызвать контролируемую гибель самих тучных клеток.
Неожиданный кандидат из психиатрии
Команда сосредоточилась на «лизосомотропных» препаратах — мелких слабоосновных молекулах, накапливающихся в кислых компартментах, таких как лизосомы и гранулы тучных клеток. При достаточной концентрации эти препараты могут ослаблять мембраны гранул и вызывать их протекание, что иногда приводит к гибели клетки. Трифлуоперазин, долго применяемый при шизофрении и тревоге, принадлежит к семейству препаратов, известных тем, что накапливаются в таких кислых компартментах. Исследователи проверили трифлуоперазин на ряде мышиных и человеческих клеток, включая гладкомышечные клетки дыхательных путей, фибробласты, эпителиальные клетки, нейтрофилы, эозинофилы и несколько популяций тучных клеток. Они обнаружили, что в клинически релевантных дозах препарат оказался резко токсичен для тучных клеток, не причиняя значительного вреда большинству других типов клеток; лишь эозинофилы, другой тип гранулообильных иммунных клеток, показали некоторую чувствительность при более высоких дозах.

Как препарат запускает самоуничтожение
Чтобы понять, что происходит внутри тучных клеток при воздействии трифлуоперазина, ученые отслеживали изменения гранул и состояние клеток во времени. Вскоре после лечения многие тучные клетки демонстрировали классические признаки апоптоза — аккуратной, невызывающей воспаления формы программируемой гибели: связывание Annexin V, фрагментация ДНК, уменьшение размера и образование мембранных блеbbов при сохранении целостности внешней мембраны. Измерения с помощью pH‑чувствительных красителей показали, что трифлуоперазин делает гранулы менее кислыми и одновременно делает окружающую цитоплазму более кислой — что свидетельствует о выходе протонов и других компонентов из гранул. Ключевой фермент тучных клеток, триптаза, обычно запертая внутри гранул, был обнаружен в цитозоле вскоре после воздействия препарата, что подтверждает проницаемость мембран гранул.
Гранулы в центре событий
Микроскопия дала визуальное подтверждение этого процесса. В электронной микроскопии необработанные тучные клетки показывали плотные, хорошо структурированные гранулы. После лечения трифлуоперазином гранулы набухали, теряли большую часть внутреннего содержимого и иногда демонстрировали видимые разрывы мембран, что согласуется с утечкой в клетку. Когда исследователи блокировали V‑ATPase — насос, поддерживающий кислотность гранул, — трифлуоперазин больше не мог эффективно делаить гранулы менее кислыми, перемещать триптазу в цитозоль, фрагментировать ДНК или убивать тучные клетки. Эта сильная защита показала, что кислотность гранул критична для разрушающего эффекта препарата. Удивительно, но каспазы — центральные исполнители во многих формах апоптоза — здесь играли лишь незначительную роль. Вместо этого другие протеазы, особенно подгруппа сериновых протеаз, по‑видимому, влияли на то, погибнет ли клетка упорядоченным апоптозным образом или более разрушительно, наподобие некроза.
Что это может значить для будущих терапий
В целом исследование показывает, что трифлуоперазин может избирательно убивать тучные клетки, дестабилизируя их кислые гранулы, из‑за чего собственное токсичное содержимое гранул просачивается наружу и вызывает в основном каспазо‑независимую, апоптозоподобную гибель. Поскольку тучные клетки являются ключевыми виновниками многих аллергических и воспалительных заболеваний, а трифлуоперазин уже одобрен для медицинского применения, этот путь, опосредованный гранулами, представляет собой перспективную возможность перепрофилирования или доработки подобных соединений для клинического использования. В принципе, при аккуратном таргетировании дозы можно было бы сократить число тучных клеток в пораженных тканях — например в дыхательных путях при астме или при назальных полипах — не нанеся широкого вреда соседним клеткам, что предлагает новую стратегию ослабления тучноклеточно‑опосредованных заболеваний.
Цитирование: Vraila, M., Hu Frisk, J.M., Mayavannan, A. et al. Trifluoperazine causes mast cell apoptosis through a secretory granule-mediated pathway. Cell Death Discov. 12, 185 (2026). https://doi.org/10.1038/s41420-026-03122-x
Ключевые слова: тучные клетки, трифлуоперазин, терапия аллергии, апоптоз, опосредованный гранулами, лизосомотропные препараты