Clear Sky Science · sv
SIRT1-brist främjar åldersrelaterat hjärtsvikt genom att öka ferroptos via GATA4-HADHA-GPX4-axeln
Varför åldrande hjärtan har det svårt
När människor lever längre utvecklar fler av oss hjärtsvikt, ett tillstånd där hjärtat inte längre kan pumpa blod effektivt. Läkare har länge känt till att åldrande och ökat oxidativt ”slitage” skadar hjärtat, men exakt vilken typ av celldegeneration som är inblandad har varit oklart. Den här studien avslöjar en specifik järndriven form av celldöd i hjärtmuskeln och kartlägger en kedja av molekylära händelser som kan förklara varför äldre hjärtan fallerar – och hur vi kanske kan bromsa eller förhindra den nedgången.
Järn, rost och sviktande hjärtan
Forskarna började med att jämföra unga och gamla råttor. De äldre djuren visade försvagad pumpfunktion, tjockare och stelare hjärtväggar samt högre blodnivåer av ett stresshormon som frisätts från ansträngda hjärtan. Inuti hjärtvävnaden fann teamet fler reaktiva syreradikaler – mycket reaktiva molekyler som kan skada fetter, proteiner och DNA – och tydliga tecken på lipidperoxidation, i praktiken en ”rostning” av de fettkomponenter som bygger upp cellmembran. De observerade också järnansamling och minskade nivåer av enzymet GPX4, som normalt neutraliserar farliga fettoxidanter. Tillsammans pekar dessa förändringar mot ferroptos, en nybeskriven typ av celldöd där järn och oxiderade fetter samverkar för att döda celler.
Bevisa att järndriven celldöd spelar roll
För att testa om denna järnrelaterade celldöd verkligen driver hjärtsvikt snarare än bara följer med den, manipulerade forskarna järnnivåer och det skyddande enzymet GPX4. Att ge åldrande råttor en diet rik på järn förvärrade hjärtfunktionen, ökade ärrbildning och undertryckte ytterligare GPX4. Tvärtom förbättrade behandling med ferrostatin-1, ett läkemedel som specifikt blockerar ferroptos, hjärtats pumpförmåga, minskade ärrbildning och återställde mer normala järnhanterande proteiner. Hos möss gjorde selektiv radering av GPX4 i hjärtmuskelceller åldersrelaterade skador och dysfunktion värre, medan förstärkning av GPX4 via en genterapivektor bevarade funktionen i en separat åldringsmodell. Dessa experiment antyder starkt att ferroptos inte bara är närvarande i åldrande hjärtan – den bidrar aktivt till deras försämring.
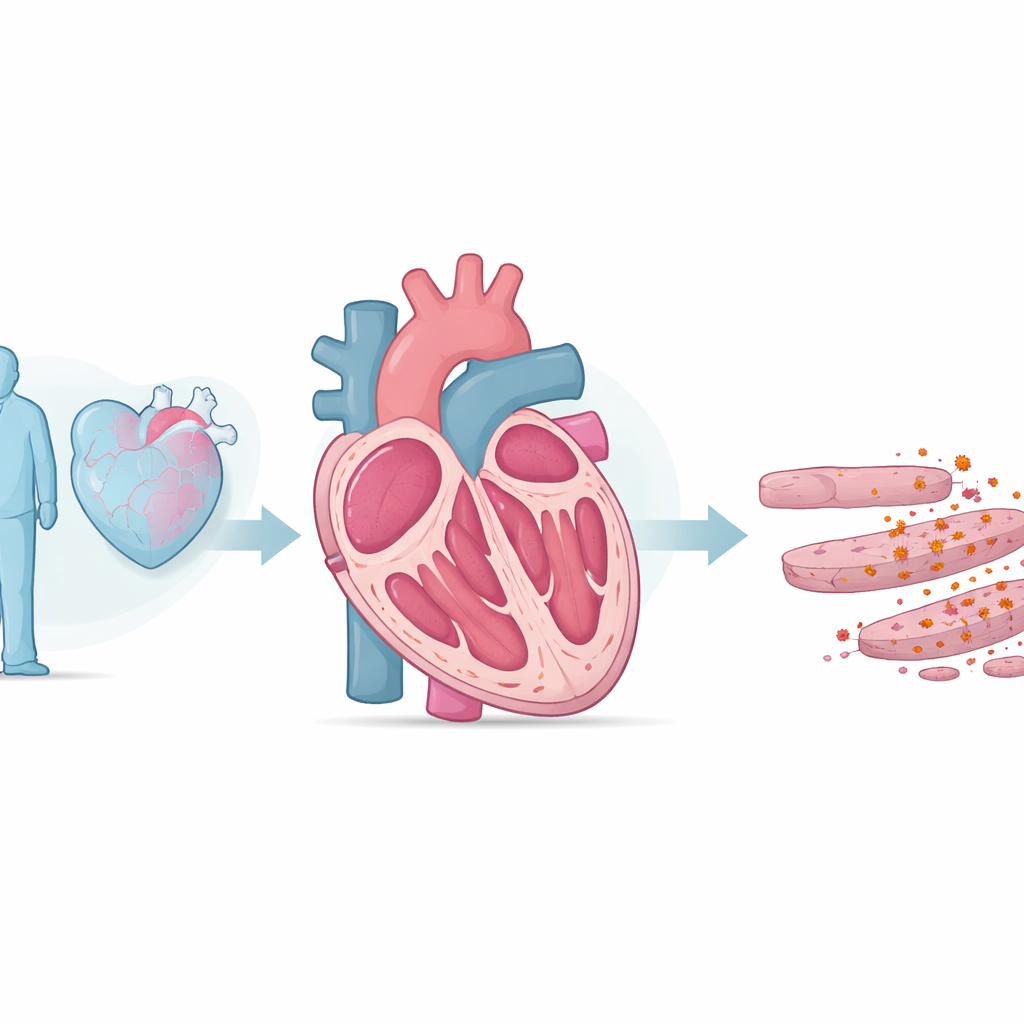
En metabolisk svag punkt inne i hjärtcellerna
För att hitta vad som gör åldrande hjärtceller mer utsatta för ferroptos skannade teamet tusentals proteiner i råtthjärtan och fann en påtaglig minskning av ett mitokondriellt enzym kallat HADHA, särskilt när gamla djur exponerades för extra järn. HADHA hjälper hjärtceller att förbränna fetter effektivt och att bevara friska mitokondriemembran. När forskarna minskade HADHA specifikt i hjärtceller hos unga möss utvecklade djuren mer fibros och biokemiska tecken på ferroptos – förändringar som kunde återställas med en ferroptoshämmare. I isolerade hjärtceller störde minskad HADHA mitokondrielfunktionen, ökade mängden reaktiva syreradikaler, tömde antioxidantmolekylen glutation och undertryckte ytterligare GPX4. Återställande av HADHA gav motsatt effekt, räddade energiproduktion och antioxidantförsvar. Detta placerar HADHA som en avgörande metabolisk skyddsmekanism som hindrar hjärtceller från att falla i järndriven celldöd.
En åldringsomkopplare: SIRT1 och dess nedströmsparter
Nästa fråga var varför HADHA minskar med ålder. Författarna fokuserade på SIRT1, ett protein som länge förknippats med livslängd och skydd mot åldersrelaterade sjukdomar. I åldrande hjärtan sjönk SIRT1-nivåerna i takt med HADHA. I cellförsök ledde nedstängning av SIRT1 till minskningar av både HADHA och GPX4 och försköt järnhanterande proteiner mot en mer riskfylld profil. Teamet upptäckte att SIRT1 interagerar med en annan protein, transkriptionsfaktorn GATA4, som normalt ökar produktionen av HADHA. När SIRT1-aktiviteten avtar försvagas GATA4:s förmåga att slå på HADHA-genen, vilket får HADHA-nivåerna att sjunka och mitokondriell stress att öka. Viktigt är att aktivering av SIRT1 med resveratrol, en småmolekyl ofta omdiskuterad i samband med ”hälsosamt åldrande”, eller genom direkt överuttryck av SIRT1 i hjärtceller återställde GATA4 och HADHA, stärkte antioxidantförsvaret, minskade ferroptos och förbättrade hjärtfunktionen i åldringsmodeller hos djur.
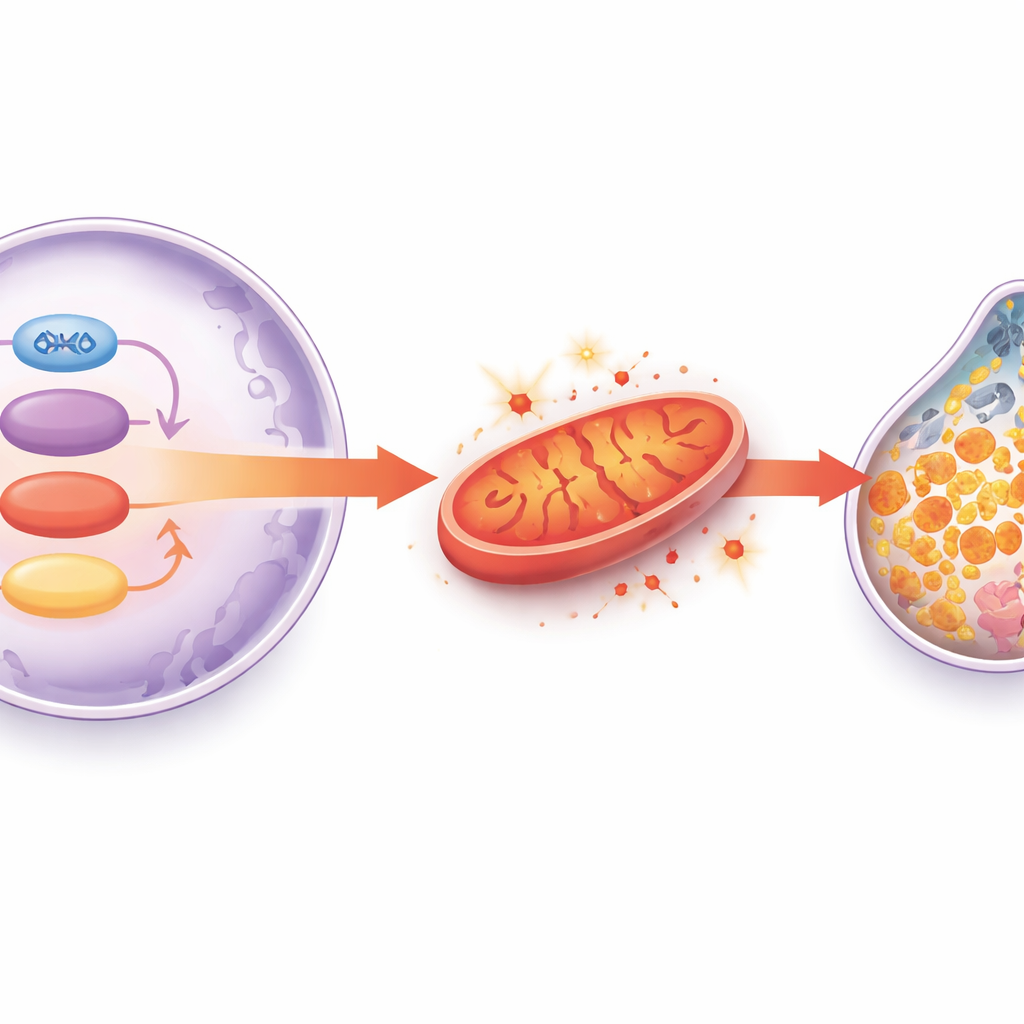
Vad detta betyder för att skydda det åldrande hjärtat
Sammanfattningsvis beskriver studien en händelsekedja: när hjärtan åldras minskar SIRT1-aktiviteten, GATA4 kan inte längre upprätthålla HADHA-nivåerna, mitokondrierna sviktar och skickar ut reaktiva syreradikaler, antioxidantssystemet centrerat kring glutation och GPX4 kollapsar, och järndriven ferroptos tar död på hjärtmuskelceller. Denna gradvisa förlust av celler och ökade fibros försvagar så småningom hjärtats pumpförmåga. Även om resultaten härstammar från djur- och cellmodeller antyder de att läkemedel eller livsstilsstrategier som bevarar SIRT1-aktivitet, stödjer HADHA och mitokondriell metabolism eller direkt blockerar ferroptos en dag kan hjälpa till att förebygga eller behandla åldersrelaterad hjärtsvikt hos människor.
Citering: Duan, Y., Luo, Y., Han, X. et al. SIRT1 deficiency promotes age-related heart failure through enhancing ferroptosis via GATA4-HADHA-GPX4 axis. Cell Death Dis 17, 343 (2026). https://doi.org/10.1038/s41419-026-08634-z
Nyckelord: åldrande hjärtsvikt, ferroptos, SIRT1-vägen, mitokondriell dysfunktion, kardiomyocytdöd