Clear Sky Science · ar
نقص SIRT1 يعزز فشل القلب المرتبط بالتقدم في العمر عبر تعزيز الفيروبتوزيس عبر محور GATA4-HADHA-GPX4
لماذا تواجه القلوب المتقدمة في العمر صعوبات
مع طول عمر الناس أصبح المزيد منا يعاني من فشل القلب، الحالة التي يعجز فيها القلب عن ضخ الدم بفعالية. لطالما عرف الأطباء أن التقدّم في العمر والضرر التأكسدي الزائد يسببان تآكل القلب، لكن نوع الضرر الخلوي المحدد ظل غامضاً. تكشف هذه الدراسة شكلاً محدداً من موت الخلايا المدفوع بالحديد في عضلة القلب، وترسم سلسلة من الأحداث الجزيئية التي قد تفسر سبب فشل القلوب الأكبر سناً — وكيف يمكن أن نبطئ أو نمنع هذا التدهور.
الحديد والصدأ والقلوب المتداعية
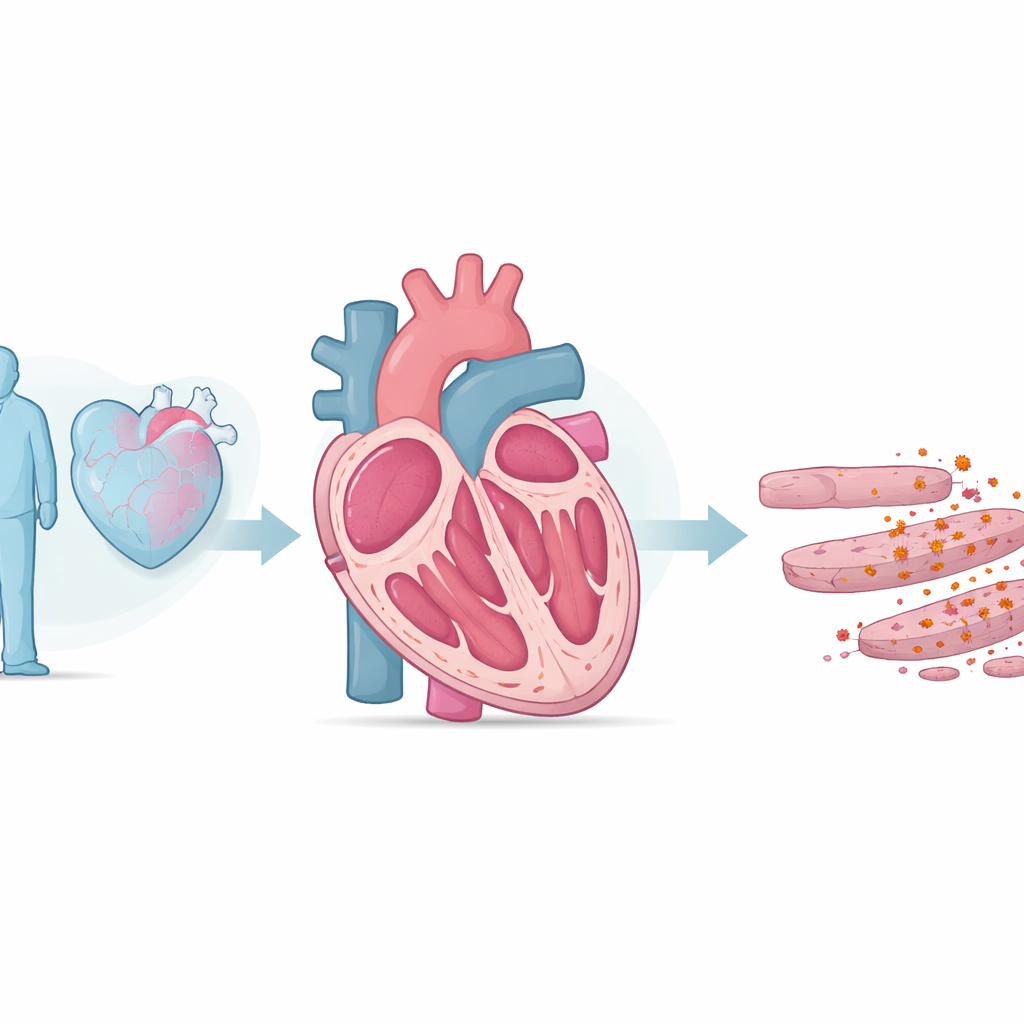
بدأ الباحثون بمقارنة جرذان شابة وقديمة. أظهرت الحيوانات الأكبر سناً ضعفاً في وظيفة الضخ، وسمكاً وتصلباً أكبر لجدران القلب، ومستويات دم أعلى لهرمون توتر يفرزه القلب المتعب. داخل أنسجة قلبهم وجد الفريق مزيداً من أنواع الأكسجين التفاعلية — جزيئات شديدة التفاعل يمكنها إتلاف الدهون والبروتينات والحمض النووي — وعلامات قوية على بيروكسدة الدهون، أي «صدأ» مكونات الدهون في أغشية الخلايا. لاحظوا أيضاً تراكم الحديد وانخفاض مستويات إنزيم واقٍ يدعى GPX4، الذي عادة ما يحيد المؤكسدات الدهنية الضارة. معاً، تشير هذه التغيرات إلى الفيروبتوزيس، نوع حديث الوصف من موت الخلايا حيث يتآزر الحديد والدهون المؤكسدة لقتل الخلايا.
إثبات أن موت الخلايا المدفوع بالحديد ذو تأثير فعلي
لاختبار ما إذا كان هذا الموت الخلوي المرتبط بالحديد يقود فعلاً فشل القلب بدلاً من كونه حدثاً مصاحباً فقط، عبث العلماء بمستويات الحديد والإنزيم الواقي GPX4. أدّى إطعام الجرذان الكبيرة سناً نظاماً غنياً بالحديد إلى تفاقم وظيفة القلب وتزايد التندّب وقمع GPX4 أكثر. في المقابل، أدى علاج الجرذان الكبيرة بمثبط الفيروبتوزيس المحدد فيروستاتين-1 إلى تحسّن في الضخ القلبي، وتقليل التندّب، واستعادة بروتينات معالجة الحديد إلى وضع أكثر طبيعية. في الفئران، جعل حذف GPX4 مخصصاً في خلايا عضلة القلب الضرر والضعف المرتبطين بالشيخوخة أسوأ، بينما حافظ تعزيز GPX4 عبر ناقل علاج جيني على الوظيفة في نموذج شيخوخة آخر. تقترح هذه التجارب بقوة أن الفيروبتوزيس ليس مجرد وجود في القلوب المسنة — بل يساهم بنشاط في تدهورها.
نقطة ضعف أيضية داخل خلايا القلب
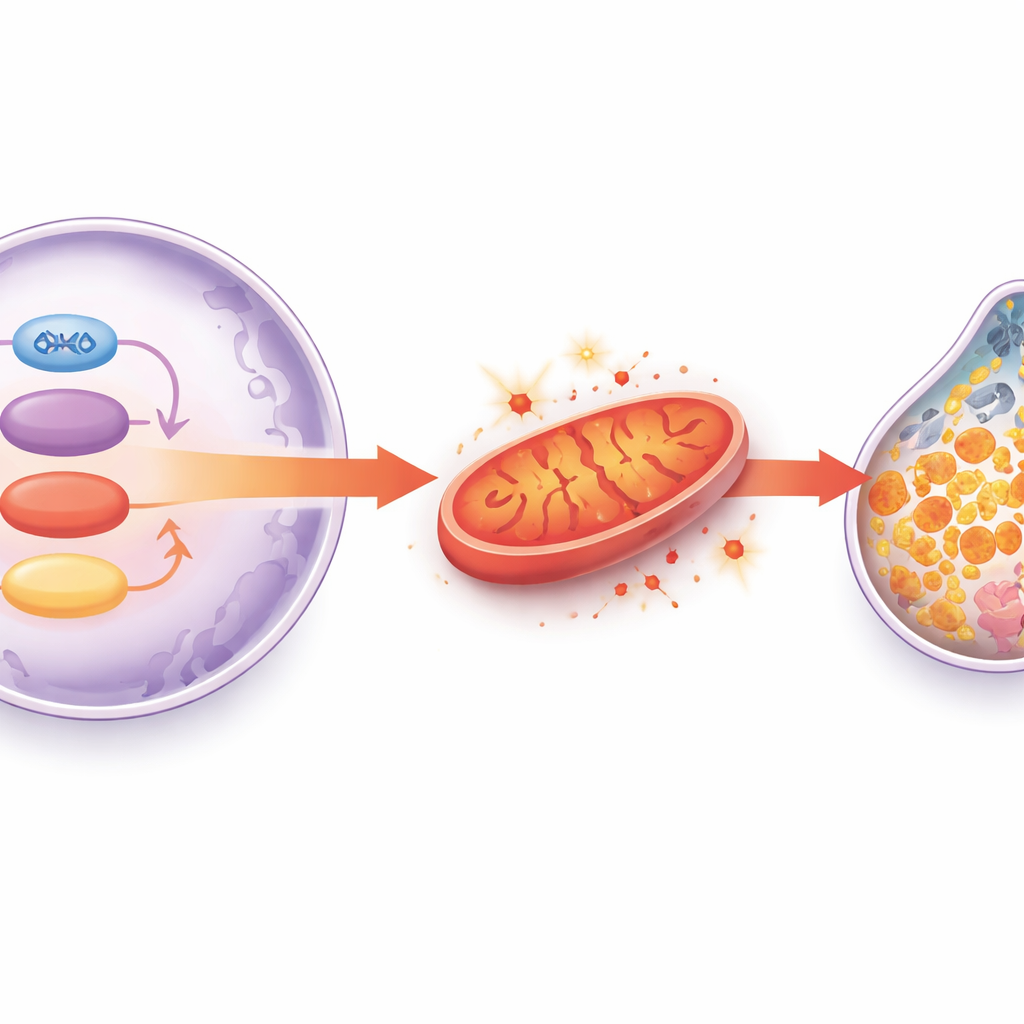
بحثاً عمّا يجعل خلايا القلب المسنة أكثر عرضة للفيروبتوزيس، مسح الفريق آلاف البروتينات في قلوب الجرذان ووجد انخفاضاً لافتاً في إنزيم ميتوكوندري يُدعى HADHA، لا سيما عندما تعرضت الحيوانات الكبيرة لسعة إضافية من الحديد. يساعد HADHA خلايا القلب على حرق الدهون بكفاءة والحفاظ على أغشية الميتوكوندريا صحية. عندما قلل العلماء HADHA تحديداً في خلايا قلب فئران شابة، طورت الحيوانات المزيد من التليف وعلامات بيوكيميائية للفيروبتوزيس، وهي تغييرات أمكن عكسها بمثبط الفيروبتوزيس. في خلايا القلب المعزولة، أدّى خفض HADHA إلى تعطيل وظيفة الميتوكوندريا، وزيادة أنواع الأكسجين التفاعلية، واستنزاف مضاد الأكسدة غلوتاثيون، وقمع GPX4 أكثر. أما استعادة HADHA فكان لها الأثر المعاكس، إذ أنقذت إنتاج الطاقة والدفاعات المضادة للأكسدة. هذا يضع HADHA كحارس أيضي حاسم يمنع خلايا القلب من الانزلاق نحو موت مدفوع بالحديد.
مفتاح الشيخوخة: SIRT1 وشركاؤه السفليون
السؤال التالي كان لماذا ينخفض HADHA مع التقدّم في العمر. ركز المؤلفون على SIRT1، بروتين مرتبط منذ زمن طويل بطول العمر والحماية من الأمراض المرتبطة بالشيخوخة. في القلوب المسنة انخفضت مستويات SIRT1 جنباً إلى جنب مع HADHA. في تجارب خلوية، أدّى إيقاف SIRT1 إلى خفض كل من HADHA وGPX4 وتحويل بروتينات معالجة الحديد إلى ملف أكثر خطورة. اكتشف الفريق أن SIRT1 يتفاعل مع بروتين آخر، عامل النسخ GATA4، الذي يعزز عادة إنتاج HADHA. عندما تضعف فعالية SIRT1، تضعف قدرة GATA4 على تشغيل جين HADHA، مما يؤدي إلى انخفاض مستويات HADHA وتصاعد إجهاد الميتوكوندريا. وهو أمر مهم، إذ أن تنشيط SIRT1 بالريزفيراترول، جزيء صغير كثير النقاش في سياق «الشيخوخة الصحية»، أو الإفراط في التعبير عن SIRT1 مباشرة في خلايا القلب أعاد GATA4 وHADHA، وعزّز دفاعات مضادات الأكسدة، وخفّض الفيروبتوزيس، وحسّن وظيفة القلب في نماذج حيوانية مسنة.
ما الذي يعنيه هذا لحماية القلب المسن
مجتمعة، تحدد الدراسة سلسلة من الأحداث: مع تقدّم القلب في العمر تنخفض فعالية SIRT1، تعجز GATA4 عن الحفاظ على مستويات HADHA، تضعف الميتوكوندريا وتطلق أنواع أكسجينية تفاعلية، ينهار نظام مضادات الأكسدة القائم على الغلوتاثيون وGPX4، ويقتل الفيروبتوزيس القائم على الحديد خلايا عضلة القلب. هذا الفقدان التدريجي للخلايا وارتفاع التندّب يضعفان في النهاية قدرة القلب على الضخ. رغم أن هذه النتائج مستمدة من نماذج حيوانية وخلوية، فإنها تشير إلى أن أدوية أو استراتيجيات نمط حياة تحافظ على نشاط SIRT1، تدعم HADHA وأيض الميتوكوندريا، أو تحجب الفيروبتوزيس مباشرة قد تساعد يوماً ما في الوقاية أو علاج فشل القلب المرتبط بالعمر لدى البشر.
الاستشهاد: Duan, Y., Luo, Y., Han, X. et al. SIRT1 deficiency promotes age-related heart failure through enhancing ferroptosis via GATA4-HADHA-GPX4 axis. Cell Death Dis 17, 343 (2026). https://doi.org/10.1038/s41419-026-08634-z
الكلمات المفتاحية: فشل القلب المرتبط بالشيخوخة, الفيروبتوزيس, مسار SIRT1, خلل الميتوكوندريا, موت الخلايا القلبية