Clear Sky Science · ru
Дефицит SIRT1 стимулирует возрастную сердечную недостаточность через усиление ферроптоза по оси GATA4-HADHA-GPX4
Почему стареющие сердца испытывают затруднения
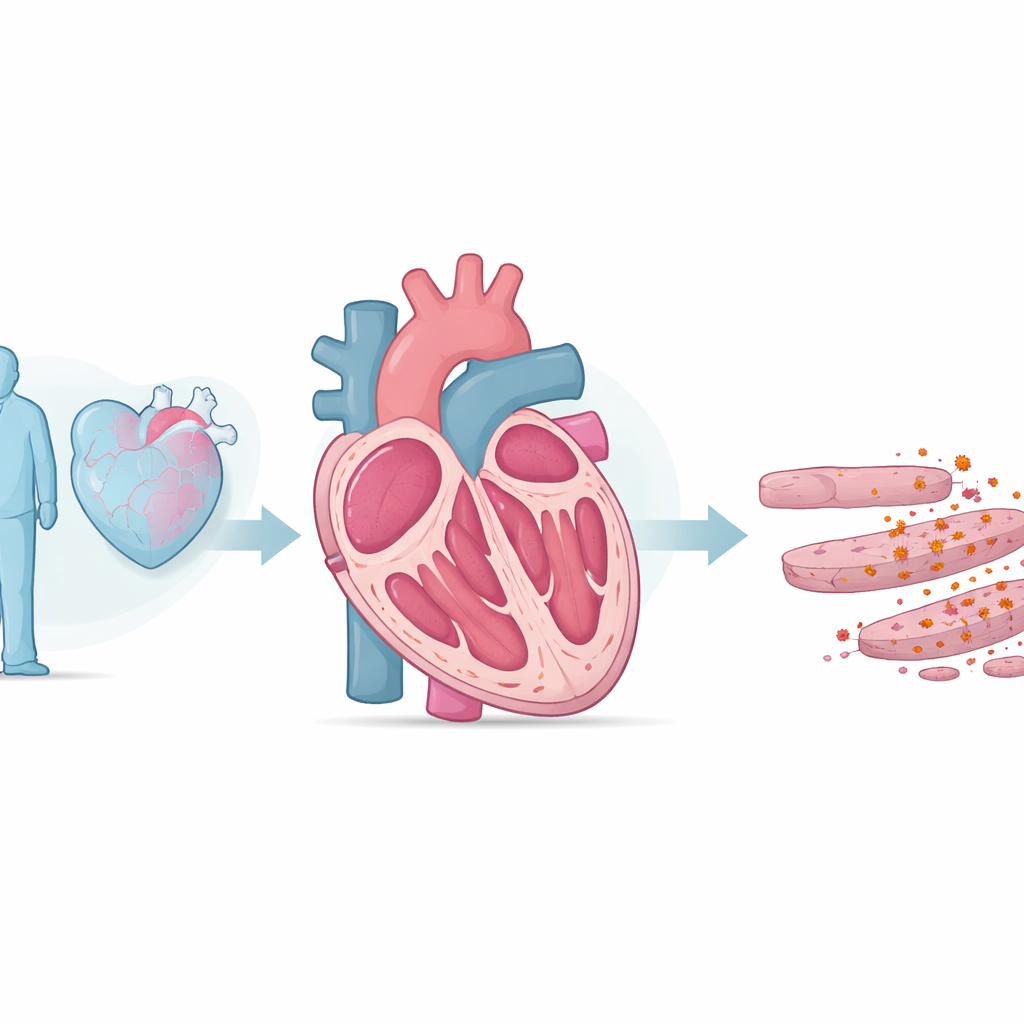
По мере того как люди живут дольше, у всё большего числа развивается сердечная недостаточность — состояние, при котором сердце больше не может эффективно перекачивать кровь. Врачи давно знали, что старение и избыточное окислительное «изнашивание» повреждают сердце, но точный характер вовлечённого поражения клеток оставался неясным. В этом исследовании выявлена специфическая железозависимая форма гибели клеток в сердечной мышце и прослежен каскад молекулярных событий, который может объяснять, почему сердца стареют — и как мы могли бы замедлить или предотвратить этот спад.
Железо, ржавчина и слабое сердце
Исследователи начали с сравнения молодых и старых крыс. У старых животных наблюдалась ослабленная сократительная функция, утолщённые и более жёсткие стенки сердца, а также повышенные уровни в крови гормона стресса, выделяемого при перегрузке сердца. В тканях сердца команда обнаружила больше реактивных форм кислорода — высокоактивных молекул, которые могут повреждать липиды, белки и ДНК — и явные признаки перекисного окисления липидов, по сути «ржавления» жировых компонентов клеточных мембран. Также отмечалось накопление железа и снижение уровня защитного фермента GPX4, который обычно нейтрализует опасные липидные окислители. Вместе эти изменения указывают на ферроптоз — недавно описанный тип гибели клеток, при котором железо и окисленные липиды совместно приводят к гибели клеток.
Доказательство значимости железозависимой гибели клеток
Чтобы проверить, является ли эта железозависимая гибель клеток драйвером сердечной недостаточности, а не просто сопутствующим явлением, учёные манипулировали уровнями железа и ключевого защитного фермента GPX4. Высокожелезная диета у старых крыс ухудшала функцию сердца и увеличивала фиброз, а также ещё сильнее подавляла GPX4. Напротив, лечение старых крыс ферростатином-1 — препаратом, который избирательно блокирует ферроптоз — улучшало сократительную функцию сердца, снижало фиброз и восстанавливало более нормальный профиль белков, отвечающих за обмен железа. У мышей удаление GPX4 специально в кардиомиоцитах усугубляло возрастные повреждения и дисфункцию, тогда как повышение экспрессии GPX4 с помощью векторной генной терапии сохраняло функцию в другой модели старения. Эти эксперименты убедительно свидетельствуют о том, что ферроптоз не просто присутствует в стареющих сердцах — он активно способствует их упадку.
Метаболическая уязвимость внутри сердечных клеток
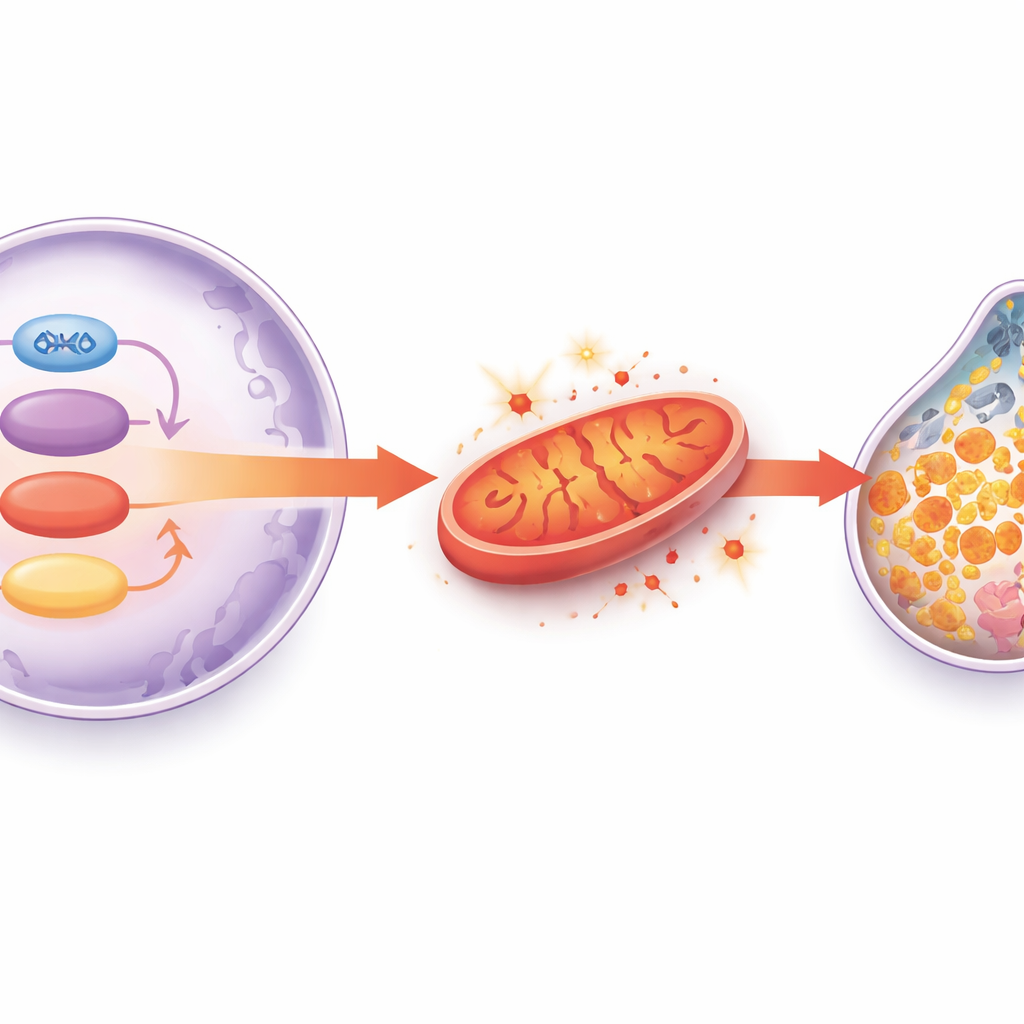
Ища причину повышенной восприимчивости стареющих кардиомиоцитов к ферроптозу, команда просканировала тысячи белков в сердцах крыс и обнаружила резкое снижение митохондриального фермента HADHA, особенно у старых животных при дополнительном поступлении железа. HADHA помогает клеткам сердца эффективно сжигать жиры и поддерживать здоровые митохондриальные мембраны. Когда учёные специфически уменьшали уровень HADHA в кардиомиоцитах молодых мышей, у животных развивался усиленный фиброз и биохимические признаки ферроптоза — изменения, которые можно было обратить с помощью ингибитора ферроптоза. В изолированных сердечных клетках понижение HADHA нарушало митохондриальную функцию, увеличивало образование реактивных форм кислорода, истощало антиоксидантный глутатион и ещё сильнее подавляло GPX4. Восстановление HADHA давало обратный эффект, спасая энергетический метаболизм и антиоксидантную защиту. Это ставит HADHA в ряд ключевых метаболических щитов, которые не дают сердечным клеткам соскользнуть в железозависимую гибель.
Переключатель старения: SIRT1 и его нисходящие партнёры
Следующий вопрос — почему HADHA уменьшается с возрастом. Авторы сосредоточились на SIRT1, белке, давно связанном с продолжительностью жизни и защитой от возрастных заболеваний. В стареющих сердцах уровни SIRT1 падали вместе с HADHA. В клеточных экспериментах подавление SIRT1 снижало и HADHA, и GPX4, а также смещало белки, управляющие железом, в более опасный профиль. Команда обнаружила, что SIRT1 взаимодействует с другим белком — транскрипционным фактором GATA4, который обычно повышает продукцию HADHA. Когда активность SIRT1 ослаблялась, способность GATA4 включать ген HADHA ухудшалась, что приводило к падению уровней HADHA и росту митохондриального стресса. Важно, что активация SIRT1 ресвератролом — малой молекулой, часто обсуждаемой в контексте «здорового старения» — или прямая сверхэкспрессия SIRT1 в кардиомиоцитах восстанавливала GATA4 и HADHA, укрепляла антиоксидантные механизмы, снижала ферроптоз и улучшала функцию сердца в моделях старения животных.
Что это значит для защиты стареющего сердца
В совокупности исследование описывает цепочку событий: с возрастом активность SIRT1 падает, GATA4 теряет способность поддерживать уровни HADHA, митохондрии дают сбой и выбрасывают реактивные формы кислорода, антиоксидантная система, основанная на глутатионе и GPX4, рушится, и железозависимый ферроптоз уничтожает кардиомиоциты. Постепенная потеря клеток и рост фиброза в конечном счёте ослабляют сократительную способность сердца. Хотя эти результаты получены в животных и клеточных моделях, они позволяют предположить, что препараты или стратегии образа жизни, которые сохраняют активность SIRT1, поддерживают HADHA и митохондриальный метаболизм или напрямую блокируют ферроптоз, однажды смогут помочь предотвратить или лечить возрастную сердечную недостаточность у людей.
Цитирование: Duan, Y., Luo, Y., Han, X. et al. SIRT1 deficiency promotes age-related heart failure through enhancing ferroptosis via GATA4-HADHA-GPX4 axis. Cell Death Dis 17, 343 (2026). https://doi.org/10.1038/s41419-026-08634-z
Ключевые слова: стареющее сердце и сердечная недостаточность, ферроптоз, путь SIRT1, митохондриальная дисфункция, гибель кардиомиоцитов