Clear Sky Science · he
חוסר SIRT1 מקדם אי‑ספיקת לב תלויה גיל באמצעות הגברה של פרופן־ברזל דרך ציר GATA4‑HADHA‑GPX4
מדוע לבבות מזדקנים מתקשים
ככל שאנשים חיים יותר זמן, יותר מתוכנו מפתחים אי‑ספיקת לב — מצב שבו הלב כבר אינו מצליח להזרים דם ביעילות. רופאים ידעו זמן רב שהזדקנות ונזק חמצוני מצטבר פוגעים בלב, אך סוג הנזק התאי המדויק נותר מעורפל. מחקר זה חושף צורת מוות תאי תלויה ברזל בשריר הלב וממפה שרשרת אירועים מולקולריים שעשויה להסביר מדוע לבבות מזדקנים נכשלות — וכיצד אפשר להאט או למנוע את השחיקה הזאת.
ברזל, חלודה ולבבות נכשלים
החוקרים התחילו בהשוואת חולדות צעירות ללא־זקנות. בבעלי החיים המבוגרים נצפו תפקוד כיווץ מוחלש, דפנות לב עבות וקשיחות גבוהה יותר, ורמות גבוהות יותר בדם של הורמון לחץ שמשתחרר מלב שנאבק. ברקמות הלב שלהם מצאו החוקרים כמות גבוהה יותר של ריאקציות חמצן תגובתיות — מולקולות מאוד תגובתיות שעלולות לפגוע בשומנים, בחלבונים וב‑DNA — וסימנים חזקים של פרוק שומנים (ליפיד פרוקסידציה), למעשה "חלודה" של מרכיבי השומן בממברנות התאים. הם גם צפו בהצטברות ברזל ורמות מופחתות של אנזים מגן בשם GPX4, שבעבר נודע כנוטרל חמצונים מסוכנים שמקורם בשומנים. שינויים אלה יחד מצביעים על פרורפטוזיס, סוג מוות תאי שתואר לאחרונה שבו ברזל ושומנים מחומצנים משולבים כדי להרוג תאים.
להוכיח שמוות תאי מונע־ברזל חשוב
כדי לבדוק האם המוות התאי התלוי ברזל אכן מניע את אי‑הספיקה ולא רק מלווה אותה, המדענים שינו את רמות הברזל ואת האנזים המגן המרכזי GPX4. תזונה עשירת ברזל לחולדות זקנות החריפה את תפקוד הלב ואת הצלקתיות והדכאה של GPX4. לעומת זאת, טיפול בחולדות זקנות ב‑ferrostatin‑1, תרופה החוסמת באופן ספציפי פרורפטוזיס, שיפר את כיווץ הלב, צמצם צלקתיות והשיב רמות תקינות יותר של חלבונים המטפלים בברזל. בעכברים, מחיקה ספציפית של GPX4 בתאי שריר הלב החריפה את נזקי הגיל והתפקוד, בעוד שהגברת GPX4 בעזרת וקטור גנטי שמרה על התפקוד במודל הזדקנות נפרד. ניסויים אלה מרמזים בחוזקה שפרורפטוזיס אינו רק נוכח בלבבות מזדקנים — הוא תורם באופן פעיל לשקיעתם.
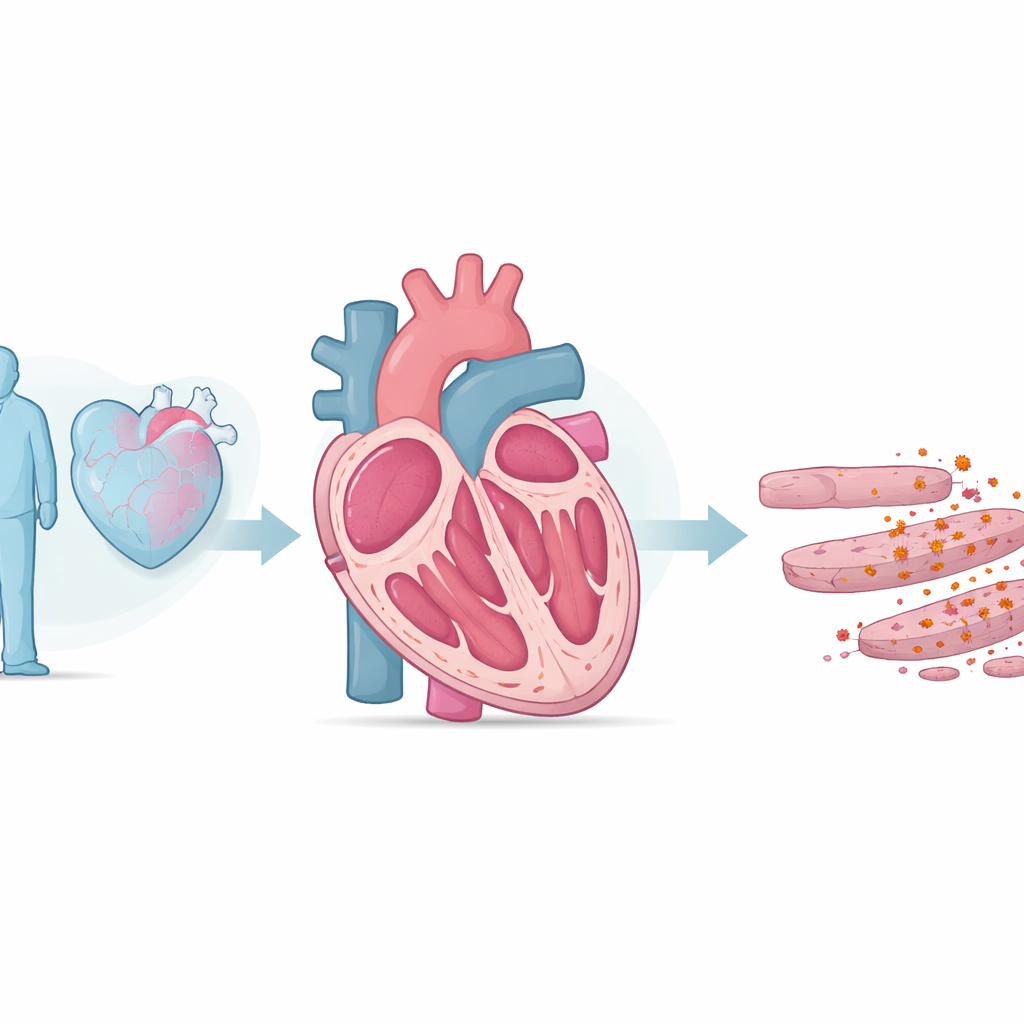
קשר מטבולי חלש בתוך תאי הלב
בחיפוש אחר מה עושה את תאי הלב המבוגרים פגיעים יותר לפרורפטוזיס, הקבוצה סרקה אלפי חלבונים בלבבות חולדות ומצאה ירידה בולטת באנזים מיטוכונדריאלי בשם HADHA, במיוחד כשהחיות המבוגרות נחשפו לברזל נוסף. HADHA מסייע לתאי הלב לשרוף שומנים ביעילות ולשמור על ממברנות מיטוכונדריאליות בריאות. כשהחוקרים צמצמו את HADHA באופן ספציפי בתאי הלב של עכברים צעירים, החיות פיתחו יותר פיברוזיס וסימנים ביוכימיים של פרורפטוזיס, שינויים שניתן היה להחזיר בעזרת מעכב פרורפטוזיס. בתאים מבודדים של הלב, הפחתת HADHA הפריעה לתפקוד המיטוכונדריה, הגברה של ריאקציות חמצן תגובתיות, דלדול של הגלוטתיון הנוגד‑חמצון ודיכוי נוסף של GPX4. השבת HADHA השפיעה הפוך והצילה את ייצור האנרגיה ואת ההגנות האנטיאוקסידנטיות. ממצא זה ממקם את HADHA כמגן מטבולי חיוני שמונע מתאי הלב להחליק לתוך מוות תלוי‑ברזל.
מفتיח הזדקנות: SIRT1 ושותפיו המורדים
השאלה הבאה הייתה מדוע HADHA יורד עם הגיל. המחברים התרכזו ב‑SIRT1, חלבון המזוהה זמן רב עם אורך חיים והגנה מפני מחלות תלויות גיל. בלבבות מזדקנים ירדו רמות SIRT1 לצד HADHA. בניסויי תאים, כיבוי SIRT1 הקטין הן את HADHA והן את GPX4 והזיז את חלבוני הטיפול בברזל לפרופיל מסוכן יותר. הקבוצה גילתה ש‑SIRT1 מתקשר עם חלבון נוסף, גורם שעתוק בשם GATA4, שבאופן רגיל מגביר את ייצור HADHA. כאשר פעילות SIRT1 פוחתת, יכולתו של GATA4 להפעיל את גן HADHA נחלשת, מה שגורם לרמות HADHA לצנוח ולמתח מיטוכונדריאלי לעלות. משמעותית, גירוי SIRT1 באמצעות רזברטרול, מולקולה קטנה שמדובר עליה בהקשר של "הזדקנות בריאה", או הבעה יתר ישירה של SIRT1 בתאי לב החזירה את GATA4 ו‑HADHA, חיזקה הגנות נוגדות חמצון, צמצמה פרורפטוזיס ושיפרה את תפקוד הלב במודלים של הזדקנות בחיות.
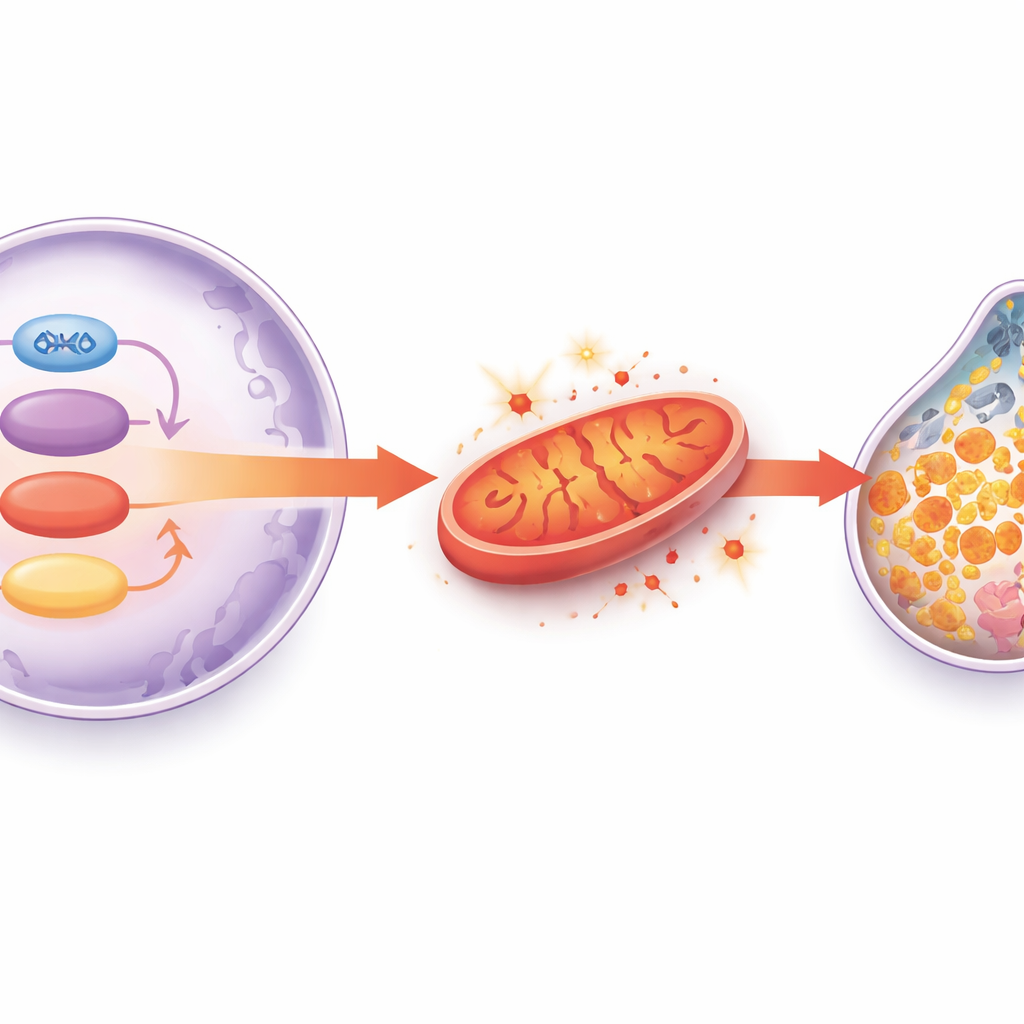
מה משמעות הממצאים להגנת הלב המזדקן
בצירוף, המחקר משרטט שרשרת אירועים: ככל שהלב מזדקן, פעילות SIRT1 פוחתת, GATA4 כבר אינה מצליחה לשמור על רמות HADHA, המיטוכונדריה נחלשות ומשחררות ריאקציות חמצן תגובתיות, מערכת הנוגדים המבוססת על גלוטתיון ו‑GPX4 קרסה, ופרורפטוזיס מונע‑ברזל הורג תאי שריר לב. אובדן הדרגתי זה של תאים ועליית הצלקתיות מחלישים לבסוף את משאבת הלב. אף שתרחישים אלה נבדקו בחיות ובמודלים תאיים, הם מצביעים על כך שתרופות או אסטרטגיות אורח‑חיים שימרזו פעילות SIRT1, יתמכו ב‑HADHA ובמטבוליזם המיטוכונדריאלי, או יחסמו פרורפטוזיס ישירות — עשויים יום אחד לסייע במניעה או בטיפול באי‑ספיקת לב תלויה גיל בבני אדם.
ציטוט: Duan, Y., Luo, Y., Han, X. et al. SIRT1 deficiency promotes age-related heart failure through enhancing ferroptosis via GATA4-HADHA-GPX4 axis. Cell Death Dis 17, 343 (2026). https://doi.org/10.1038/s41419-026-08634-z
מילות מפתח: אי‑ספיקת לב קשורה להזדקנות, פרורפטוזיס, מסלול SIRT1, תפקוד מיטוכונדריאלי לקוי, מוות תאי של קרדיומיוציטים