Clear Sky Science · es
La deficiencia de SIRT1 promueve la insuficiencia cardíaca relacionada con la edad al potenciar la ferroptosis a través del eje GATA4-HADHA-GPX4
Por qué los corazones envejecidos flaquean
A medida que las personas viven más años, un número creciente desarrolla insuficiencia cardíaca, una condición en la que el corazón ya no puede bombear sangre de forma eficaz. Los médicos saben desde hace tiempo que el envejecimiento y el exceso de “desgaste” oxidativo dañan el corazón, pero el tipo exacto de daño celular implicado ha sido poco claro. Este estudio descubre una forma específica de muerte celular impulsada por el hierro en el músculo cardíaco y traza una cadena de eventos moleculares que puede explicar por qué los corazones envejecidos fallan —y cómo podríamos ralentizar o prevenir ese deterioro.
Hierro, óxido y corazones en fallo
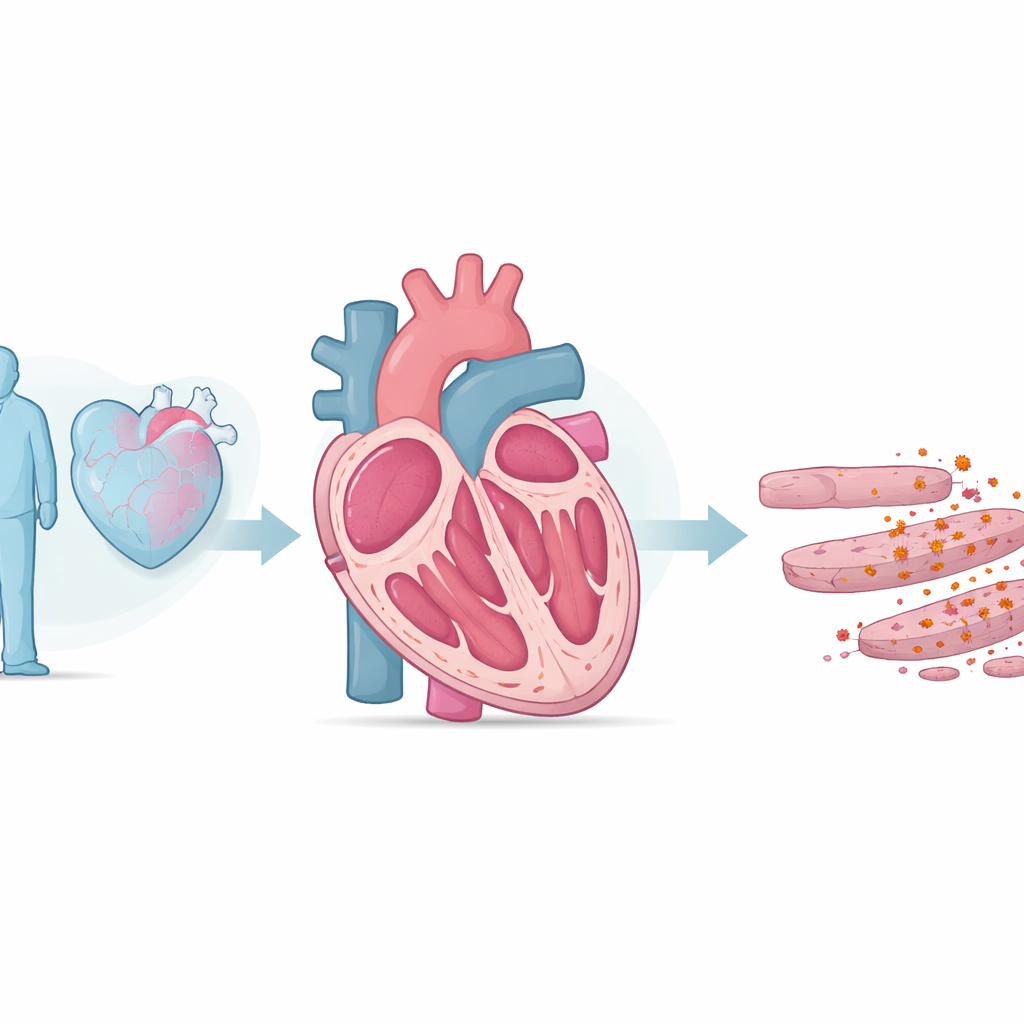
Los investigadores empezaron comparando ratas jóvenes y viejas. Los animales mayores mostraron una función de bombeo debilitada, paredes cardíacas más gruesas y rígidas, y niveles sanguíneos más altos de una hormona de estrés liberada por corazones en apuros. En su tejido cardíaco, el equipo halló más especies reactivas de oxígeno —moléculas altamente reactivas que pueden dañar lípidos, proteínas y ADN— y fuertes señales de peroxidación lipídica, básicamente un “oxidado” de los componentes grasos de las membranas celulares. También observaron acumulación de hierro y niveles disminuidos de una enzima protectora llamada GPX4, que normalmente neutraliza oxidantes derivados de lípidos. En conjunto, estos cambios apuntan a la ferroptosis, un tipo de muerte celular descrita recientemente en la que el hierro y los lípidos oxidados se combinan para matar células.
Demostrando que la muerte celular impulsada por hierro importa
Para comprobar si esta muerte celular relacionada con el hierro impulsa realmente la insuficiencia cardíaca y no solo la acompaña, los científicos manipularon los niveles de hierro y la enzima protectora clave GPX4. Dar a ratas viejas una dieta alta en hierro empeoró la función cardíaca y la cicatrización y suprimió aún más GPX4. En contraste, tratar a ratas ancianas con ferrostatina-1, un fármaco que bloquea específicamente la ferroptosis, mejoró el bombeo cardíaco, redujo la cicatrización y restauró proteínas más normales de manejo del hierro. En ratones, eliminar GPX4 específicamente en las células del músculo cardíaco agravó el daño y la disfunción relacionados con la edad, mientras que aumentar GPX4 mediante un vector de terapia génica preservó la función en otro modelo de envejecimiento. Estos experimentos sugieren con fuerza que la ferroptosis no solo está presente en los corazones envejecidos: contribuye activamente a su declive.
Un punto débil metabólico dentro de las células cardíacas
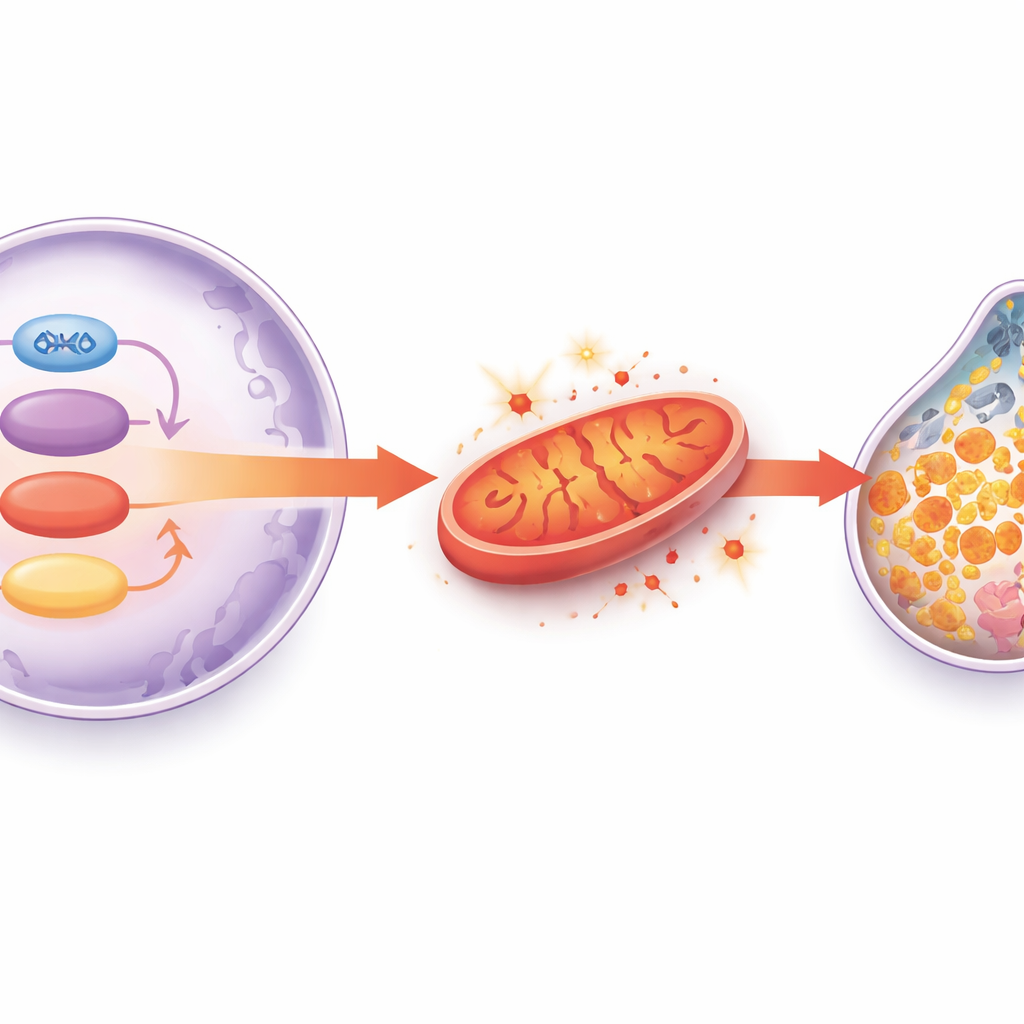
Buscando qué hace a las células cardíacas envejecidas más vulnerables a la ferroptosis, el equipo analizó miles de proteínas en corazones de rata y encontró una disminución notable de una enzima mitocondrial llamada HADHA, especialmente cuando los animales mayores se exponían a hierro adicional. HADHA ayuda a las células cardíacas a quemar grasas de forma eficiente y a mantener membranas mitocondriales sanas. Cuando los científicos redujeron HADHA específicamente en las células del corazón de ratones jóvenes, los animales desarrollaron más fibrosis y signos bioquímicos de ferroptosis, cambios que podían revertirse con un inhibidor de la ferroptosis. En cardiomiocitos aislados, disminuir HADHA alteró la función mitocondrial, aumentó las especies reactivas de oxígeno, agotó el glutatión antioxidante y suprimió aún más GPX4. Restaurar HADHA tuvo el efecto opuesto, rescatando la producción de energía y las defensas antioxidantes. Esto sitúa a HADHA como un salvaguarda metabólico crucial que impide que las células cardíacas caigan en la muerte impulsada por el hierro.
Un interruptor del envejecimiento: SIRT1 y sus socios a la baja
La siguiente pregunta fue por qué HADHA disminuye con la edad. Los autores se centraron en SIRT1, una proteína vinculada desde hace tiempo a la longevidad y a la protección frente a enfermedades relacionadas con la edad. En corazones envejecidos, los niveles de SIRT1 cayeron junto con los de HADHA. En experimentos celulares, inhibir SIRT1 redujo tanto HADHA como GPX4 y desplazó las proteínas de manejo del hierro hacia un perfil más peligroso. El equipo descubrió que SIRT1 interactúa con otra proteína, el factor de transcripción GATA4, que normalmente estimula la producción de HADHA. Cuando la actividad de SIRT1 disminuye, la capacidad de GATA4 para activar el gen HADHA se debilita, provocando la caída de HADHA y un aumento del estrés mitocondrial. De forma importante, activar SIRT1 con resveratrol, una pequeña molécula a menudo mencionada en el contexto del “envejecimiento saludable”, o sobreexpresando directamente SIRT1 en células cardíacas restauró GATA4 y HADHA, reforzó las defensas antioxidantes, redujo la ferroptosis y mejoró la función cardíaca en modelos animales de envejecimiento.
Qué significa esto para proteger el corazón envejecido
En conjunto, el estudio describe una cadena de eventos: al envejecer, la actividad de SIRT1 disminuye, GATA4 ya no mantiene los niveles de HADHA, las mitocondrias fallan y generan especies reactivas de oxígeno, el sistema antioxidante centrado en el glutatión y GPX4 colapsa, y la ferroptosis impulsada por el hierro acaba con las células del músculo cardíaco. Esta pérdida gradual de células y el aumento de la cicatrización debilitan finalmente la capacidad de bombeo del corazón. Aunque estos resultados proceden de modelos animales y celulares, sugieren que fármacos o estrategias de estilo de vida que preserven la actividad de SIRT1, apoyen HADHA y el metabolismo mitocondrial, o bloqueen directamente la ferroptosis podrían en el futuro ayudar a prevenir o tratar la insuficiencia cardíaca relacionada con la edad en humanos.
Cita: Duan, Y., Luo, Y., Han, X. et al. SIRT1 deficiency promotes age-related heart failure through enhancing ferroptosis via GATA4-HADHA-GPX4 axis. Cell Death Dis 17, 343 (2026). https://doi.org/10.1038/s41419-026-08634-z
Palabras clave: insuficiencia cardíaca por envejecimiento, ferroptosis, vía SIRT1, disfunción mitocondrial, muerte de cardiomiocitos