Clear Sky Science · sv
Koppla ihop inertiala, viskoelastiska och förstärkta sekundära flöden i en kompositmikrokanal: uppnå högprecisions 3D-central samfokusering av partiklar i flera storlekar
Få små resenärer att rada upp sig
Föreställ dig att du försöker fotografera tusentals snabbrörliga bilar på en motorväg, men några är motorcyklar och några är bussar. För att mäta varje fordon noggrant vill du att de passerar din kamera i en prydlig kö, inte utspridda över filerna. I biomedicinska laboratorier står forskare inför ett liknande problem med celler och mikroskopiska pärlor som rusar genom hårfina kanaler. Denna artikel beskriver en ny mikrofluidisk chip som varsamt tvingar partiklar och vita blodkroppar i olika storlekar in i samma smala tredimensionella bana, vilket förbättrar hur vi räknar, sorterar och analyserar dem för diagnostik och forskning. 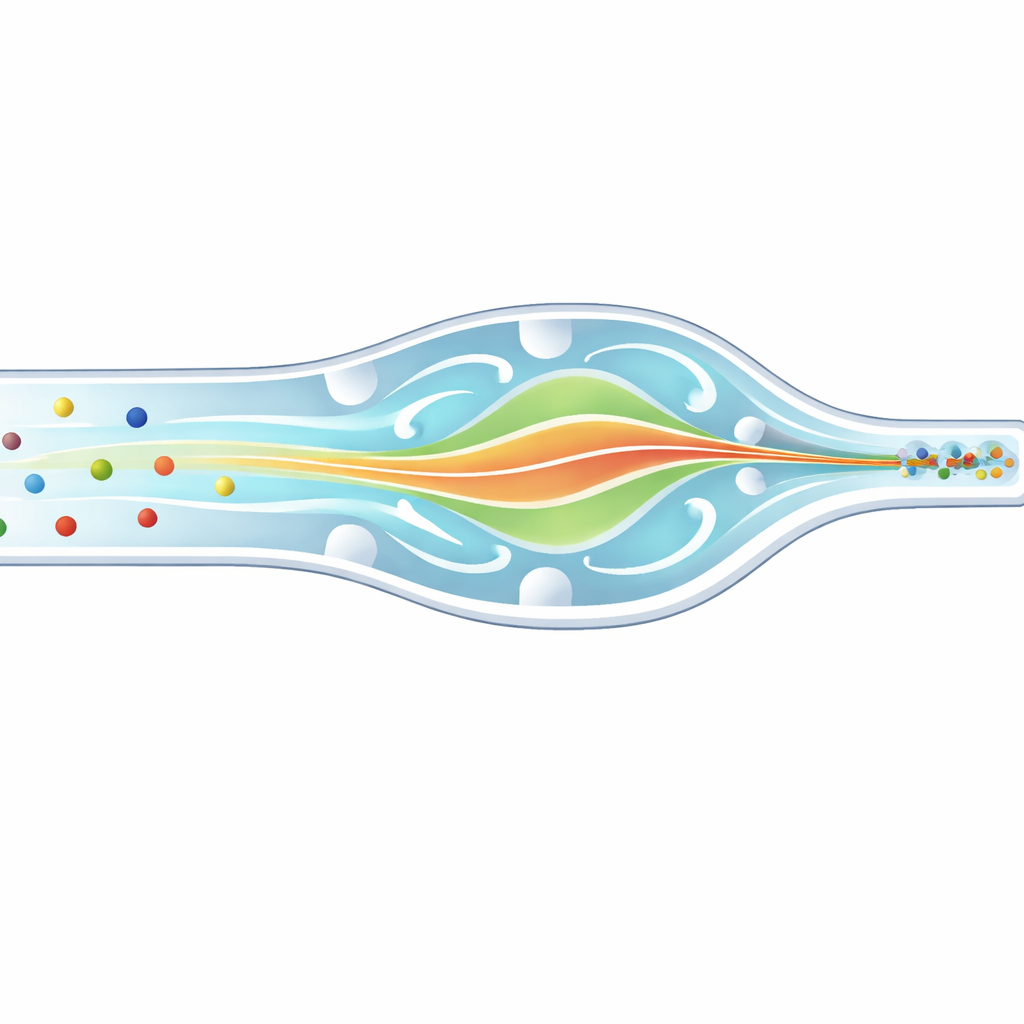
Varför det är viktigt att rada upp celler
Många avancerade medicinska instrument, såsom flödescytometrar och analysatorer för enskilda celler, fungerar genom att skicka celler genom små kanaler och undersöka dem med ljus eller elektriska signaler. Om vissa celler passerar nära väggen och andra glider genom mitten, utsätts de för olika belysning och krafter, vilket suddar ut mätningarna och döljer subtila skillnader mellan cellerna. Konventionella mikrofluidiska konstruktioner kan fokusera partiklar, men vanligtvis bara en storlek åt gången eller genom att pressa dem mot hörn snarare än mot det verkliga centret. Det betyder att blandningar av celler—som de olika vita blodkropparna i vårt blod—är svåra att mäta rent i ett enda genomlopp.
Kombinera tre varsamma påtryckningar i mikroskala
Forskarna angrep detta genom att bygga en noggrant utformad ”komposit”mikrokanal som utnyttjar tre vätskebeteenden samtidigt: tröghet (tendensen hos rörlig vätska och partiklar att fortsätta röra sig), elasticitet (extra fjädring tillsatt genom att lösa en biopolymer kallad hyaluronsyra) och virvlande sekundära strömmar skapade av böjar och hinder. I deras design kröker kanalen sig som en lugn spiral och bär en serie halvcirkelformade utskott längs både sidoväggen och i taket och golvet. Dessa inslag skapar kontrollerade virvlar som sveper partiklar bort från hörn, medan de elastiska krafterna i vätskan knuffar dem mot regioner med mildare flöde. Genom att finjustera kanalgeometrin och vätskans egenskaper skapar författarna ett synergistiskt läge de kallar INVEST, där de tre effekterna samarbetar i stället för att konkurrera. 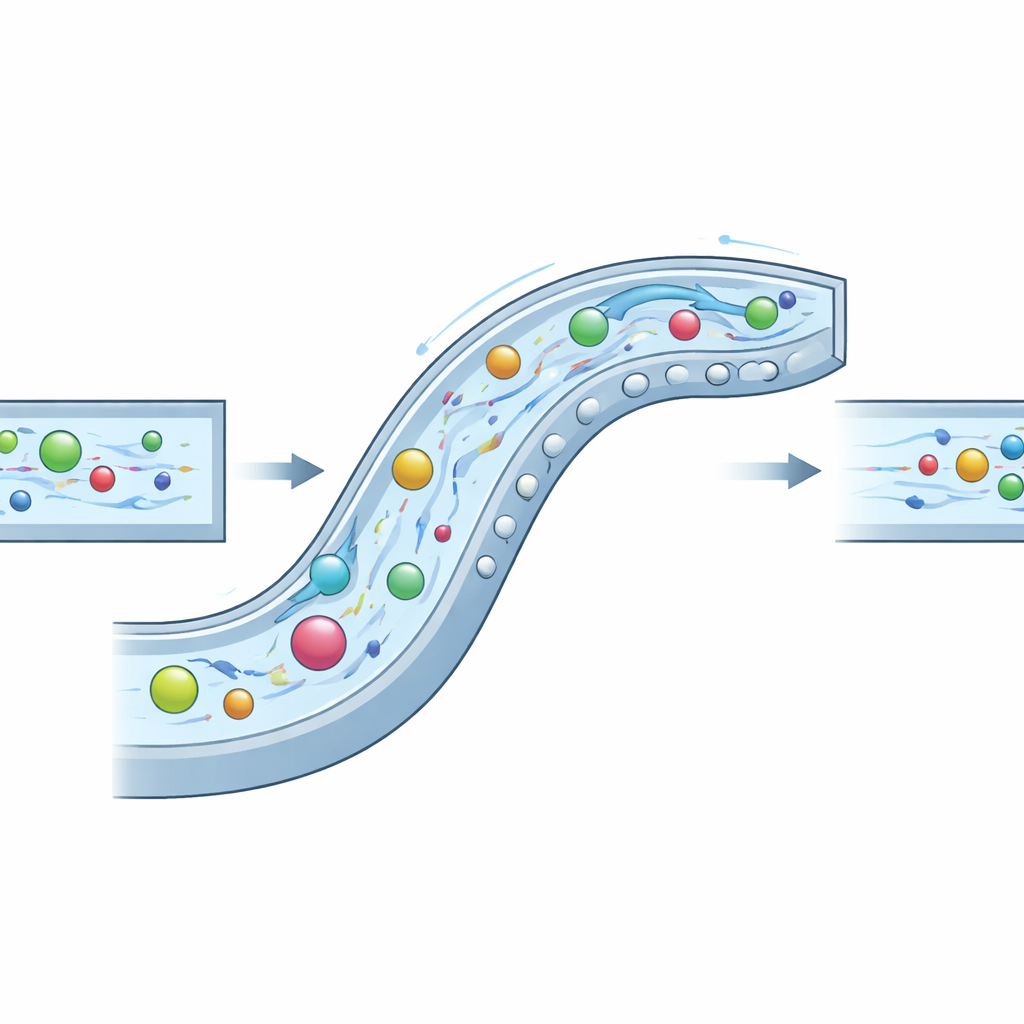
Testa den nya mikrokanalens motorväg
För att förstå hur detta system beter sig körde teamet först detaljerade datorsimuleringar av flödesmönstren, de interna virvlarna och hur kraftigt vätskan skjuvas nära väggarna. De införde ett nytt mått—”jämviktszonsbredden”—som uppskattar hur tätt partiklar kan begränsas i kanalens centrum. Den bästa designen, med sido- och vertikala hinder i fas, gav en mycket smal jämviktszon på cirka 16 mikrometer, vilket tyder på att partiklar skulle samlas i en tunn kärnström. Simuleringarna visade också att den tillförda elasticiteten knappt ändrade styrkan hos virvlarna men ökade återställande krafter mot centrum, vilket skärpte fokuseringen utan att destabilisera flödet.
Justera vätskan och hantera olika partikelstorlekar
Nästa steg byggde forskarna chippet och pumpade in fluorescerande plastpärlor suspenderade i saltlösningar som innehöll olika mängder hyaluronsyra. Genom att filma partiklarna ovanifrån och från sidan vid tusentals bildrutor per sekund mätte de både hur brett det fokuserade bandet var och vilken andel av partiklarna som faktiskt anslöt sig till det. Med rätt polymerkoncentration producerade kanalen ett enda klart streck endast något bredare än själva partiklarna över ett brett spektrum av flödeshastigheter. Pärlor med diametrar från 10 till 20 mikrometer—som normalt skulle hamna på olika positioner—fördes alla in i samma centrala bana med fokuseringseffektivitet över 95 % under optimala förhållanden. En mer komplex, förskjuten hinderlayout fungerade också, men inte lika väl eller lika robust.
Från plastpärlor till levande vita blodkroppar
Slutligen utmanade teamet enheten med vita blodkroppar, som varierar kraftigt i storlek och kan deformeras under starka krafter. Ändå riktade kanalen de flesta av dessa celler—ungefär i intervallet 7 till 20 mikrometer—till en enda smal ström vid måttliga flöden och uppnådde en toppfokuseringseffektivitet på strax över 96 %. Vid mycket höga hastigheter sträcktes och krympte cellerna, vilket gjorde dem mer sårbara för de virvlande strömmarna och fick dem att driva av från mitten, men inom praktiska arbetsfönster förblev fokuseringen stark. Detta visar att INVEST-strategin är kompatibel med känsliga biologiska prover, inte bara med styva testpärlor.
Vad detta innebär för framtida labbutrustning
I korthet visar detta arbete att genom att konstfullt forma en mikrokanal och välja en lätt elastisk vätska är det möjligt att driva en mångfald av mikroskopiska resenärer—styva partiklar eller mjuka celler—i samma tredimensionella fil. Det gör optiska och elektriska mätningar mer konsekventa, ökar genomströmningen i mikroskopiska analysatorer och minskar behovet av komplex mekanisk inpassning. Författarnas kompositkanal vänder ett ingenjörsproblem—att partiklar i olika storlek tar olika vägar—till en fördel genom att låta tröghet, elasticitet och virvlande flöde samverka. Detta tillvägagångssätt kan hjälpa till att krympa kraftfulla diagnostikinstrument till chipnivå och föra mer precisa blodanalyser och enkelscellsstudier närmare rutinmässig klinisk användning.
Citering: Zhao, T., Zeng, P., Ji, C. et al. Coupling inertial, viscoelastic, and enhanced secondary flow in a composite microchannel: achieving high-precision multi-sized particle 3D central co-focusing. Microsyst Nanoeng 12, 134 (2026). https://doi.org/10.1038/s41378-026-01254-9
Nyckelord: mikrofluidik, cellsamfokusering, inertialt flöde, viskoelastiska vätskor, flödescytometri