Clear Sky Science · it
Accoppiare inerzia, viscoelasticità e flusso secondario potenziato in un microcanale composito: ottenere un co‑focusing centrale 3D ad alta precisione per particelle di dimensioni multiple
Mettere in fila i piccoli viaggiatori
Immaginate di dover fotografare migliaia di auto veloci su un’autostrada, ma alcune sono motociclette e altre autobus. Per misurarle accuratamente vorreste che passassero davanti alla vostra macchina fotografica in un’unica fila ordinata, non sparse tra le corsie. Nei laboratori biomedici, gli scienziati affrontano un problema simile con cellule e sfere microscopiche che corrono attraverso canali sottilissimi. Questo articolo descrive un nuovo chip microfluidico che induce delicatamente particelle e globuli bianchi di dimensioni diverse a convergere sullo stesso stretto percorso tridimensionale, migliorando il conteggio, l’ordinamento e l’analisi per diagnostica e ricerca. 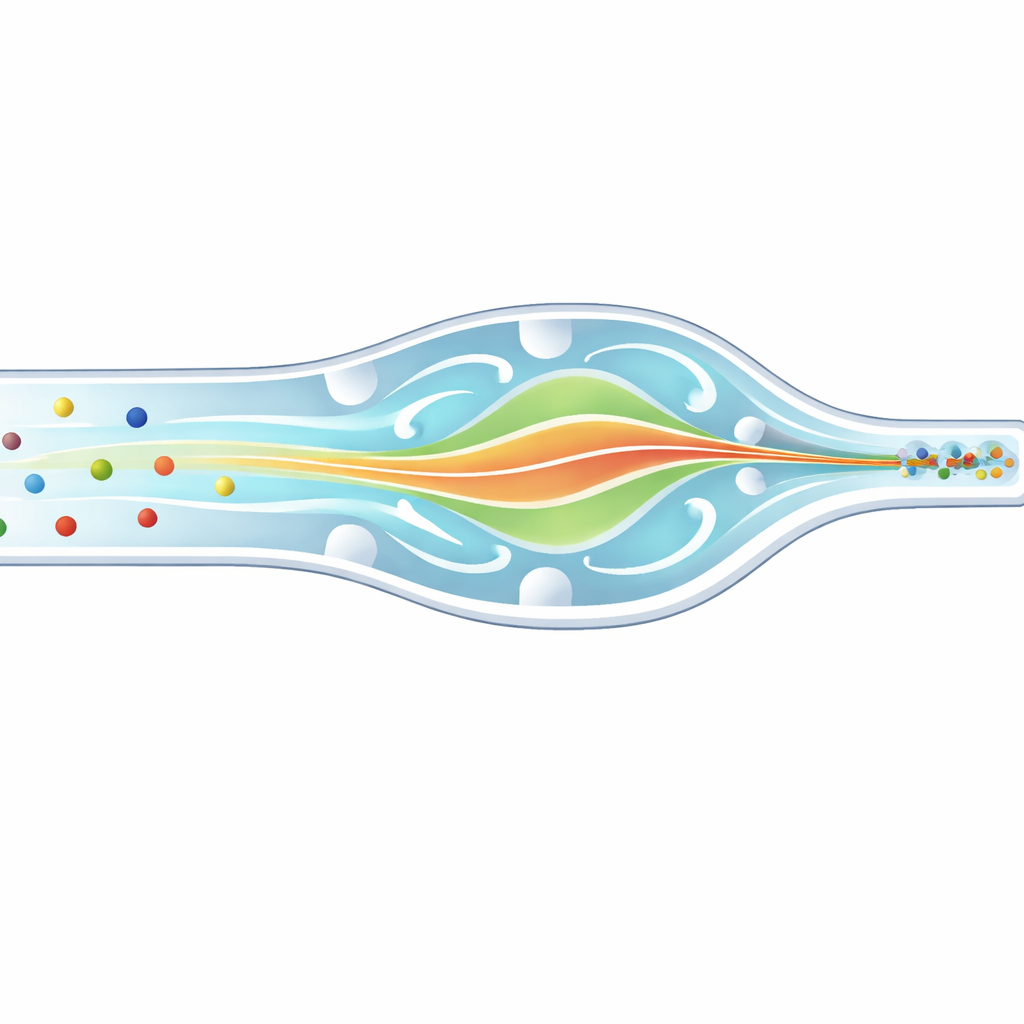
Perché allineare le cellule è davvero importante
Molti strumenti medici all’avanguardia, come i citometri a flusso e gli analizzatori a singola cellula, funzionano facendo scorrere le cellule attraverso canali minuscoli e interrogandole con luce o segnali elettrici. Se alcune cellule passano vicino alla parete e altre scorrono al centro, sperimentano illuminazione e forze diverse, il che sfuma le misure e nasconde differenze sottili tra le cellule. I progetti microfluidici convenzionali possono focalizzare le particelle, ma di solito solo di una dimensione per volta, oppure le spingono verso gli angoli anziché verso il vero centro. Ciò significa che miscele di cellule—come i diversi tipi di globuli bianchi presenti nel sangue—sono difficili da analizzare in modo pulito in un’unica passata.
Combinare tre spinte delicate su scala microscopica
I ricercatori hanno affrontato il problema costruendo un microcanale "composito" attentamente scolpito che sfrutta contemporaneamente tre comportamenti del fluido: l’inerzia (la tendenza del fluido e delle particelle in movimento a proseguire), l’elasticità (una rigidezza aggiunta sciogliendo un biopolimero chiamato acido ialuronico) e correnti secondarie vorticoshe generate da curvature e ostacoli. Nel loro progetto il canale curva come una spirale lenta e presenta una serie di protuberanze semicircolari sia lungo la parete laterale sia su soffitto e pavimento. Queste caratteristiche creano vortici controllati che allontanano le particelle dagli angoli, mentre le forze elastiche nel fluido le spingono verso regioni di flusso più dolce. Sintonizzando la geometria del canale e le proprietà del fluido, gli autori ottengono un regime sinergico che chiamano INVEST, in cui i tre effetti cooperano anziché competere. 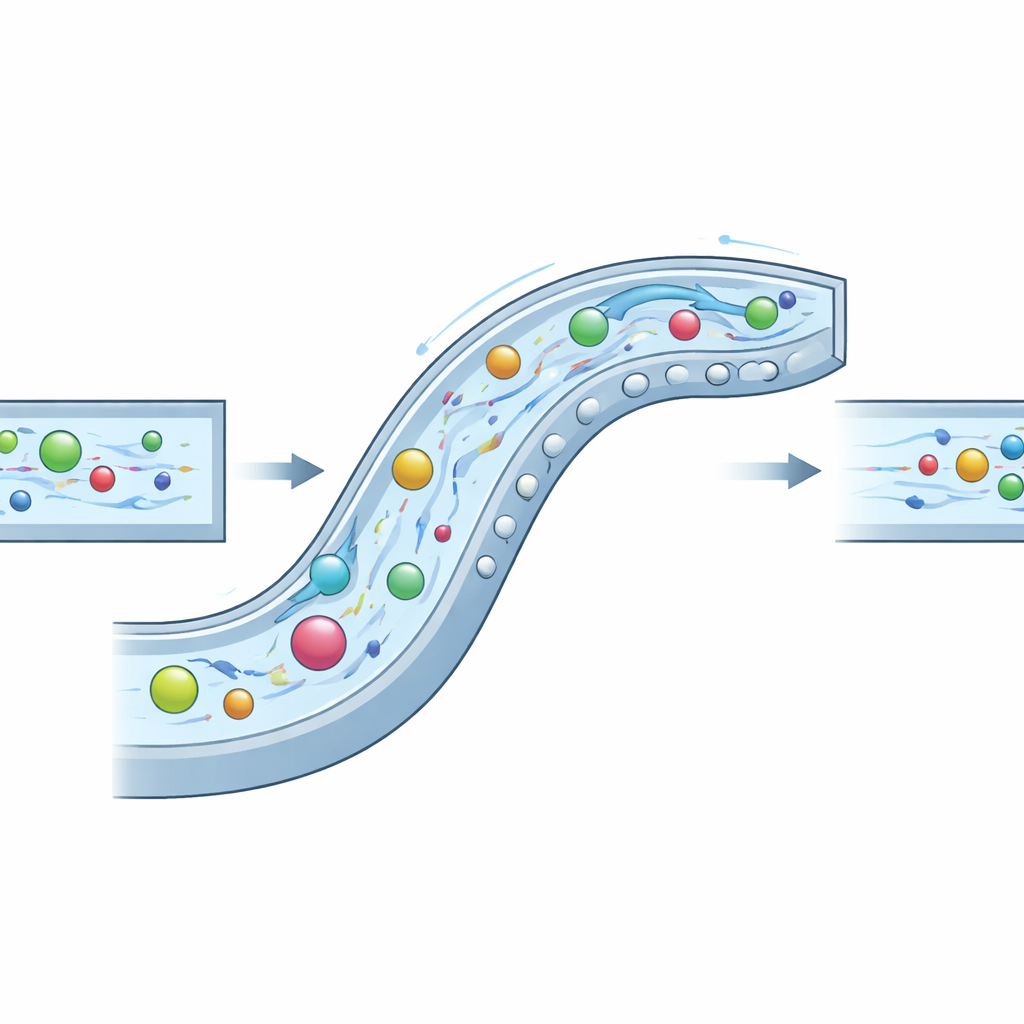
Mettere alla prova la nuova autostrada microcanale
Per capire come si comporta il sistema, il team ha prima eseguito dettagliate simulazioni al computer dei modelli di flusso, dei vortici interni e di quanto il fluido si taglia vicino alle pareti. Hanno introdotto un nuovo metro di misura—la "larghezza della zona di equilibrio"—che stima quanto strettamente le particelle possano essere confinate al centro del canale. Il miglior progetto, con ostacoli laterali e verticali allineati in fase, ha prodotto una zona di equilibrio molto stretta di circa 16 micrometri, suggerendo che le particelle si raccoglierebbero in un sottile flusso centrale. Le simulazioni hanno mostrato anche che l’elasticità aggiunta cambiava di poco la forza dei vortici ma incrementava le forze di richiamo verso il centro, affilando il focusing senza destabilizzare il flusso.
Regolare il fluido e gestire diverse dimensioni di particelle
Successivamente i ricercatori hanno costruito il chip e fatto scorrere sfere plastiche fluorescenti sospese in soluzioni saline contenenti diverse concentrazioni di acido ialuronico. Filmando le particelle dall’alto e di lato a migliaia di fotogrammi al secondo, hanno misurato sia la larghezza della banda focalizzata sia la frazione di particelle effettivamente catturate in essa. Con la giusta concentrazione di polimero, il canale ha prodotto una singola striscia luminosa solo leggermente più larga delle particelle stesse su un ampio intervallo di velocità di flusso. Sfere da 10 a 20 micrometri di diametro—che normalmente si posizionerebbero in punti diversi—sono state tutte convogliate sullo stesso percorso centrale con efficienze di focalizzazione superiori al 95% nelle condizioni ottimali. Un layout di ostacoli più complesso e sfalsato funzionava, ma non altrettanto bene o in modo altrettanto robusto.
Dalle sfere di plastica ai globuli bianchi vivi
Infine, il team ha messo alla prova il dispositivo con globuli bianchi, che variano molto in dimensione e possono deformarsi sotto forze elevate. Nonostante ciò, il canale ha allineato la maggior parte di queste cellule—che variano approssimativamente da 7 a 20 micrometri—in un unico stretto flusso a velocità moderate, raggiungendo un’efficienza di focalizzazione di picco poco superiore al 96%. A velocità molto elevate le cellule si allungavano e si comprimavano, rendendole più sensibili alle correnti vorticoshe e facendole deviare dalla linea centrale, ma entro finestre operative pratiche il focusing è rimasto robusto. Questo dimostra che la strategia INVEST è compatibile con campioni biologici delicati, non solo con sfere rigide di prova.
Cosa significa per gli strumenti di laboratorio futuri
In sostanza, questo lavoro dimostra che modellando con cura un microcanale e scegliendo un fluido leggermente elastico è possibile convogliare una folla eterogenea di viaggiatori microscopici—particelle rigide o cellule morbide—sullo stesso corridoio tridimensionale. Ciò rende le misure ottiche ed elettriche più coerenti, aumenta la capacità degli analizzatori su scala micro e riduce la necessità di complessi sistemi di allineamento. Il canale composito degli autori trasforma un problema ingegneristico—particelle di dimensioni diverse che prendono percorsi diversi—in un vantaggio facendo cooperare inerzia, elasticità e flusso vorticoso. Questo approccio potrebbe aiutare a miniaturizzare potenti strumenti diagnostici su chip, avvicinando analisi del sangue più precise e studi a singola cellula a un uso clinico di routine.
Citazione: Zhao, T., Zeng, P., Ji, C. et al. Coupling inertial, viscoelastic, and enhanced secondary flow in a composite microchannel: achieving high-precision multi-sized particle 3D central co-focusing. Microsyst Nanoeng 12, 134 (2026). https://doi.org/10.1038/s41378-026-01254-9
Parole chiave: microfluidica, allineamento cellulare, flusso inerziale, fluidi viscoelastici, citometria a flusso