Clear Sky Science · fr
Coupler l’inertie, la viscoélasticité et l’écoulement secondaire amplifié dans un microcanal composite : obtenir un co‑focalisation centrale 3D à haute précision pour particules de tailles multiples
Rassembler les petits voyageurs en file
Imaginez devoir photographier des milliers de voitures rapides sur une autoroute, dont certaines sont des motos et d’autres des bus. Pour mesurer chacune avec précision, vous voudriez qu’elles passent devant votre caméra en un seul rang, et non dispersées sur plusieurs voies. Dans les laboratoires biomédicaux, les chercheurs affrontent un problème similaire avec des cellules et des billes microscopiques s’écoulant dans des canaux d’une finesse extrême. Cet article décrit une nouvelle puce microfluidique qui contraint en douceur des particules et des globules blancs de tailles différentes à emprunter le même trajet étroit en trois dimensions, améliorant ainsi le comptage, le tri et l’analyse pour le diagnostic et la recherche. 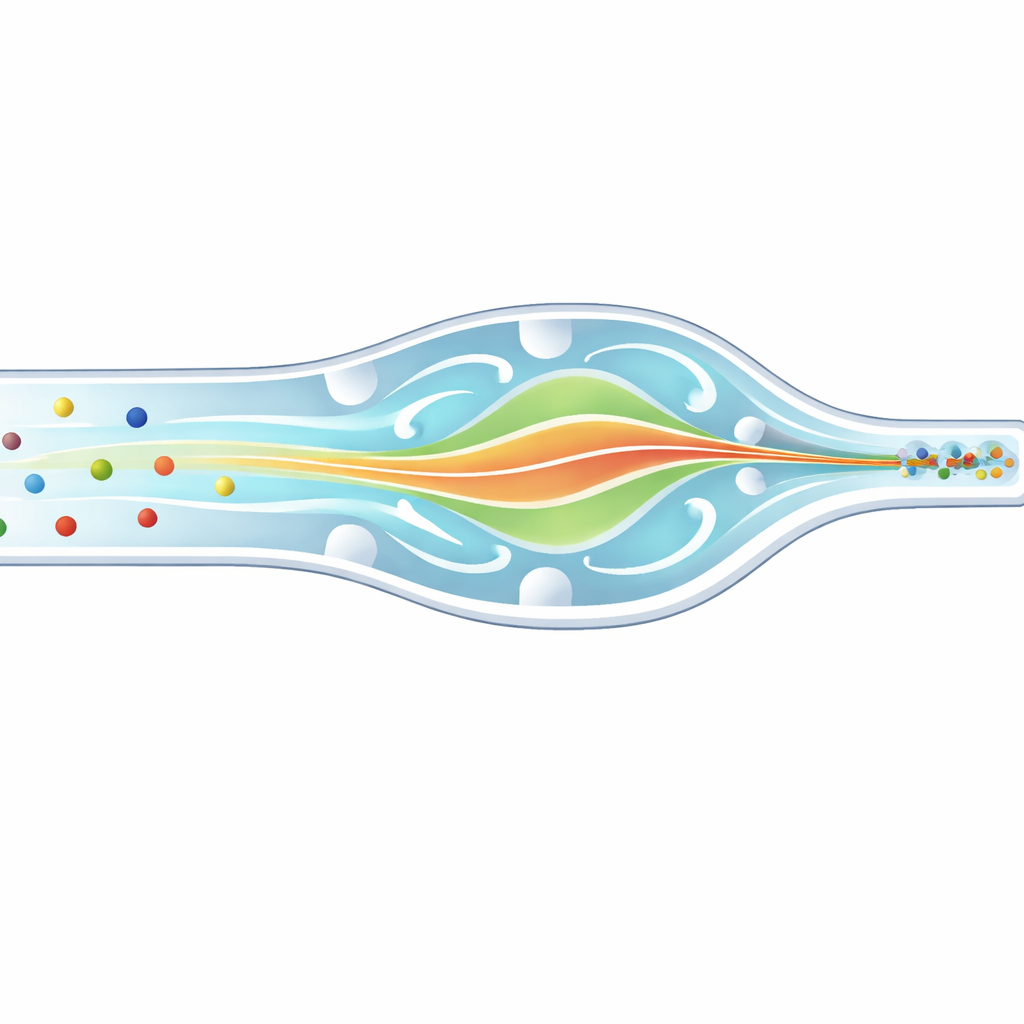
Pourquoi aligner les cellules est crucial
De nombreux outils médicaux de pointe, comme les cytomètres en flux et les analyseurs unicellulaires, fonctionnent en faisant passer des cellules dans de petits canaux et en les sondant par la lumière ou des signaux électriques. Si certaines cellules passent près des parois et d’autres au centre, elles subissent un éclairage et des forces différents, ce qui brouille les mesures et masque des différences subtiles entre cellules. Les conceptions microfluidiques classiques peuvent focaliser des particules, mais généralement d’une seule taille à la fois, ou elles les poussent vers les coins plutôt que vers le véritable centre. Cela rend les mélanges cellulaires — comme la diversité des globules blancs dans le sang — difficiles à mesurer proprement en une seule passe.
Combiner trois poussées douces à l’échelle microscopique
Les auteurs ont résolu ce problème en concevant un microcanal « composite » finement sculpté qui exploite simultanément trois comportements fluides : l’inertie (la tendance des fluides et des particules en mouvement à conserver leur trajectoire), l’élasticité (une élasticité additionnelle apportée par la dissolution d’un biopolymère, l’acide hyaluronique) et des courants secondaires tourbillonnants créés par des virages et des obstacles. Dans leur conception, le canal suit une courbe semblable à une spirale douce et comporte une série de bosses semi‑circulaires le long de la paroi latérale ainsi que au plafond et au sol. Ces éléments génèrent des vortex contrôlés qui balayent les particules hors des coins, tandis que les forces élastiques du fluide les poussent vers des régions d’écoulement plus doux. En ajustant la géométrie du canal et les propriétés du fluide, les auteurs obtiennent un régime synergique qu’ils nomment INVEST, dans lequel les trois effets coopèrent plutôt que de se concurrencer. 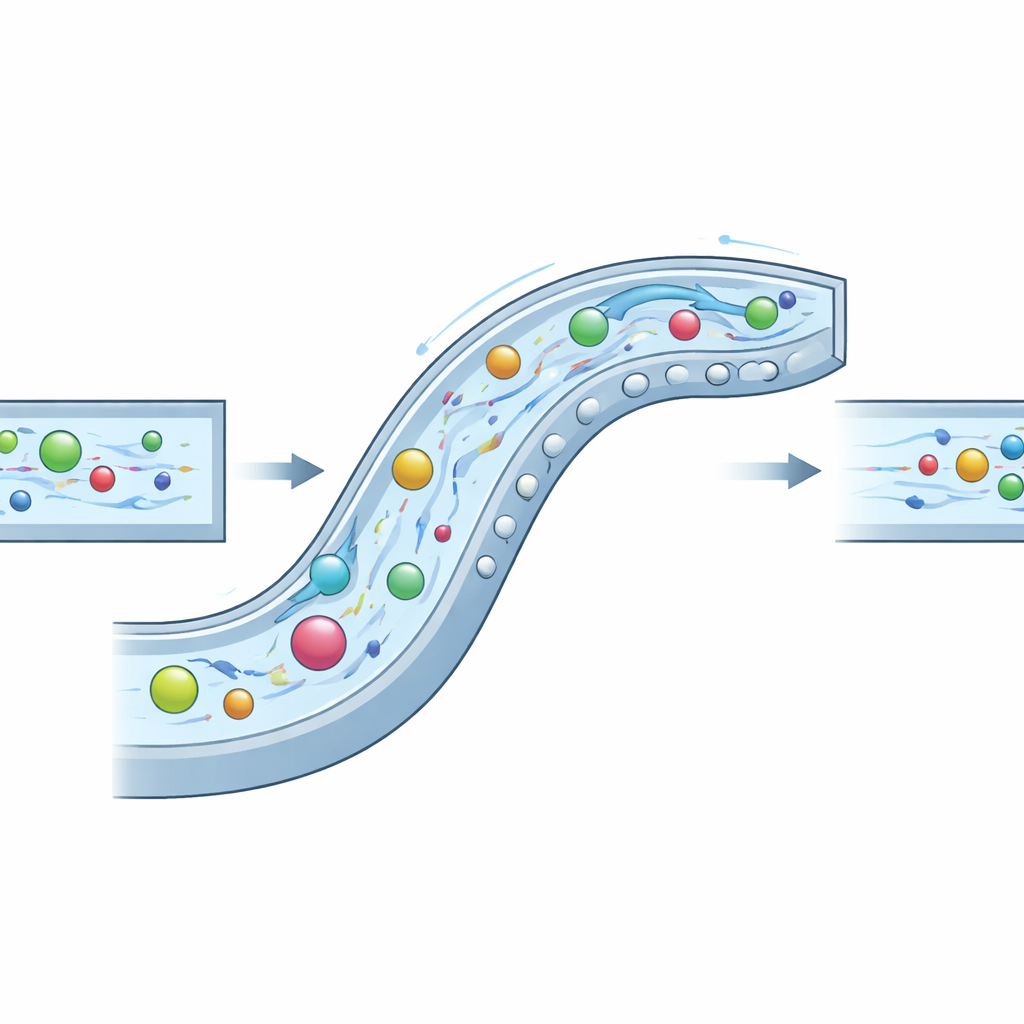
Tester cette nouvelle « autoroute » microfluidique
Pour comprendre le comportement du système, l’équipe a d’abord réalisé des simulations informatiques détaillées des motifs d’écoulement, des vortex internes et des cisaillements proches des parois. Ils ont introduit une nouvelle référence — la « largeur de la zone d’équilibre » — qui estime à quel point les particules peuvent être confinées au centre du canal. La meilleure configuration, avec obstacles latéraux et verticaux alignés en phase, a produit une zone d’équilibre très étroite d’environ 16 micromètres, suggérant que les particules se rassembleraient en un flux central mince. Les simulations ont également montré que l’ajout d’élasticité modifiait peu l’intensité des tourbillons mais augmentait les forces de rappel vers le centre, affinant la focalisation sans déstabiliser l’écoulement.
Ajuster le fluide et gérer différentes tailles de particules
Ensuite, les chercheurs ont fabriqué la puce et ont injecté des billes plastiques fluorescentes suspendues dans des solutions salines contenant différentes concentrations d’acide hyaluronique. En filmant les particules par le dessus et par la tranche à des milliers d’images par seconde, ils ont mesuré à la fois la largeur de la bande focalisée et la fraction de particules qui s’y joignaient réellement. Avec la concentration de polymère appropriée, le canal a produit une unique traînée lumineuse à peine plus large que les particules sur une large plage de débits. Des billes de 10 à 20 micromètres de diamètre — qui se placeraient normalement à des positions différentes — ont toutes été amenées dans la même voie centrale avec des efficacités de focalisation supérieures à 95 % dans des conditions optimales. Une disposition d’obstacles plus complexe et décalée fonctionnait aussi, mais moins bien et avec moins de robustesse.
Des billes plastiques aux globules blancs vivants
Enfin, l’équipe a mis le dispositif à l’épreuve avec des globules blancs, qui varient largement en taille et peuvent se déformer sous de fortes forces. Pourtant, le canal a aligné la plupart de ces cellules — d’environ 7 à 20 micromètres — dans un flux étroit unique à des débits modérés, atteignant une efficacité de focalisation maximale légèrement supérieure à 96 %. À des vitesses très élevées, les cellules s’étiraient et se contractaient, les rendant plus sensibles aux courants tourbillonnants et les faisant dériver hors de la ligne centrale ; mais dans les plages d’utilisation pratiques, la focalisation restait robuste. Cela montre que la stratégie INVEST est compatible avec des échantillons biologiques délicats, pas seulement avec des billes rigides de test.
Ce que cela implique pour les outils de laboratoire à venir
En substance, ce travail montre qu’en façonnant habilement un microcanal et en choisissant un fluide légèrement élastique, il est possible de conduire une foule diverse de voyageurs microscopiques — particules rigides ou cellules souples — dans la même voie tridimensionnelle. Cela rend les mesures optiques et électriques plus cohérentes, augmente le débit des analyseurs à l’échelle microscopique et réduit le besoin de matériel d’alignement complexe. Le canal composite des auteurs transforme un casse‑tête d’ingénierie — des particules de tailles différentes suivant des trajectoires différentes — en une force en faisant coopérer l’inertie, l’élasticité et l’écoulement tourbillonnant. Cette approche pourrait contribuer à miniaturiser des instruments diagnostiques puissants sur puce, rapprochant une analyse sanguine plus précise et des études unicellulaires d’une utilisation clinique courante.
Citation: Zhao, T., Zeng, P., Ji, C. et al. Coupling inertial, viscoelastic, and enhanced secondary flow in a composite microchannel: achieving high-precision multi-sized particle 3D central co-focusing. Microsyst Nanoeng 12, 134 (2026). https://doi.org/10.1038/s41378-026-01254-9
Mots-clés: microfluidique, focalisation cellulaire, écoulement inertiel, fluides viscoélastiques, cytométrie en flux