Clear Sky Science · nl
Koppeling van traagheid, visco-elasticiteit en versterkte secundaire stroming in een samengestelde microkanaal: het bereiken van hoogprecisie driedimensionale centrale co-focusering van meerdere deeltjesgroottes
Kleine reizigers op één lijn brengen
Stel je voor dat je duizenden snel rijdende auto’s op een snelweg wilt fotograferen, terwijl sommigen motoren en anderen bussen zijn. Om elke voertuig nauwkeurig te meten, wil je dat ze keurig in enkel file langs je camera rijden, niet verspreid over de rijstroken. In biomedische laboratoria staan wetenschappers voor een vergelijkbaar probleem met cellen en microscopische bolletjes die door haarfijne kanaaltjes razen. Dit artikel beschrijft een nieuwe microfluidische chip die deeltjes en witte bloedcellen van verschillende groottes voorzichtig dwingt om via hetzelfde smalle driedimensionale pad te reizen, waardoor tellen, scheiden en analyseren voor diagnostiek en onderzoek verbetert. 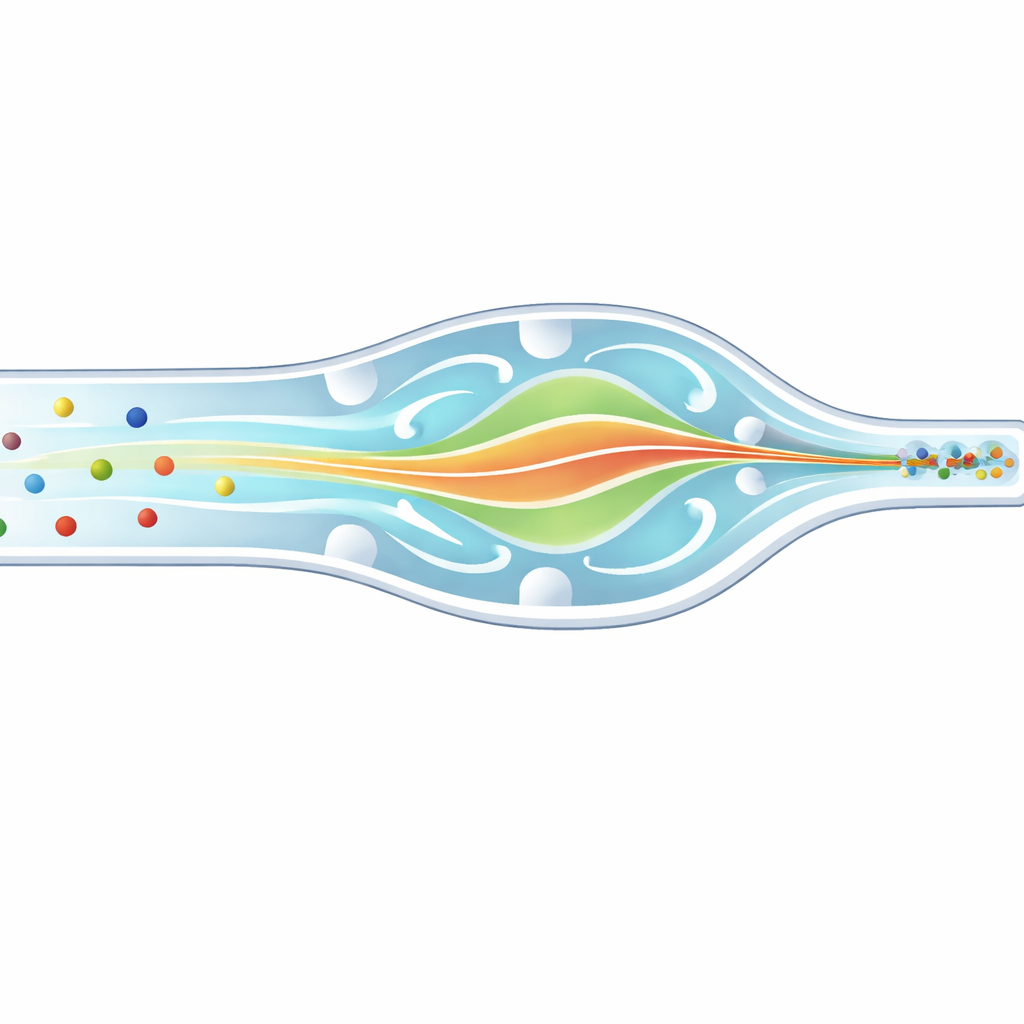
Waarom het op een rij zetten van cellen écht telt
Veel geavanceerde medische instrumenten, zoals flowcytometers en single‑cell analysers, werken door cellen door tiny kanaaltjes te sturen en ze met licht of elektrische signalen te onderzoeken. Als sommige cellen dicht bij de wand passeren en andere door het centrum glijden, ondervinden ze verschillende belichting en krachten, wat de metingen vervaagt en subtiele verschillen tussen cellen verbergt. Conventionele microfluidische ontwerpen kunnen deeltjes focussen, maar meestal slechts van één grootte tegelijk, of ze duwen ze naar hoeken in plaats van naar het echte centrum. Dat maakt het moeilijk om mengsels van cellen — zoals de diverse witte bloedcellen in ons bloed — in één doorgang zuiver te meten.
Drie zachte stuwende mechanismen combineren op microschaal
De onderzoekers gingen dit probleem te lijf door een zorgvuldig gevormd “samengesteld” microkanaal te bouwen dat drie vloeigedragingen tegelijk benut: traagheid (de neiging van bewegende vloeistof en deeltjes om door te blijven bewegen), elasticiteit (extra veerkracht door het oplossen van een biopolymeer genaamd hyaluronzuur) en zwenkende secundaire stromingen die ontstaan door bochten en obstakels. In hun ontwerp kronkelt het kanaal als een trage spiraal en draagt een reeks halfronde uitsteeksels zowel langs de zijwand als op plafond en vloer. Deze kenmerken creëren gecontroleerde wervels die deeltjes van de hoeken wegvegen, terwijl de elastische krachten in de vloeistof ze naar gebieden met zachte stroming duwen. Door de kanaalgeometrie en de eigenschappen van de vloeistof af te stemmen, creëren de auteurs een synergistische regime die zij INVEST noemen, waarin die drie effecten samenwerken in plaats van concurreren. 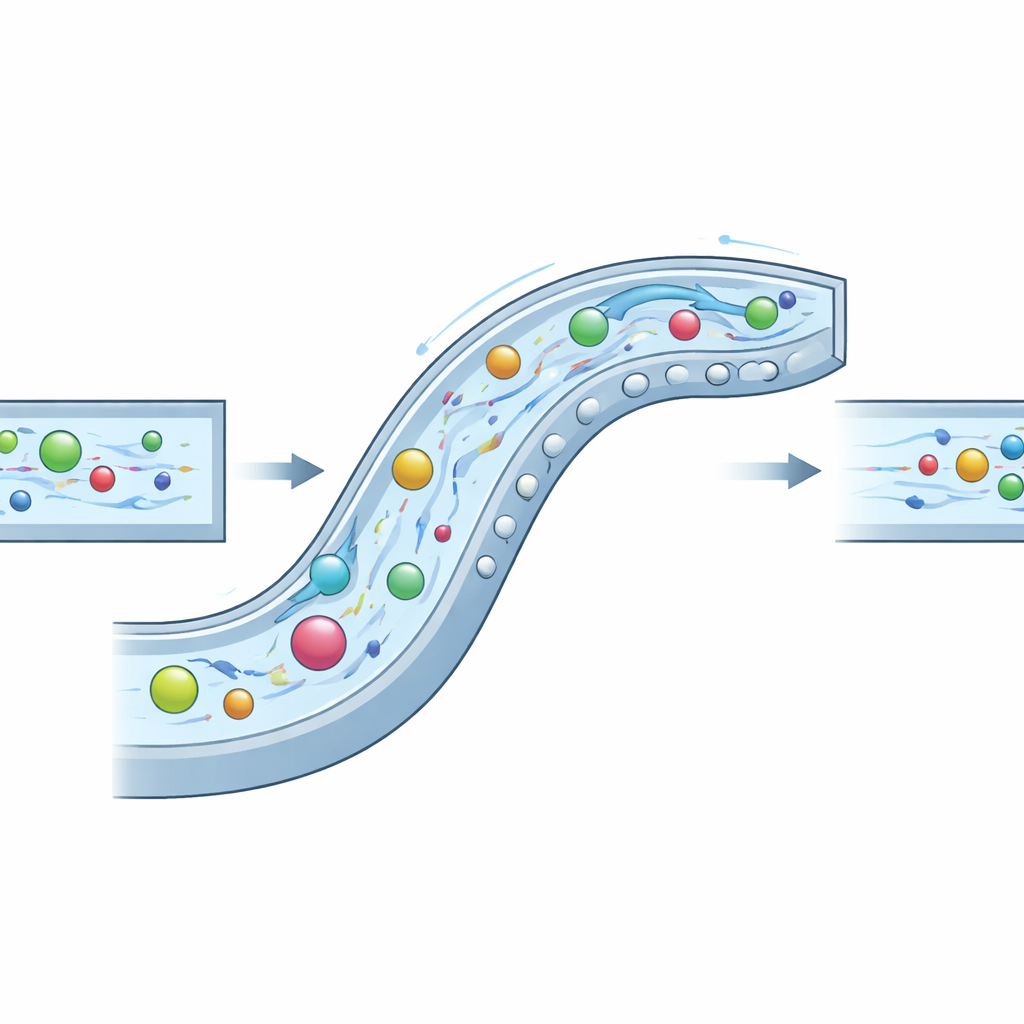
Testen van de nieuwe microkanaal-snelweg
Om te begrijpen hoe dit systeem zich gedraagt, voerde het team eerst gedetailleerde computersimulaties uit van de stromingspatronen, de interne werveling en hoe scherp de vloeistof langs de wanden schuurt. Ze introduceerden een nieuwe maatstaf — de “breedte van de evenwichtszone” — die inschat hoe strak deeltjes in het centrum van het kanaal kunnen worden ingesloten. Het beste ontwerp, met zij- en verticale obstakels in fase uitgelijnd, produceerde een zeer smalle evenwichtszone van ongeveer 16 micrometer, wat suggereert dat deeltjes zich zouden verzamelen in een dunne kernstroom. Simulaties toonden ook aan dat de toegevoegde elasticiteit de sterkte van de wervels nauwelijks veranderde maar wel de herstellende krachten naar het centrum vergrootte, waardoor de focus scherper werd zonder de stroming te destabiliseren.
De vloeistof afstemmen en omgaan met verschillende deeltjesgroottes
Vervolgens bouwden de onderzoekers de chip en pompten fluorescerende plastic bolletjes in, gesuspendeerd in zoutoplossingen met verschillende hoeveelheden hyaluronzuur. Door de deeltjes van boven en van opzij te filmen met duizenden frames per seconde, maten ze zowel hoe breed de gefocuste band was als welk aandeel deeltjes zich er daadwerkelijk bij voegde. Met de juiste polymeerconcentratie produceerde het kanaal één heldere streep die slechts iets breder was dan deeltjes zelf over een breed bereik aan debieten. Bolletjes van 10 tot 20 micrometer in diameter — die normaal op verschillende posities zouden neerslaan — werden allemaal in hetzelfde centrale pad gebracht met focus-efficiënties boven 95% onder optimale omstandigheden. Een complexere, verspringende obstakelindeling werkte ook, maar niet zo goed of zo robuust.
Van plastic bolletjes naar levende witte bloedcellen
Tenslotte daagde het team het apparaat uit met witte bloedcellen, die sterk variëren in grootte en onder sterke krachten vervormen. Desondanks zette het kanaal het merendeel van deze cellen — grofweg van 7 tot 20 micrometer — op een enkele smalle stroom bij matige debieten, met een piekfocus-efficiëntie van net boven 96%. Bij zeer hoge snelheden rekten en krimpten cellen, waardoor ze gevoeliger werden voor de wervelende stromingen en van de centrale lijn wegdreven, maar binnen praktische bedrijfsvensters bleef de focusering sterk. Dit toont aan dat de INVEST‑strategie compatibel is met kwetsbare biologische monsters, niet alleen met stijve testbolletjes.
Wat dit betekent voor toekomstige labtools
In wezen laat dit werk zien dat je door het kunstzinnig vormgeven van een microkanaal en het kiezen van een licht elastische vloeistof een diverse menigte microscopische reizigers — stijve deeltjes of zachte cellen — in hetzelfde driedimensionale rijvak kunt samenbrengen. Dat maakt optische en elektrische metingen consistenter, verhoogt de doorvoer van microschaal‑analysers en vermindert de noodzaak voor complexe uitlijningshardware. Het samengestelde kanaal van de auteurs verandert een engineeringprobleem — deeltjes van verschillende grootte die verschillende paden volgen — in een voordeel door traagheid, elasticiteit en wervelende stroming samen te laten werken. Deze benadering kan helpen krachtige diagnostische instrumenten op chips te verkleinen, waardoor nauwkeurigere bloedanalyses en single‑cell studies dichter bij routinematige klinische toepassing komen.
Bronvermelding: Zhao, T., Zeng, P., Ji, C. et al. Coupling inertial, viscoelastic, and enhanced secondary flow in a composite microchannel: achieving high-precision multi-sized particle 3D central co-focusing. Microsyst Nanoeng 12, 134 (2026). https://doi.org/10.1038/s41378-026-01254-9
Trefwoorden: microfluidica, celfocusering, inertiële stroming, visco-elastische vloeistoffen, flowcytometrie