Clear Sky Science · de
Kopplung von Trägheit, viskoelastischen Effekten und verstärkter Sekundärströmung in einem Verbund-Mikrokanal: Hochpräzises 3D-Zentralko-Fokussieren von Partikeln verschiedener Größen
Kleine Reisende in eine Reihe bringen
Stellen Sie sich vor, Sie müssten Tausende sich schnell bewegender Autos auf einer Autobahn fotografieren, wobei einige Motorräder und andere Busse sind. Um jedes Fahrzeug genau zu messen, möchten Sie, dass sie in einer sauberen Reihe an Ihrer Kamera vorbeifahren, nicht über die Fahrspuren verteilt. In biomedizinischen Laboren stehen Wissenschaftler vor einem ähnlichen Problem: Zellen und mikroskopische Kügelchen rasen durch haarfeine Kanäle. Diese Arbeit beschreibt einen neuen mikrofluidischen Chip, der Partikel und weiße Blutkörperchen unterschiedlicher Größe sanft in denselben schmalen dreidimensionalen Pfad zwingt und so das Zählen, Sortieren und Analysieren für Diagnostik und Forschung verbessert. 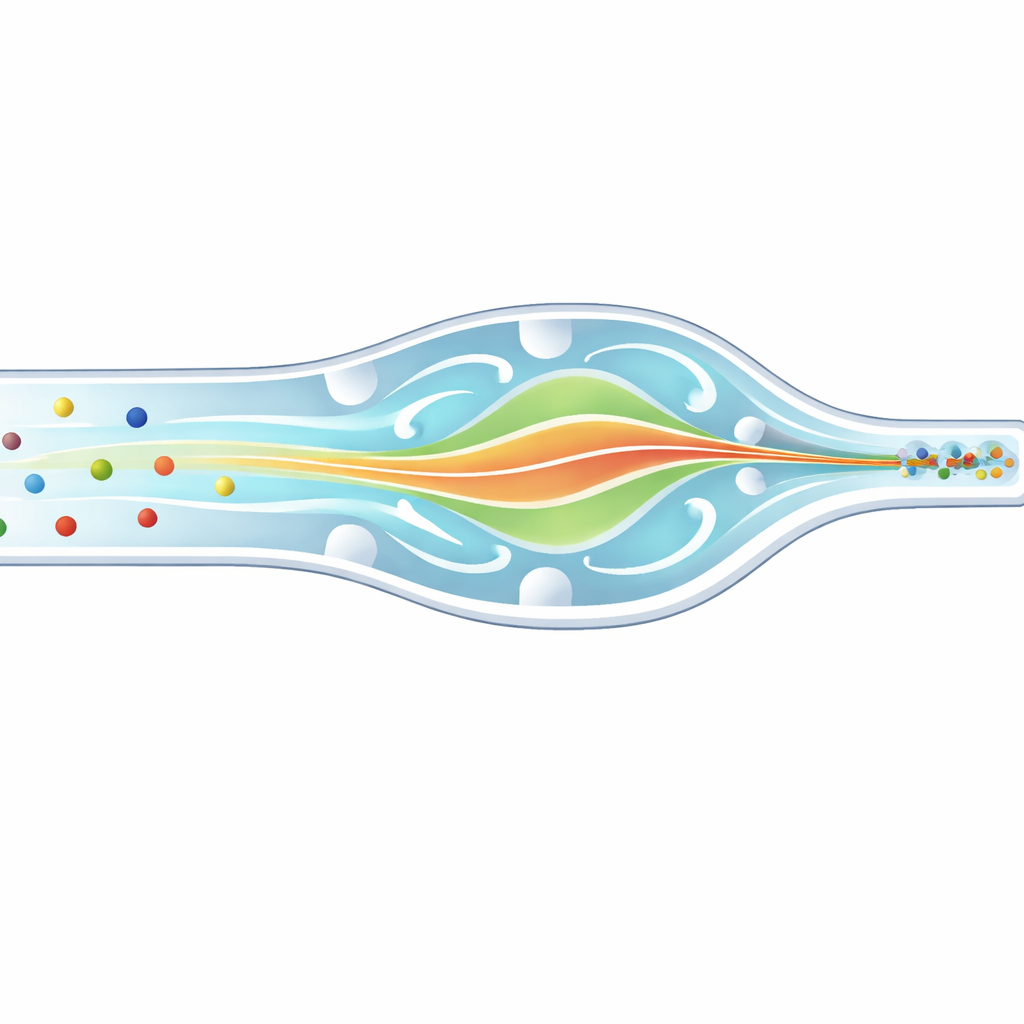
Warum das Reihenbilden von Zellen wirklich wichtig ist
Viele hochentwickelte medizinische Geräte, wie Durchflusszytometer und Einzelzellanalysatoren, arbeiten, indem sie Zellen durch winzige Kanäle schicken und sie mit Licht oder elektrischen Signalen auslesen. Wenn einige Zellen in Wandnähe und andere in der Kanalmitte vorbeiziehen, erfahren sie unterschiedliche Beleuchtung und Kräfte, was die Messungen verwischt und feine Unterschiede zwischen Zellen überdeckt. Konventionelle mikrofluidische Designs können Partikel fokussieren, meist jedoch nur einer Größe gleichzeitig oder sie drängen sie in Ecken statt in den tatsächlichen Kanalzentrum. Das macht es schwierig, Mischungen von Zellen – etwa die vielfältigen weißen Blutkörperchen im Blut – in einem Durchgang sauber zu messen.
Drei sanfte Kräfte im Mikromaßstab kombinieren
Die Forscher begegneten diesem Problem, indem sie einen sorgfältig gestalteten „Verbund“-Mikrokanal bauten, der drei Strömungsverhalten gleichzeitig nutzt: Trägheit (die Tendenz bewegter Flüssigkeit und Partikel, in Bewegung zu bleiben), Elastizität (zusätzliche Federwirkung durch Auflösen eines Biopolymers, Hyaluronsäure) und Wirbel sekundärer Strömungen, die durch Krümmungen und Hindernisse erzeugt werden. In ihrem Design krümmt sich der Kanal wie eine langsame Spirale und trägt eine Reihe von halbrunden Erhebungen sowohl an der Seitenwand als auch an Decke und Boden. Diese Merkmale erzeugen kontrollierte Wirbel, die Partikel aus Ecken fegen, während die elastischen Kräfte in der Flüssigkeit sie in Regionen sanfter Strömung lenken. Durch Abstimmung der Kanalgeometrie und der Eigenschaften der Flüssigkeit schaffen die Autoren ein synergistisches Regime, das sie INVEST nennen, in dem die drei Effekte kooperieren statt konkurrieren. 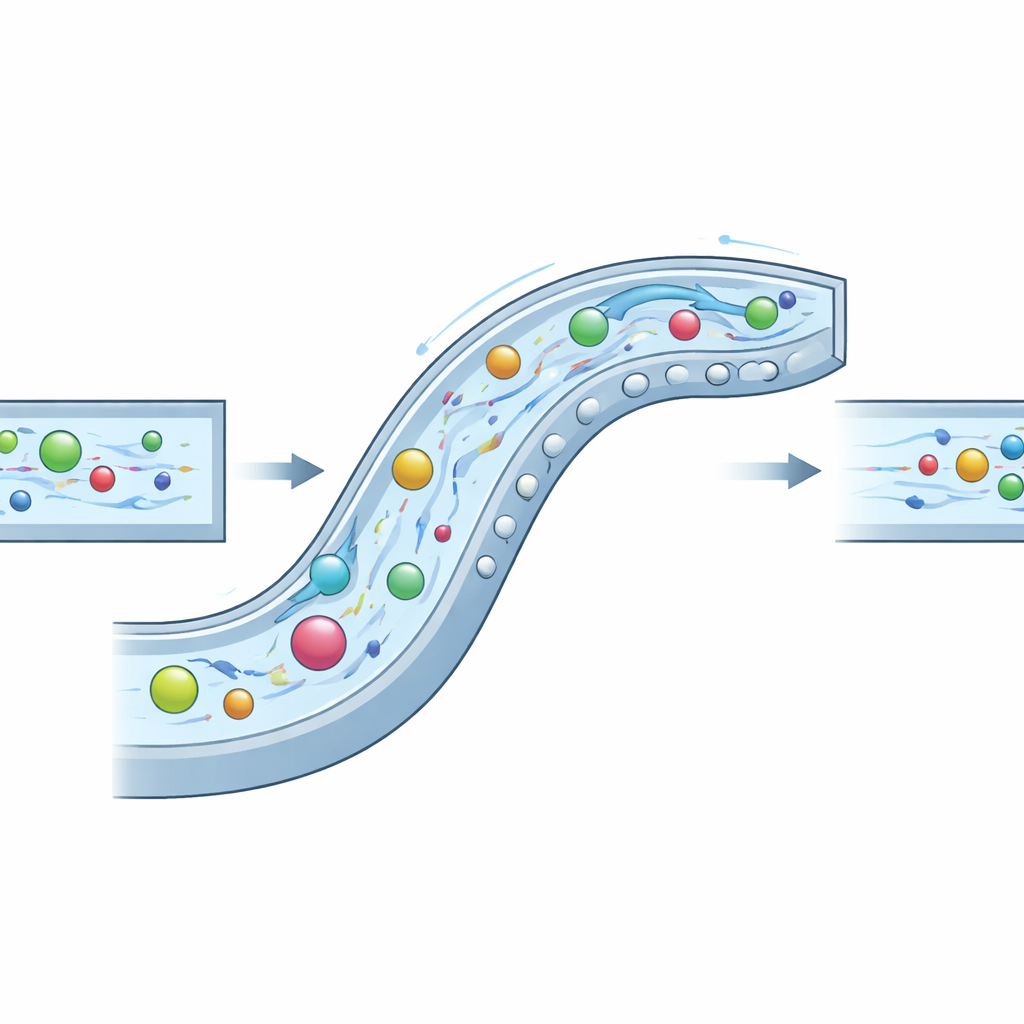
Den neuen Mikrokanal-Highway testen
Um das Verhalten des Systems zu verstehen, führte das Team zunächst detaillierte Computersimulationen der Strömungsmuster, der inneren Wirbel und der Scherkräfte nahe den Wänden durch. Sie führten eine neue Messgröße ein – die «Breite der Gleichgewichtszone» – die abschätzt, wie eng Partikel in der Kanalmitte eingeschlossen werden können. Das beste Design, bei dem Seiten- und vertikale Hindernisse phasengleich ausgerichtet waren, erzeugte eine sehr schmale Gleichgewichtszone von etwa 16 Mikrometern, was darauf hindeutet, dass Partikel zu einem dünnen Kernstrom zusammenlaufen würden. Simulationen zeigten außerdem, dass die zusätzliche Elastizität die Stärke der Wirbel kaum veränderte, wohl aber die rückstellenden Kräfte zur Mitte verstärkte und so das Fokussieren schärfte, ohne die Strömung zu destabilisieren.
Die Flüssigkeit abstimmen und verschiedene Partikelgrößen behandeln
Als Nächstes bauten die Forscher den Chip und pumpten fluoreszierende Kunststoffkügelchen in Salzlösungen mit unterschiedlichen Hyaluronsäure-Gehalten ein. Durch Aufnahmen der Partikel von oben und von der Seite mit Tausenden von Bildern pro Sekunde maßen sie sowohl die Breite des fokussierten Bands als auch den Anteil der Partikel, der tatsächlich daran teilnahm. Mit der richtigen Polymerkonzentration erzeugte der Kanal einen einzelnen hellen Streifen, der nur geringfügig breiter war als die Partikel selbst, über einen weiten Bereich von Durchflussraten. Kügelchen mit 10 bis 20 Mikrometern Durchmesser – die normalerweise an unterschiedlichen Positionen sitzen würden – wurden alle in denselben zentralen Pfad gebracht, mit Fokussierungseffizienzen über 95 % unter optimalen Bedingungen. Eine komplexere, versetzte Hindernisanordnung funktionierte ebenfalls, jedoch nicht so gut oder robust.
Von Kunststoffkügelchen zu lebenden weißen Blutkörperchen
Schließlich testete das Team das Gerät mit weißen Blutkörperchen, die stark in der Größe variieren und sich unter starken Kräften verformen können. Dennoch brachte der Kanal die meisten dieser Zellen – grob im Bereich von 7 bis 20 Mikrometern – bei moderaten Flussraten in einen einzigen schmalen Strom und erreichte eine Spitzenfokussierungseffizienz von knapp über 96 %. Bei sehr hohen Geschwindigkeiten dehnten und verkürzten sich die Zellen, wodurch sie empfindlicher gegenüber den Wirbelströmen wurden und von der Mittellinie abdrifteten; innerhalb praktikabler Betriebsfenster blieb das Fokussieren jedoch stark. Das zeigt, dass die INVEST-Strategie mit empfindlichen biologischen Proben kompatibel ist, nicht nur mit starren Testkügelchen.
Was das für künftige Laborinstrumente bedeutet
Im Kern zeigt diese Arbeit, dass man durch geschicktes Gestalten eines Mikrokanals und die Wahl einer leicht elastischen Flüssigkeit eine vielfältige Menge mikroskopischer Reisender – starre Partikel wie auch weiche Zellen – in dieselbe dreidimensionale Spur lenken kann. Das macht optische und elektrische Messungen konsistenter, erhöht den Durchsatz mikro‑skaliger Analysatoren und reduziert den Bedarf an komplexer Ausrichttechnik. Der Verbundkanal der Autoren verwandelt ein ingenieurtechnisches Problem – unterschiedlich große Partikel auf unterschiedlichen Wegen – in einen Vorteil, indem er Trägheit, Elastizität und Wirbelströmung zusammenarbeiten lässt. Dieser Ansatz könnte helfen, leistungsfähige diagnostische Instrumente auf Chips zu schrumpfen und so präzisere Blutanalysen und Einzelzellstudien näher an die routinemäßige klinische Praxis zu bringen.
Zitation: Zhao, T., Zeng, P., Ji, C. et al. Coupling inertial, viscoelastic, and enhanced secondary flow in a composite microchannel: achieving high-precision multi-sized particle 3D central co-focusing. Microsyst Nanoeng 12, 134 (2026). https://doi.org/10.1038/s41378-026-01254-9
Schlüsselwörter: Mikrofluidik, Zellfokussierung, träger Fluss, viskoelastische Flüssigkeiten, Durchflusszytometrie