Clear Sky Science · es
Acoplando inercia, viscoelasticidad y flujo secundario potenciado en un microcanal compuesto: logrando co‑enfoque central 3D de partículas de múltiples tamaños con alta precisión
Poniendo en fila a los pequeños viajeros
Imagínese intentar fotografiar miles de coches moviéndose rápidamente por una autopista, pero algunos son motocicletas y otros son autobuses. Para medir cada uno con precisión, querría que pasaran frente a su cámara en una sola fila ordenada, no repartidos por los carriles. En los laboratorios biomédicos, los científicos enfrentan un problema similar con células y microesferas que corren por canales delgados como un pelo. Este artículo describe un nuevo chip microfluídico que dirige con suavidad partículas y glóbulos blancos de distintos tamaños hacia la misma trayectoria tridimensional estrecha, mejorando cómo se cuentan, separan y analizan para diagnóstico e investigación. 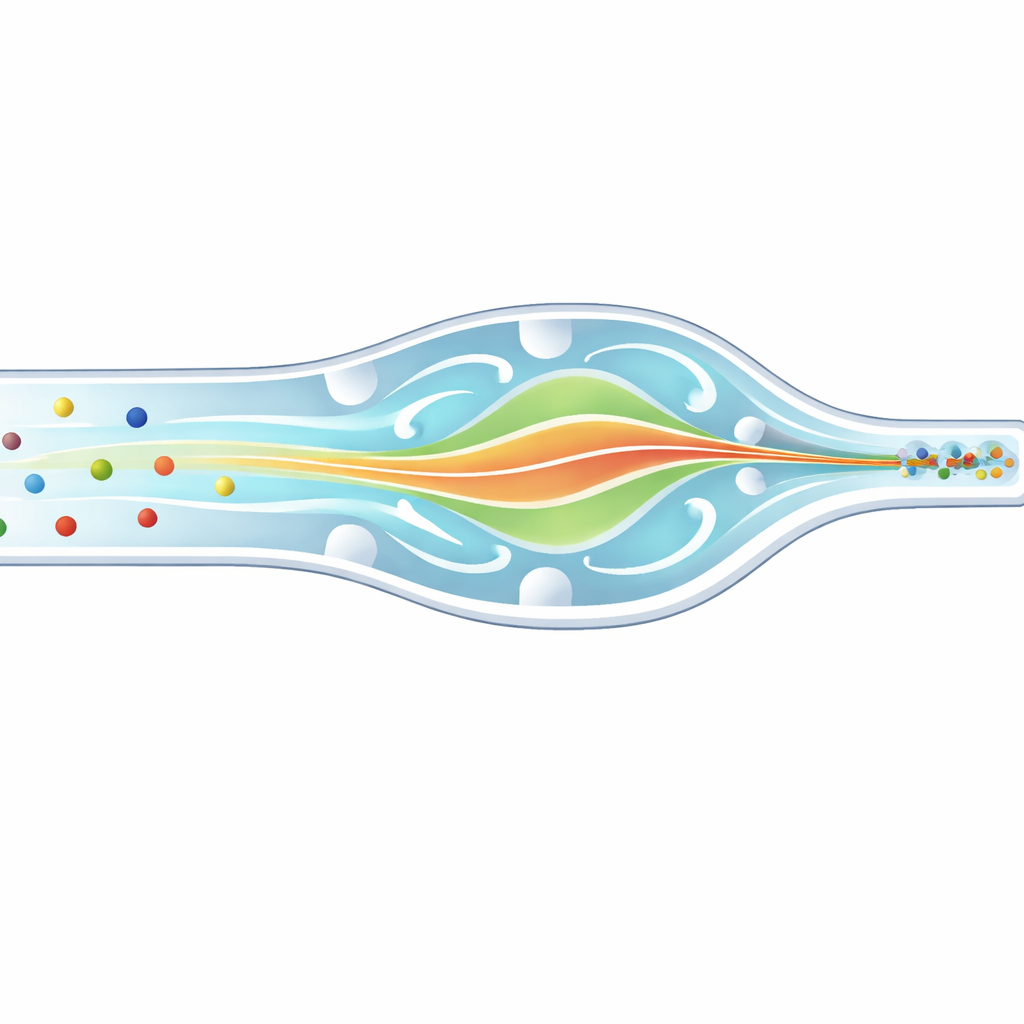
Por qué alinear las células importa de verdad
Muchas herramientas médicas de vanguardia, como los citómetros de flujo y los analizadores de célula única, funcionan enviando células por canales diminutos y examinándolas con luz o señales eléctricas. Si unas células pasan cerca de la pared y otras cruzan por el centro, experimentan iluminación y fuerzas diferentes, lo que emborrona las medidas y oculta diferencias sutiles entre células. Los diseños microfluídicos convencionales pueden enfocar partículas, pero por lo general solo de un tamaño a la vez, o las empujan hacia las esquinas en lugar del verdadero centro. Eso significa que mezclas de células —como la diversa población de glóbulos blancos en la sangre— son difíciles de medir de forma limpia en una sola pasada.
Combinando tres empujes suaves a microescala
Los investigadores abordaron esto construyendo un microcanal «compuesto» cuidadosamente esculpido que explota tres comportamientos del fluido a la vez: inercia (la tendencia del fluido y las partículas en movimiento a seguir), elasticidad (una elasticidad añadida al disolver un biopolímero llamado ácido hialurónico) y corrientes secundarias de remolino creadas por curvas y obstáculos. En su diseño, el canal se curva como una espiral lenta y lleva una serie de protuberancias semicirculares tanto a lo largo de la pared lateral como en el techo y el suelo. Estas características generan vórtices controlados que arrastran las partículas lejos de las esquinas, mientras que las fuerzas elásticas del fluido las empujan hacia regiones de flujo más suave. Al ajustar la geometría del canal y las propiedades del fluido, los autores crean un régimen sinérgico que llaman INVEST, en el que los tres efectos cooperan en lugar de competir. 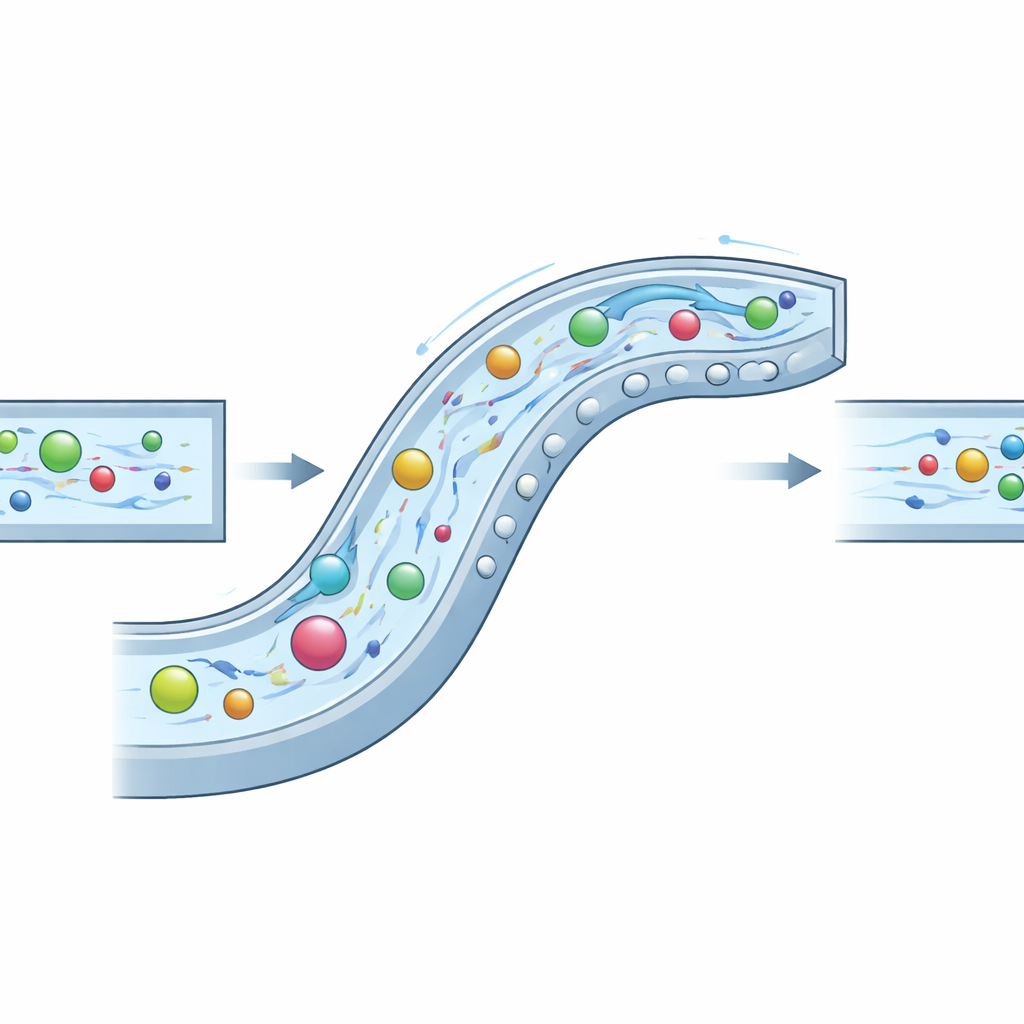
Probando la nueva autopista microcanal
Para comprender cómo se comporta este sistema, el equipo primero realizó simulaciones informáticas detalladas de los patrones de flujo, de los remolinos internos y de la intensidad del cizallamiento cerca de las paredes. Introdujeron una nueva medida —la «anchura de la zona de equilibrio»— que estima cuán firmemente se pueden confinar las partículas en el centro del canal. El mejor diseño, con obstáculos laterales y verticales alineados en fase, produjo una zona de equilibrio muy estrecha de unos 16 micrómetros, lo que sugiere que las partículas se agruparían en una corriente central fina. Las simulaciones también mostraron que la elasticidad añadida apenas cambió la fuerza de los remolinos pero sí aumentó las fuerzas restauradoras hacia el centro, afinando el enfoque sin desestabilizar el flujo.
Afinando el fluido y manejando distintos tamaños de partículas
A continuación, los investigadores construyeron el chip e introdujeron perlas plásticas fluorescentes suspendidas en soluciones salinas con distintas cantidades de ácido hialurónico. Filmando las partículas desde arriba y desde un costado a miles de fotogramas por segundo, midieron tanto el ancho de la banda enfocada como la fracción de partículas que realmente se unían a ella. Con la concentración adecuada de polímero, el canal produjo una sola franja brillante solo un poco más ancha que las propias partículas en un amplio rango de caudales. Perlas de 10 a 20 micrómetros de diámetro —que normalmente se situarían en posiciones diferentes— se llevaron todas a la misma trayectoria central con eficiencias de enfoque superiores al 95% en condiciones óptimas. Un diseño de obstáculos más complejo y escalonado funcionó, pero no tan bien ni tan robustamente.
De perlas plásticas a glóbulos blancos vivos
Por último, el equipo puso a prueba el dispositivo con glóbulos blancos, que varían mucho en tamaño y pueden deformarse bajo fuerzas intensas. Aun así, el canal alineó la mayoría de estas células —con tamaños aproximados entre 7 y 20 micrómetros— en una sola corriente estrecha a caudales moderados, alcanzando una eficiencia máxima de enfoque de algo más del 96%. A velocidades muy altas, las células se estiraron y encogieron, volviéndolas más vulnerables a las corrientes de remolino y provocando que se desviaran de la línea central, pero dentro de ventanas de operación prácticas el enfoque se mantuvo sólido. Esto demuestra que la estrategia INVEST es compatible con muestras biológicas delicadas, no solo con microesferas rígidas de prueba.
Qué significa esto para futuras herramientas de laboratorio
En esencia, este trabajo muestra que, al dar forma con arte a un microcanal y elegir un fluido ligeramente elástico, es posible conducir a una multitud diversa de viajeros microscópicos —partículas rígidas o células blandas— hacia el mismo carril tridimensional. Eso hace que las mediciones ópticas y eléctricas sean más consistentes, aumenta el rendimiento de los analizadores a microescala y reduce la necesidad de hardware complejo de alineación. El canal compuesto de los autores convierte un problema de ingeniería —partículas de distinto tamaño tomando rutas diferentes— en una ventaja al permitir que inercia, elasticidad y flujo de remolino trabajen en conjunto. Este enfoque podría ayudar a reducir a chips instrumentos diagnósticos potentes, acercando análisis sanguíneos más precisos y estudios de célula única a la práctica clínica rutinaria.
Cita: Zhao, T., Zeng, P., Ji, C. et al. Coupling inertial, viscoelastic, and enhanced secondary flow in a composite microchannel: achieving high-precision multi-sized particle 3D central co-focusing. Microsyst Nanoeng 12, 134 (2026). https://doi.org/10.1038/s41378-026-01254-9
Palabras clave: microfluidos, enfoque de células, flujo inercial, fluidos viscoelásticos, citometría de flujo