Clear Sky Science · pt
Acoplamento de inércia, viscoelasticidade e fluxo secundário aprimorado em um microcanal composto: atingindo co-focalização central 3D de partículas multirresponsivas com alta precisão
Alinhando pequenos viajantes
Imagine tentar fotografar milhares de carros em alta velocidade numa rodovia, mas alguns são motocicletas e outros são ônibus. Para medir cada um com precisão, você gostaria que passassem pela sua câmera em fila única, não espalhados pelas pistas. Em laboratórios biomédicos, os cientistas enfrentam um problema semelhante com células e microesferas que correm por canais finíssimos. Este artigo descreve um novo chip microfluídico que força suavemente partículas e glóbulos brancos de diferentes tamanhos a seguirem o mesmo caminho estreito tridimensional, melhorando a contagem, a separação e a análise para diagnóstico e pesquisa. 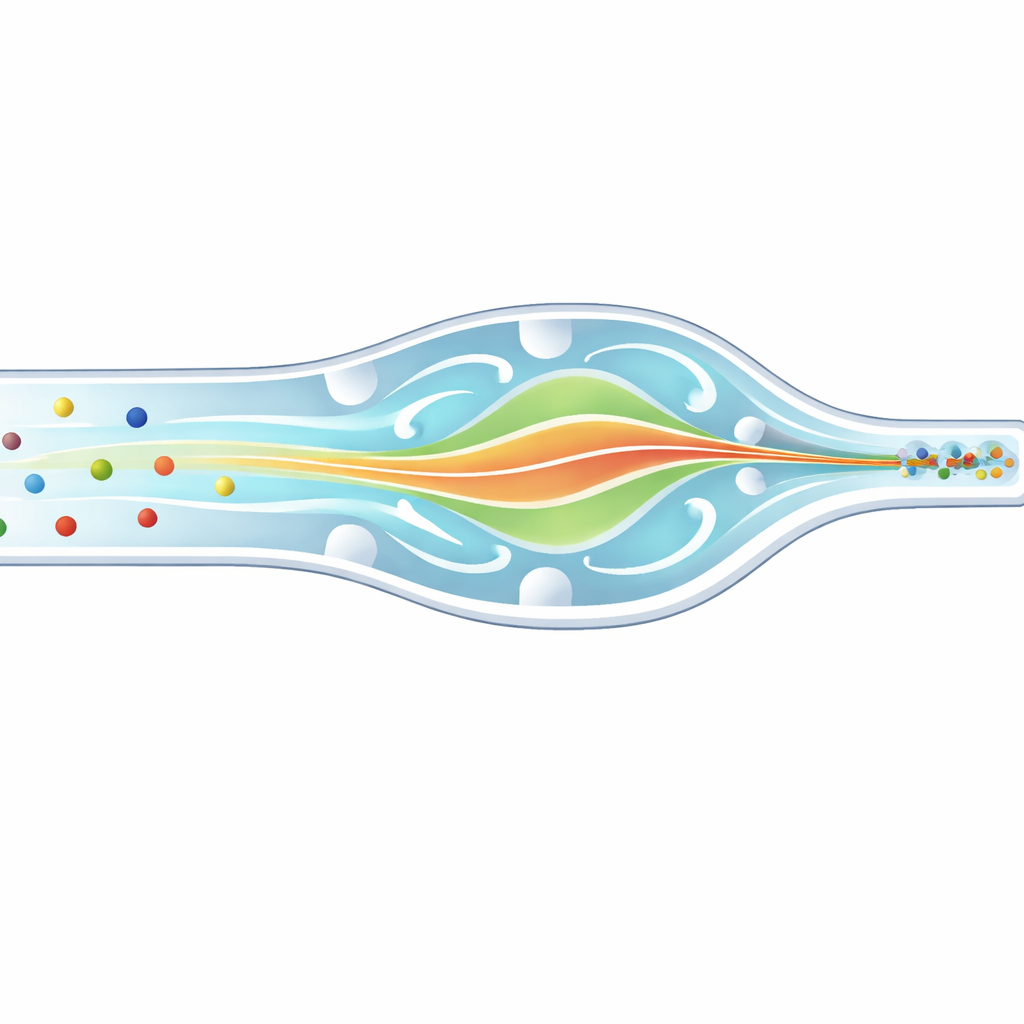
Por que alinhar células é realmente importante
Muitos instrumentos médicos de ponta, como citômetros de fluxo e analisadores de célula única, funcionam enviando células por canais minúsculos e interrogando-as com luz ou sinais elétricos. Se algumas células passam perto da parede e outras pelo centro, elas experimentam iluminação e forças diferentes, o que borrará as medições e ocultará diferenças sutis entre as células. Projetos microfluídicos convencionais podem focalizar partículas, mas geralmente apenas de um tamanho por vez, ou as empurram para os cantos em vez do verdadeiro centro. Isso significa que misturas de células — como os diversos glóbulos brancos presentes no sangue — são difíceis de medir de forma limpa em uma única passagem.
Combinando três impulsos suaves em escala micro
Os pesquisadores abordaram isso construindo um microcanal "composto" cuidadosamente esculpido que explora três comportamentos do fluido ao mesmo tempo: inércia (a tendência do fluido e das partículas em movimento de continuar), elasticidade (uma maleabilidade extra adicionada pela dissolução de um biopolímero chamado ácido hialurônico) e correntes secundárias em redemoinho criadas por curvas e obstáculos. No projeto deles, o canal curva-se como uma espiral lenta e carrega uma série de protuberâncias semicirculares tanto ao longo da parede lateral quanto no teto e no piso. Essas características criam vórtices controlados que varrem as partículas para longe dos cantos, enquanto as forças elásticas no fluido as empurram em direção a regiões de fluxo mais suave. Ao ajustar a geometria do canal e as propriedades do fluido, os autores criam um regime sinérgico que chamam de INVEST, no qual os três efeitos cooperam em vez de competir. 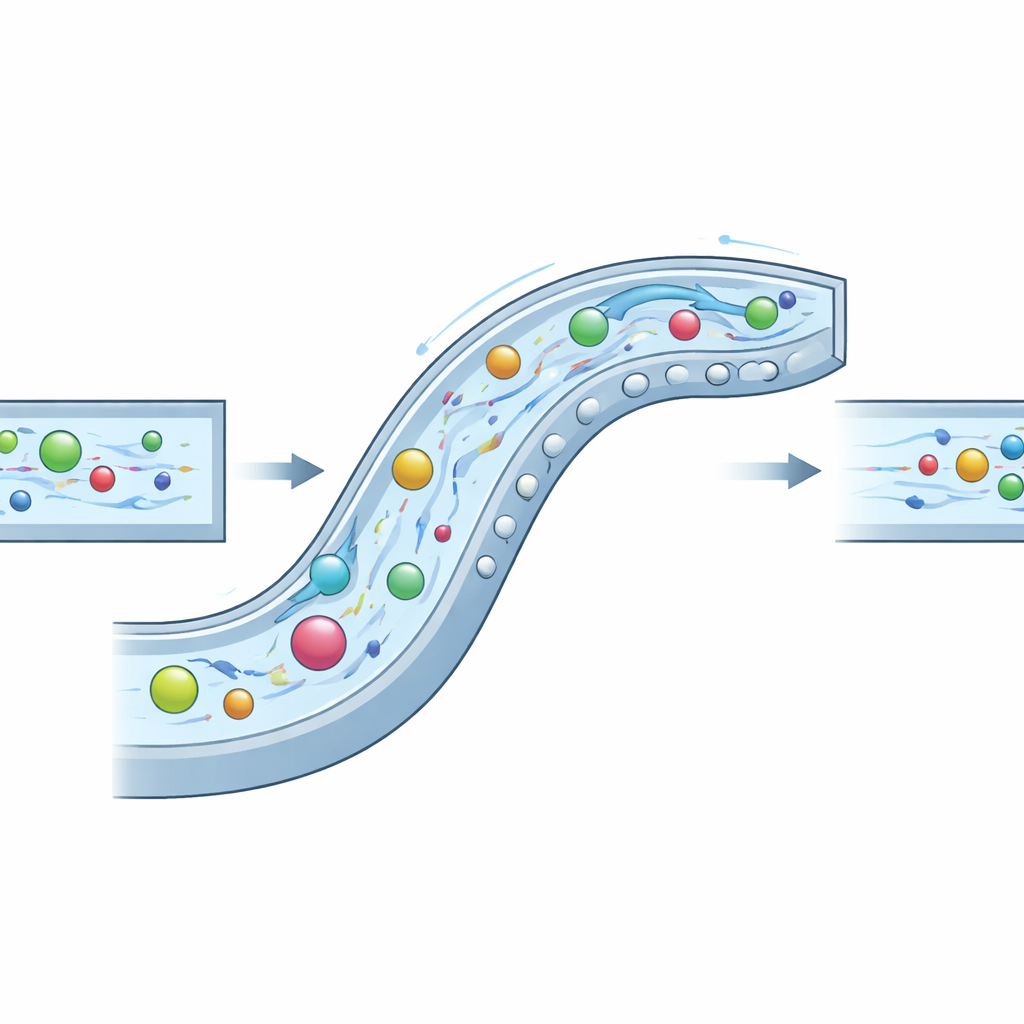
Testando a nova rodovia microcanal
Para entender como o sistema se comporta, a equipe primeiro executou simulações computacionais detalhadas dos padrões de fluxo, dos redemoinhos internos e de quão intensamente o fluido cisalha perto das paredes. Eles introduziram uma nova referência — a "largura da zona de equilíbrio" — que estima quão firmemente as partículas podem ser confinadas no centro do canal. O melhor projeto, com obstáculos laterais e verticais alinhados em fase, produziu uma zona de equilíbrio muito estreita de cerca de 16 micrômetros, sugerindo que as partículas se reuniriam em um fluxo central fino. As simulações também mostraram que a elasticidade adicionada mal alterou a força dos redemoinhos, mas aumentou as forças restauradoras em direção ao centro, aguçando o foco sem desestabilizar o fluxo.
Ajustando o fluido e lidando com diferentes tamanhos de partícula
Em seguida, os pesquisadores construíram o chip e injetaram esferas plásticas fluorescentes suspensas em soluções salinas contendo diferentes quantidades de ácido hialurônico. Filmando as partículas de cima e de lado a milhares de quadros por segundo, mediram tanto a largura da faixa focalizada quanto a fração de partículas que realmente se juntavam a ela. Com a concentração certa do polímero, o canal produziu uma faixa única e brilhante apenas um pouco mais larga do que as próprias partículas ao longo de uma ampla faixa de taxas de fluxo. Esferas de 10 a 20 micrômetros de diâmetro — que normalmente se posicionariam em pontos diferentes — foram todas trazidas para o mesmo caminho central com eficiências de focalização acima de 95% em condições ótimas. Um arranjo de obstáculos mais complexo e escalonado funcionou, mas não tão bem nem tão robustamente.
De esferas plásticas a glóbulos brancos vivos
Finalmente, a equipe desafiou o dispositivo com glóbulos brancos, que variam amplamente em tamanho e podem se deformar sob forças fortes. Ainda assim, o canal alinhou a maioria dessas células — variando aproximadamente de 7 a 20 micrômetros — em um fluxo estreito único em taxas de fluxo moderadas, alcançando uma eficiência máxima de focalização pouco acima de 96%. Em velocidades muito altas, as células alongaram‑se e encolheram, tornando‑se mais vulneráveis às correntes em redemoinho e fazendo‑as desviar da linha central, mas dentro de janelas operacionais práticas a focalização permaneceu forte. Isso demonstra que a estratégia INVEST é compatível com amostras biológicas delicadas, não apenas com esferas de teste rígidas.
O que isso significa para ferramentas de laboratório futuras
Em essência, este trabalho mostra que, ao modelar habilidosamente um microcanal e escolher um fluido ligeiramente elástico, é possível guiar uma multidão diversa de viajantes microscópicos — partículas rígidas ou células moles — para a mesma pista tridimensional. Isso torna as medições ópticas e elétricas mais consistentes, aumenta o rendimento de analisadores em microescala e reduz a necessidade de hardware complexo de alinhamento. O canal composto dos autores transforma uma dor de cabeça de engenharia — partículas de tamanhos diferentes seguindo trajetórias distintas — em uma vantagem ao permitir que inércia, elasticidade e fluxo em redemoinho atuem em conjunto. Essa abordagem pode ajudar a reduzir instrumentos diagnósticos poderosos em chips, aproximando análises sanguíneas mais precisas e estudos de célula única da prática clínica rotineira.
Citação: Zhao, T., Zeng, P., Ji, C. et al. Coupling inertial, viscoelastic, and enhanced secondary flow in a composite microchannel: achieving high-precision multi-sized particle 3D central co-focusing. Microsyst Nanoeng 12, 134 (2026). https://doi.org/10.1038/s41378-026-01254-9
Palavras-chave: microfluídica, focalização de células, fluxo inercial, fluidos viscoelásticos, citometria de fluxo