Clear Sky Science · sv
Single-cell multi-omics-sekvensering avslöjar cellspecifika transkriptom- och kromatinåtkomlighetsprofiler i tarmmikrobiommet: butyratproducerad smärtmodulation
Varför din tarm kan spela roll för käksmärta
Personer med temporomandibulära ledproblem (TMJ) lever ofta med envis käksmärta som gör det svårt att prata, äta och sova. Många nuvarande behandlingar ger bara partiell eller tillfällig lindring och kan medföra biverkningar, särskilt när de bygger på smärtstillande läkemedel som opioider. Denna studie utforskar en oväntad allierad i jakten på säkrare behandlingar: små molekyler som bildas av tarmbakterier. Genom att granska enskilda hjärnceller i detalj visar forskarna hur en tarm-deriverad substans kallad butyrat kan dämpa TMJ-smärta och peka mot framtida icke-opioida behandlingar.
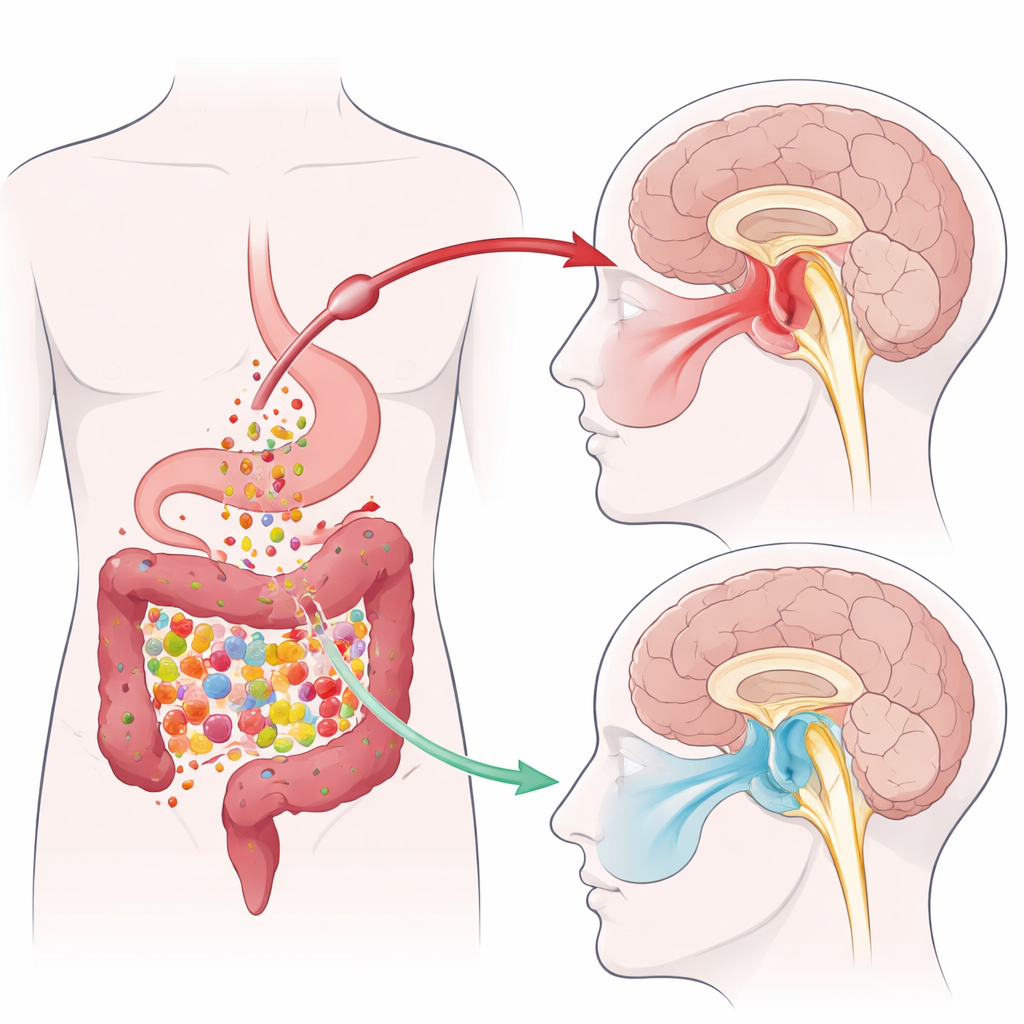
Från tarmbakterier till lindring av käksmärta
Forskargruppen använde en modell för inflammatorisk TMJ-smärta hos möss, framkallad genom injektion av ett irriterande ämne i käkleden. Denna procedur gjorde djuren mer känsliga för beröring på den sida av ansiktet som är kopplad till den skadade leden. Tidigare arbete från samma grupp hade visat att TMJ-inflammation sänker nivåerna av kortkedjiga fettsyror som produceras av tarmmikrober, särskilt butyrat. I denna studie gavs mössen tributyrin, en stabil föregångare som bryts ned till butyrat i tarmen, oralt i 10 dagar. Denna behandling ökade djurens smärttrösklar på den drabbade sidan av ansiktet—de reagerade alltså mindre kraftigt på mekanisk stimulering—samtidigt som den motsatta sidan var oförändrad. Mätningar i avföring, blod och en hjärnstamsregion kallad spinal trigeminus nucleus caudalis (Sp5C) visade att TMJ-inflammation minskade butyratnivåer i hela kroppen—och att tributyrin återställde dem till normala nivåer.
Kartläggning av smärtporten i hjärnstammen
Sp5C fungerar som en viktig relästation för ansiktssmärta, inklusive signaler från TMJ. För att förstå vad som sker där under smärta och återhämtning använde forskarna en kraftfull "single-cell multi-omics"-metod. De isolerade kärnor från Sp5C-vävnad och mätte för varje enskild cell både vilka gener som var aktiva och hur öppet det omgivande DNA:t var—en indikation på hur lätt gener kan aktiveras. Detta gjorde det möjligt att identifiera 12 distinkta celltyper, inklusive flera neuronala typer, immunceller och stödjeceller kallade gliaceller, samt att se hur var och en reagerade på TMJ-inflammation och tributyrin. Intressant nog förändrades inte celltypssammansättningen i stort; istället påverkade smärta och behandling huvudsakligen hur befintliga celler använde sina gener.
Viktiga brytare som slås på av smärta och återställs av butyrat
Genom att jämföra friska möss, möss med TMJ-smärta och möss behandlade med tributyrin identifierade teamet specifika gener vars aktivitet konsekvent stördes av smärta och sedan återställdes av butyrat. I flera neurongrupper och precursorceller framhölls fem gener—Nop14, Matk, Idh3b, Ndst2 och Tomm6—som centrala aktörer. TMJ-inflammation påverkade både aktiviteten hos dessa gener och åtkomligheten i närliggande DNA-regioner, medan tributyrin vände dessa förändringar. Forskarna zoomade sedan in på Nop14 i en cellklass kallad neuropeptidneuroner, som visade särskilt starka förändringar. De använde ytterligare analyser för att kartlägga hur lokala DNA-kontrollelement och regulatoriska proteiner interagerar för att öka eller dämpa denna gens aktivitet under smärtförhållanden och efter behandling.
Hur genpaketering kopplas till smärtsignalering
Eftersom det är känt att butyrat påverkar hur tätt DNA är lindat kring histonproteiner undersökte forskarna också histonacetylering, en kemisk märkning kopplad till mer permissiv genaktivitet. TMJ-inflammation sänkte den övergripande histonacetyleringen i Sp5C, medan tributyrin återförde den mot normala nivåer. Samtidigt blev en specifik region nära Nop14-genen mer öppen och mer acetylerad under smärta, i linje med ökad genaktivitet. När teamet använde en virusbaserad metod för att minska Nop14-nivåerna direkt i Sp5C observerade de två effekter: histonacetyleringen i denna region återgick mot baslinje och djurens TMJ-smärtrespons minskade. Detta tyder på att Nop14 sitter i en avgörande korsning där förändringar i genpaketering, utlösta av förlust eller återställande av butyrat, kan förstärka eller dämpa smärtvägar.
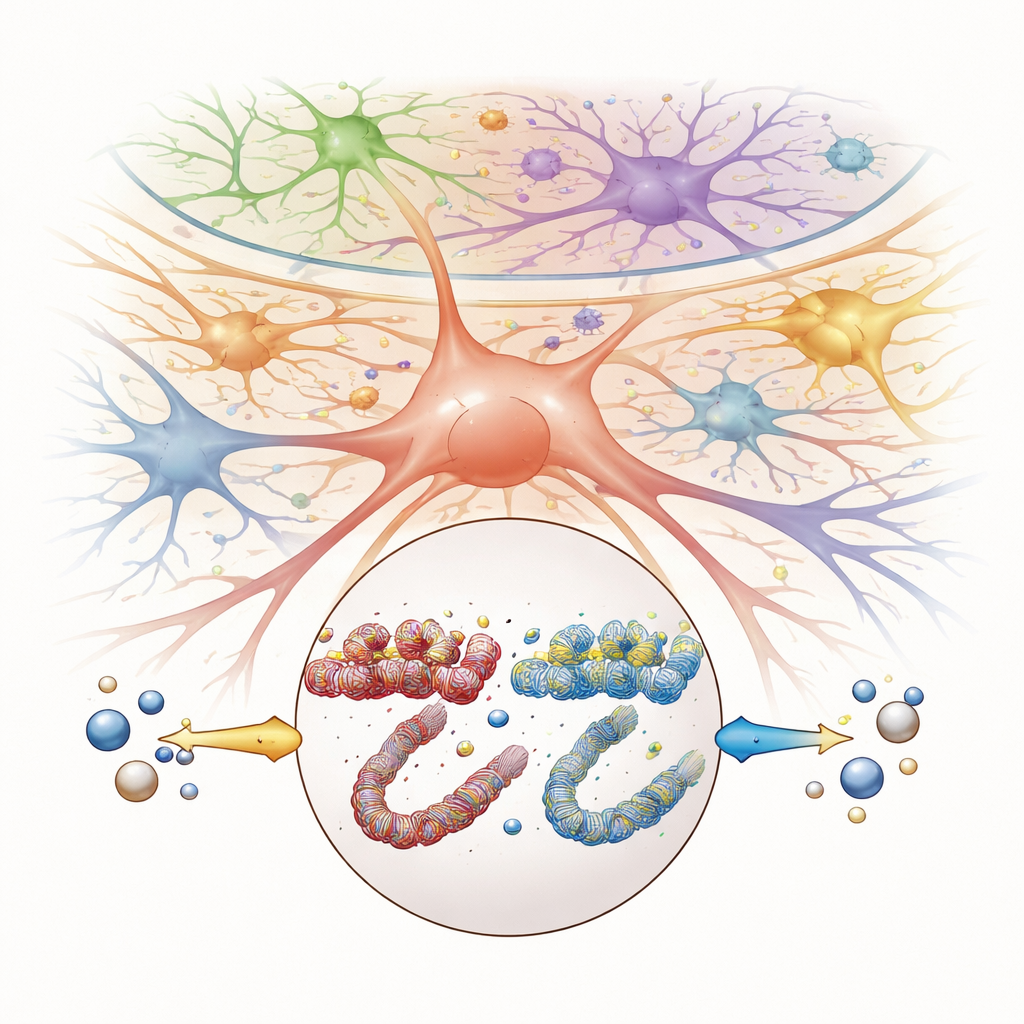
En ny väg mot icke-opioida smärtbehandlingar
Sammanfattningsvis kopplar studien tarmderiverat butyrat till lindring av TMJ-smärta genom precisa, cellspecifika förändringar i genreglering inom ett smärtcenter i hjärnstammen. Istället för att bara bedöva smärtsignaler tycks tributyrin korrigera molekylära obalanser som TMJ-inflammation skapar i specifika neuroner och stödjeceller, där Nop14 framträder som ett lovande måltavla. För patienter innebär detta arbete ännu ingen omedelbar terapi, men det stärker idén att manipulera tarmmetaboliter—eller direkt rikta in sig på samma gendonsomkopplare de reglerar—kan erbjuda framtida icke-opioida behandlingar för TMJ-störningar och möjligen andra former av kronisk inflammatorisk smärta.
Citering: Tao, R., Liu, S., Crawford, J. et al. Single-cell multi-omics sequencing reveals cell-specific transcriptomic and chromatin accessibility profiles in gut microbiome metabolite butyrate-produced pain modulation. Int J Oral Sci 18, 37 (2026). https://doi.org/10.1038/s41368-026-00432-9
Nyckelord: temporomandibulär ledsmärta, tarmmikrobiom, butyrat, epigenetisk reglering, single-cell-sekvensering