Clear Sky Science · nl
Single-cell multi-omics sequencing onthult celspecifieke transcriptomische en chromatine-toegankelijkheidsprofielen in darmmicrobioommetaboliet butyraat-geïnduceerde pijnmodulatie
Waarom je darm relevant kan zijn voor kaakpijn
Mensen met temporomandibulaire gewrichtsstoornissen (TMJ) leven vaak met hardnekkige kaakpijn die praten, eten en slapen bemoeilijkt. Veel huidige behandelingen bieden slechts gedeeltelijke of tijdelijke verlichting en kunnen bijwerkingen hebben, vooral wanneer ze afhangen van pijnstillers zoals opioïden. Deze studie onderzoekt een onverwachte bondgenoot in de zoektocht naar veiligere therapieën: kleine moleculen geproduceerd door darmbacteriën. Door diep in individuele hersencellen te kijken, tonen de onderzoekers aan hoe een darmafgeleide stof genaamd butyraat TMJ-pijn kan dempen en richting kan geven aan toekomstige, niet-opioïde behandelingen.
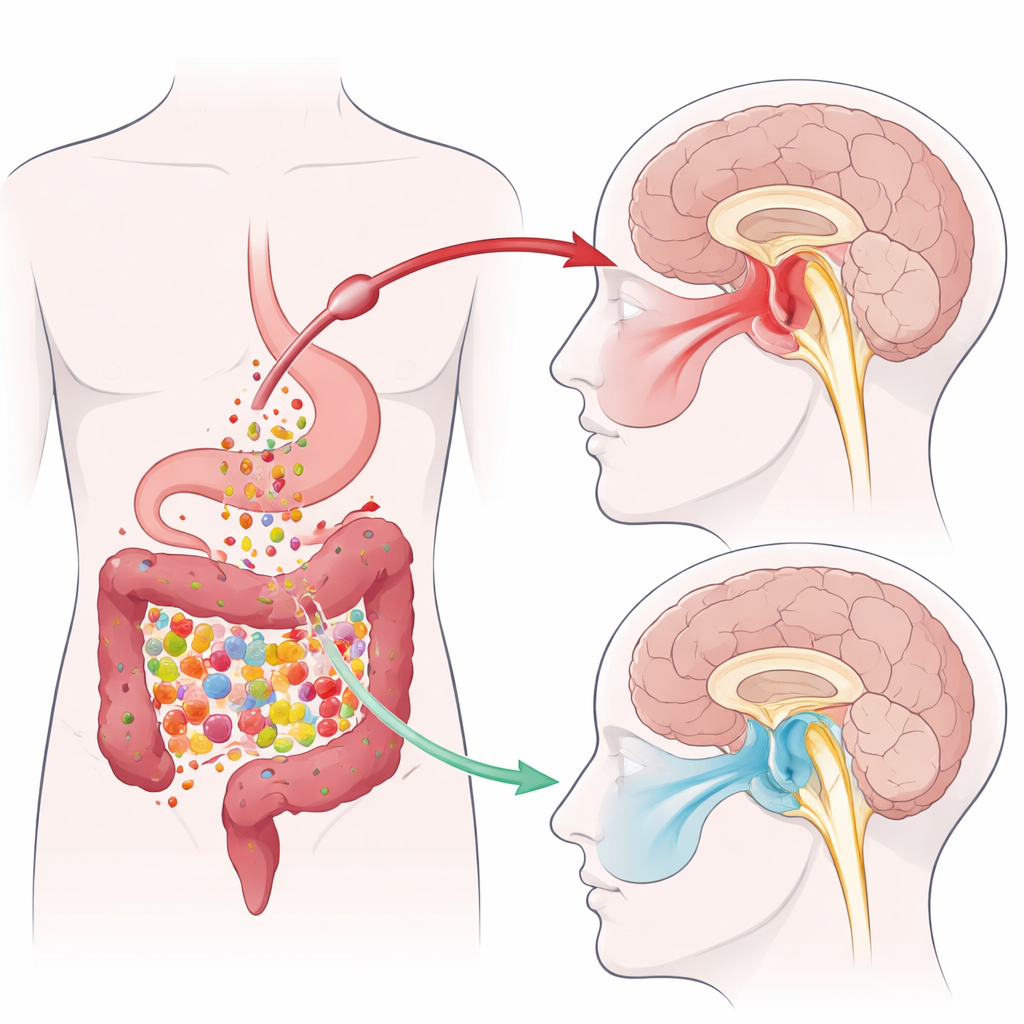
Van darmbacteriën naar verlichting van kaakpijn
Het team gebruikte een muismodel van inflammatoire TMJ-pijn dat werd opgezet door een irriterende stof in het kaakgewricht te injecteren. Deze procedure maakte de dieren gevoeliger voor aanraking aan de zijde van het gezicht die verbonden is met het beschadigde gewricht. Eerder werk van dezelfde groep had aangetoond dat TMJ-ontsteking de niveaus van korteketenvetzuren geproduceerd door darmmicroben verlaagt, met name butyraat. In deze studie kregen muizen gedurende 10 dagen tributyryn toegediend, een stabieler verbinding die in de darm afbreekt tot butyraat. Deze behandeling verhoogde de pijndrempels van de dieren aan de aangedane zijde van het gezicht, wat betekent dat ze minder sterk reageerden op mechanische prikkels, terwijl de andere zijde ongewijzigd bleef. Metingen van feces, bloed en een hersenstamgebied genaamd nucleus spinalis trigeminus caudalis (Sp5C) toonden aan dat TMJ-ontsteking butyraat in het hele lichaam verminderde — en dat tributyryn dit weer op normale niveaus bracht.
De pijnpoort in de hersenstam in kaart brengen
De Sp5C fungeert als een belangrijke schakelpost voor aangezichtspijn, inclusief signalen van het TMJ. Om te begrijpen wat daar gebeurt tijdens pijn en herstel, gebruikten de onderzoekers een krachtige "single-cell multi-omics" aanpak. Ze isoleerden kernen uit Sp5C-weefsel en maten voor elke individuele cel zowel welke genen actief waren als hoe open het omringende DNA was — een aanwijzing voor hoe gemakkelijk genen geactiveerd kunnen worden. Hierdoor konden ze 12 verschillende celtypen identificeren, waaronder meerdere soorten neuronen, immuuncellen en ondersteunende cellen genaamd glia, en zien hoe elk type reageerde op TMJ-ontsteking en tributyryn. Interessant genoeg veranderde de algehele samenstelling van celtypen niet veel; in plaats daarvan beïnvloedden pijn en behandeling vooral hoe bestaande cellen hun genen gebruikten.
Belangrijke schakelaars omgeklapt door pijn en teruggezet door butyraat
Door gezonde muizen, muizen met TMJ-pijn en muizen behandeld met tributyryn te vergelijken, bracht het team specifieke genen in kaart waarvan de activiteit consequent verstoord werd door pijn en vervolgens door butyraat werd teruggezet. In verschillende neurongroepen en voorlopercellen identificeerden ze vijf genen — Nop14, Matk, Idh3b, Ndst2 en Tomm6 — als centrale spelers. TMJ-ontsteking veranderde zowel de activiteit van deze genen als de toegankelijkheid van nabijgelegen DNA-regio's, terwijl tributyryn deze verschuivingen ongedaan maakte. De onderzoekers zoomden vervolgens in op Nop14 in een klasse van cellen die neuropeptide-neuronen worden genoemd, welke bijzonder sterke veranderingen lieten zien. Met aanvullende analyses brachten ze in kaart hoe lokale DNA-controle-elementen en regulatoire eiwitten samenwerken om dit gen onder pijncondities en na behandeling te versterken of te onderdrukken.
Hoe genverpakking verbonden is met pijnsignalen
Aangezien bekend is dat butyraat invloed heeft op hoe strak DNA rond histon-eiwitten gewikkeld zit, onderzochten de onderzoekers ook histonacetylering, een chemische markering die geassocieerd wordt met meer toegankelijke genexpressie. TMJ-ontsteking verlaagde de algemene histonacetylering in de Sp5C, terwijl tributyryn deze weer richting normale niveaus bracht. Tegelijkertijd werd een specifieke regio nabij het Nop14-gen tijdens pijn opener en sterker geacetyleerd, wat overeenkomt met verhoogde genactiviteit. Toen het team met een virusgebaseerde methode Nop14-niveaus direct in de Sp5C verlaagde, zagen ze twee effecten: histonacetylering in deze regio keerde deels terug naar het uitgangsniveau en de TMJ-pijnresponsen van de dieren namen af. Dit suggereert dat Nop14 een cruciale knooppuntfunctie vervult waarbij veranderingen in genverpakking, veroorzaakt door verlies of herstel van butyraat, pijnroutes kunnen versterken of kalmeren.
Een nieuw pad naar niet-opioïde pijntherapieën
Al met al koppelt de studie darmafgeleid butyraat aan TMJ-pijnverlichting via precieze, celspecifieke veranderingen in genregulatie binnen een pijnknooppunt in de hersenstam. In plaats van simpelweg pijnsignalen te verdoven, lijkt tributyryn moleculaire onevenwichtigheden te corrigeren die TMJ-ontsteking veroorzaakt in bepaalde neuronen en ondersteunende cellen, waarbij Nop14 naar voren komt als een veelbelovend doelwit. Voor patiënten vertaalt dit werk zich nog niet direct in een onmiddellijke behandeling, maar het ondersteunt het idee dat het manipuleren van darmmetabolieten — of het direct richten op dezelfde genschakelaars die ze beïnvloeden — in de toekomst niet-opioïde behandelingen voor TMJ-stoornissen en mogelijk andere vormen van chronische inflammatoire pijn kan bieden.
Bronvermelding: Tao, R., Liu, S., Crawford, J. et al. Single-cell multi-omics sequencing reveals cell-specific transcriptomic and chromatin accessibility profiles in gut microbiome metabolite butyrate-produced pain modulation. Int J Oral Sci 18, 37 (2026). https://doi.org/10.1038/s41368-026-00432-9
Trefwoorden: temporomandibulaire gewrichtspijn, darmmicrobioom, butyraat, epigenetische regulatie, single-cell sequencing