Clear Sky Science · pt
Sequenciamento single-cell multi-ômico revela perfis específicos por célula de transcriptoma e acessibilidade de cromatina na modulação da dor produzida pelo butirato, metabólito do microbioma intestinal
Por que seu intestino pode importar para a dor no maxilar
Pessoas com transtornos da articulação temporomandibular (ATM) frequentemente convivem com dor persistente no maxilar que dificulta falar, comer e dormir. Muitos tratamentos atuais oferecem apenas alívio parcial ou temporário e podem ter efeitos colaterais, especialmente quando dependem de analgésicos como opioides. Este estudo explora um aliado inesperado na busca por terapias mais seguras: pequenas moléculas produzidas por bactérias intestinais. Ao investigar em profundidade células individuais do sistema nervoso, os pesquisadores mostram como uma substância derivada do intestino chamada butirato pode reduzir a dor da ATM e apontar caminhos para tratamentos não opioides no futuro.
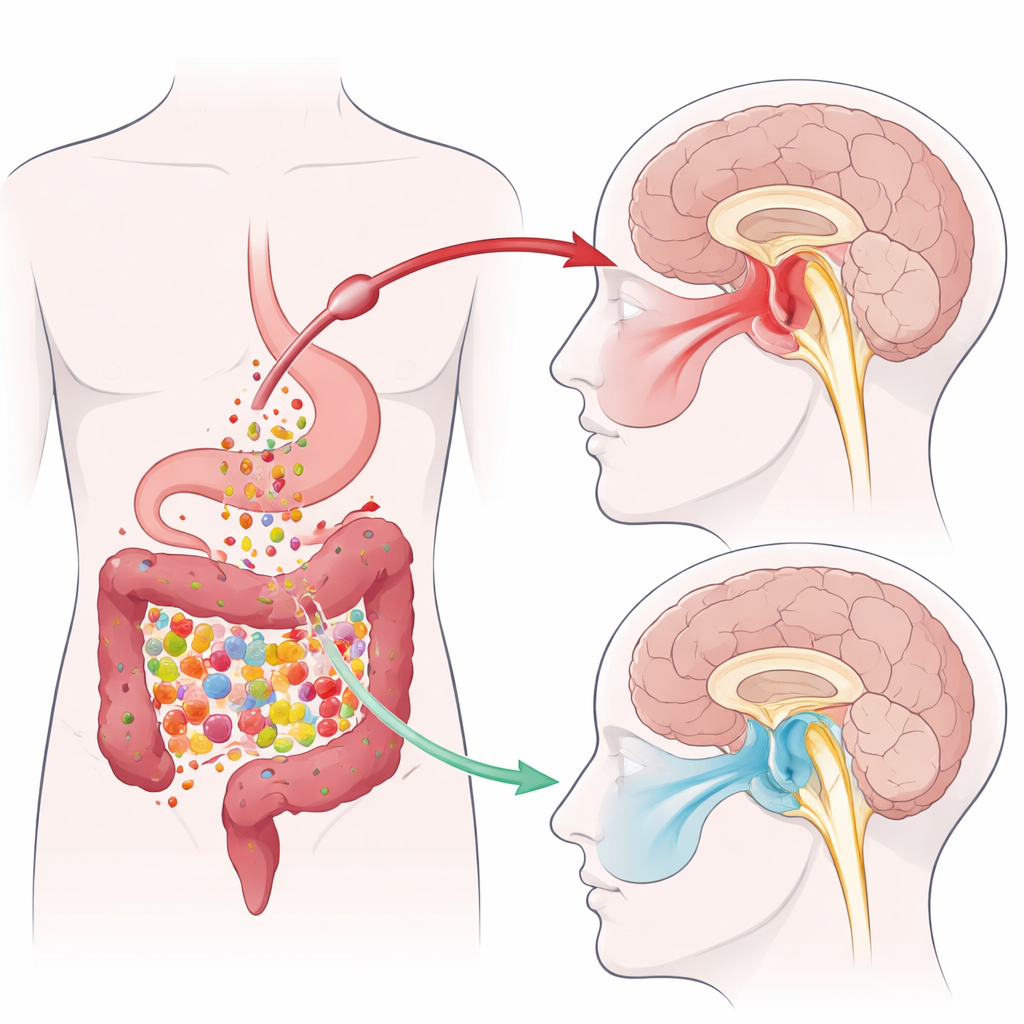
Das bactérias intestinais ao alívio da dor no maxilar
A equipe utilizou um modelo murino de dor inflamatória da ATM criado pela injeção de um irritante na articulação mandibular. Esse procedimento deixou os animais mais sensíveis ao toque no lado da face conectado à articulação lesionada. Trabalhos anteriores do mesmo grupo mostraram que a inflamação da ATM reduz os níveis de ácidos graxos de cadeia curta produzidos pelos micróbios intestinais, especialmente o butirato. Neste estudo, os cientistas administraram por via oral tributirina — um composto estável que se transforma em butirato no intestino — durante 10 dias. Esse tratamento aumentou os limiares de dor dos animais no lado afetado da face, ou seja, eles reagiram menos a estímulos mecânicos, enquanto o lado oposto permaneceu inalterado. Medições de fezes, sangue e de uma região do tronco encefálico chamada núcleo trigêmeo caudal (Sp5C) mostraram que a inflamação da ATM reduziu o butirato por todo o corpo — e que a tributirina o restaurou ao normal.
Mapeando a porta de entrada da dor no tronco encefálico
O Sp5C atua como uma estação de retransmissão chave para a dor facial, incluindo sinais vindos da ATM. Para entender o que ocorre ali durante a dor e a recuperação, os pesquisadores usaram uma abordagem poderosa de “multi-ômica single-cell”. Eles isolaram núcleos do tecido do Sp5C e, para cada célula individual, mediram tanto quais genes estavam ativados quanto quão acessível estava o DNA ao redor — um indicador de quão fácil é a ativação gênica. Isso permitiu identificar 12 tipos celulares distintos, incluindo vários tipos de neurônios, células imunes e células de suporte chamadas glia, e observar como cada um respondeu à inflamação da ATM e à tributirina. Curiosamente, a composição geral de tipos celulares não mudou muito; em vez disso, a dor e o tratamento alteraram principalmente como as células existentes utilizavam seus genes.
Chaves regulatórias acionadas pela dor e reiniciadas pelo butirato
Ao comparar camundongos saudáveis, com dor de ATM e tratados com tributirina, a equipe identificou genes específicos cuja atividade foi consistentemente perturbada pela dor e então restaurada pelo butirato. Em vários grupos de neurônios e em células precursoras, destacaram cinco genes — Nop14, Matk, Idh3b, Ndst2 e Tomm6 — como atores centrais. A inflamação da ATM alterou tanto a atividade desses genes quanto a acessibilidade de regiões de DNA próximas, enquanto a tributirina reverteu essas mudanças. Os pesquisadores então focaram no Nop14 em uma classe de células chamadas neurônios neuropeptidérgicos, que apresentaram alterações particularmente fortes. Usaram análises adicionais para mapear como elementos de controle locais do DNA e proteínas regulatórias interagem para aumentar ou suprimir esse gene em condições de dor e após o tratamento.
Como a organização dos genes se conecta aos sinais de dor
Como o butirato é conhecido por influenciar o grau de enrolamento do DNA em torno das histonas, os pesquisadores também examinaram a acetilação das histonas, uma marca química associada a maior permissividade à atividade gênica. A inflamação da ATM reduziu a acetilação global das histonas no Sp5C, enquanto a tributirina a trouxe de volta em direção ao normal. Ao mesmo tempo, uma região específica próxima ao gene Nop14 tornou-se mais acessível e mais acetilada durante a dor, consistente com aumento da atividade gênica. Quando a equipe usou um método viral para reduzir diretamente os níveis de Nop14 no Sp5C, observaram dois efeitos: a acetilação das histonas nessa região retornou em direção ao baseline, e as respostas de dor da ATM nos animais diminuíram. Isso sugere que Nop14 ocupa uma junção crucial onde mudanças na embalagem dos genes, desencadeadas pela perda ou restauração do butirato, podem amplificar ou acalmar os caminhos da dor.
Um novo caminho para terapias analgésicas não opioides
De modo geral, o estudo conecta o butirato derivado do intestino ao alívio da dor na ATM por meio de mudanças precisas e específicas por célula na regulação gênica dentro de um centro de dor do tronco encefálico. Em vez de simplesmente anestesiar os sinais de dor, a tributirina parece corrigir desequilíbrios moleculares que a inflamação da ATM cria em neurônios e células de suporte específicos, com Nop14 emergindo como um alvo promissor. Para pacientes, esse trabalho ainda não se traduz em uma terapia imediata, mas apoia a ideia de que manipular metabólitos intestinais — ou direcionar diretamente os mesmos interruptores gênicos que eles controlam — poderia oferecer no futuro tratamentos não opioides para transtornos da ATM e possivelmente outras formas de dor inflamatória crônica.
Citação: Tao, R., Liu, S., Crawford, J. et al. Single-cell multi-omics sequencing reveals cell-specific transcriptomic and chromatin accessibility profiles in gut microbiome metabolite butyrate-produced pain modulation. Int J Oral Sci 18, 37 (2026). https://doi.org/10.1038/s41368-026-00432-9
Palavras-chave: dor na articulação temporomandibular, microbioma intestinal, butirato, regulação epigenética, sequenciamento single-cell