Clear Sky Science · pl
Sekwencjonowanie multi-omiczne pojedynczych komórek ujawnia komórkowo-swoiste profile transkryptomiczne i dostępności chromatyny w modulacji bólu produkowanej przez metabolit mikrobiomu jelitowego — butyrat
Dlaczego jelita mogą mieć znaczenie przy bólu szczęki
Osoby z zaburzeniami stawu skroniowo-żuchwowego (TMJ) często zmagają się z uporczywym bólem szczęki, który utrudnia mówienie, jedzenie i spanie. Wiele dostępnych terapii przynosi tylko częściową lub czasową ulgę i może wiązać się z działaniami niepożądanymi, zwłaszcza gdy opiera się na lekach przeciwbólowych, takich jak opioidy. W tym badaniu przyjrzano się niespodziewanemu sprzymierzeńcowi w poszukiwaniu bezpieczniejszych terapii: małym cząsteczkom wytwarzanym przez bakterie jelitowe. Analiza pojedynczych komórek mózgu pokazuje, jak substancja pochodząca z jelit, butyrat, może osłabić ból TMJ i wskazać kierunki dla przyszłych, nieopioidowych terapii.
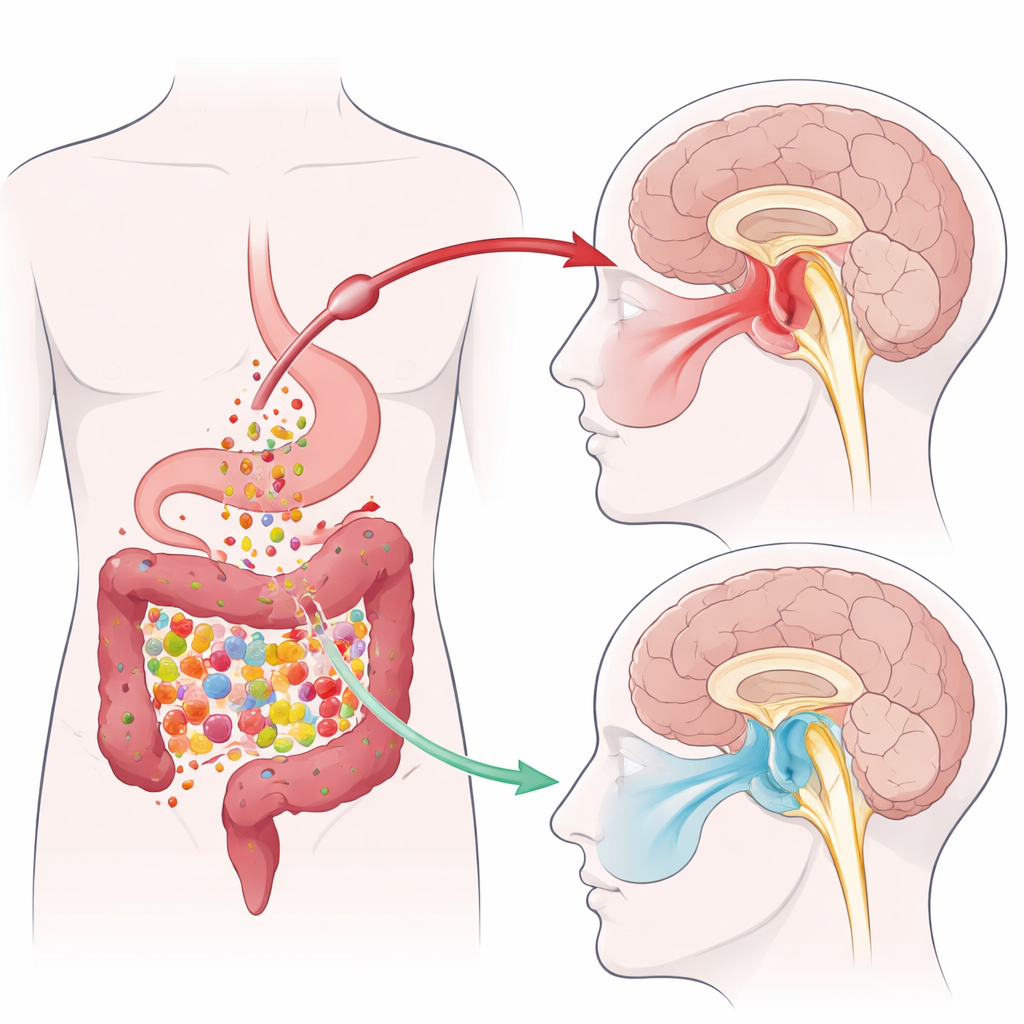
Od bakterii jelitowych do ulgi w bólu szczęki
Zespół użył modelu mysiego zapalnego bólu TMJ, wywołanego wstrzyknięciem drażniącej substancji do stawu szczękowego. Procedura spowodowała zwiększoną wrażliwość na dotyk po stronie twarzy powiązanej z uszkodzonym stawem. Wcześniejsze prace tej grupy wykazały, że zapalenie TMJ obniża poziomy krótkołańcuchowych kwasów tłuszczowych produkowanych przez mikroby jelitowe, w szczególności butyratu. W tym badaniu naukowcy podawali myszom doustnie tributyrynę — stabilny związek, który w jelicie rozkłada się do butyratu — przez 10 dni. Leczenie to podniosło progi bólowe po stronie twarzy objętej zmianą, czyli zwierzęta słabiej reagowały na stymulację mechaniczną, przy zachowaniu niezmienionych reakcji po przeciwnej stronie. Pomiary kału, krwi oraz obszaru mózgu zwanego jądrem rdzeniowym trójdzielnym (Sp5C) wykazały, że zapalenie TMJ zmniejszało poziom butyratu w całym organizmie — a tributyryna przywracała go do normy.
Mapowanie bramy bólu w pniu mózgu
Sp5C pełni rolę kluczowej stacji przekaźnikowej dla bólu twarzy, w tym sygnałów z TMJ. Aby zrozumieć, co tam się dzieje podczas bólu i rekonwalescencji, badacze zastosowali potężne podejście „multi-omics pojedynczych komórek”. Wyizolowali jądra z tkanki Sp5C i dla każdej pojedynczej komórki zmierzyli zarówno aktywność genów, jak i dostępność otaczającego DNA — wskaźnik tego, jak łatwo geny mogą zostać uaktywnione. Pozwoliło to zidentyfikować 12 odrębnych typów komórek, w tym kilka rodzajów neuronów, komórek odpornościowych i komórek wspierających zwanych glejem, oraz zobaczyć, jak każda z nich reagowała na zapalenie TMJ i na tributyrynę. Co ciekawe, ogólny skład typów komórek nie zmienił się znacząco; zamiast tego ból i leczenie głównie modyfikowały sposób, w jaki istniejące komórki korzystają ze swoich genów.
Kluczowe przełączniki uruchamiane przez ból i przywracane przez butyrat
Porównując myszy zdrowe, z bólem TMJ i leczone tributyryną, zespół wyodrębnił konkretne geny, których aktywność była konsekwentnie zaburzona przez ból, a następnie przywracana przez butyrat. W kilku grupach neuronów i komórkach prekursorowych wyróżniono pięć genów — Nop14, Matk, Idh3b, Ndst2 i Tomm6 — jako kluczowych uczestników. Zapalenie TMJ zmieniało zarówno aktywność tych genów, jak i dostępność pobliskich regionów DNA, natomiast tributyryna odwracała te zmiany. Badacze przyjrzeli się następnie bliżej Nop14 w klasie komórek nazywanych neuronami neuropeptydowymi, które wykazywały szczególnie silne zmiany. Wykorzystali dodatkowe analizy, by odwzorować, jak lokalne elementy kontrolne DNA i białka regulatorowe współdziałają, by wzmacniać lub tłumić ten gen w warunkach bólu i po leczeniu.
Jak upakowanie genów łączy się z sygnałami bólowymi
Ponieważ wiadomo, że butyrat wpływa na stopień, w jakim DNA owinięte jest wokół białek histonowych, badacze zbadali również acetylację histonów — chemiczny znak powiązany z bardziej podatną na aktywację aktywnością genów. Zapalenie TMJ obniżało ogólny poziom acetylacji histonów w Sp5C, natomiast tributyryna przywracała go w kierunku wartości prawidłowych. Jednocześnie specyficzny rejon w pobliżu genu Nop14 stawał się bardziej otwarty i bardziej acetylowany podczas bólu, co jest spójne ze zwiększoną aktywnością tego genu. Gdy zespół zastosował metodę opartą na wirusach, by bezpośrednio obniżyć poziom Nop14 w Sp5C, zaobserwował dwa efekty: acetylacja histonów w tym rejonie wróciła w kierunku wartości wyjściowej, a reakcje zwierząt na ból TMJ zmniejszyły się. Sugeruje to, że Nop14 znajduje się w kluczowym węźle, gdzie zmiany w upakowaniu genów, wywołane utratą lub przywróceniem butyratu, mogą wzmacniać lub łagodzić ścieżki bólowe.
Nowa ścieżka ku nieopioidowym terapiom przeciwbólowym
Podsumowując, badanie łączy butyrat pochodzący z jelit z ulgą w bólu TMJ poprzez precyzyjne, komórkowo-swoiste zmiany w regulacji genów w obrębie ośrodka bólu w pniu mózgu. Zamiast jedynie tłumić sygnały bólowe, tributyryna wydaje się korygować molekularne zaburzenia, które zapalenie TMJ wywołuje w konkretnych neuronach i komórkach wspierających, przy czym Nop14 wyłania się jako obiecujący cel. Dla pacjentów praca ta nie przekłada się jeszcze na natychmiastową terapię, ale wspiera pomysł, że manipulowanie metabolitami jelitowymi — lub bezpośrednie celowanie w te same przełączniki genowe, które one regulują — może w przyszłości oferować nieopioidowe terapie dla zaburzeń TMJ i prawdopodobnie innych postaci przewlekłego bólu zapalnego.
Cytowanie: Tao, R., Liu, S., Crawford, J. et al. Single-cell multi-omics sequencing reveals cell-specific transcriptomic and chromatin accessibility profiles in gut microbiome metabolite butyrate-produced pain modulation. Int J Oral Sci 18, 37 (2026). https://doi.org/10.1038/s41368-026-00432-9
Słowa kluczowe: ból stawu skroniowo-żuchwowego, mikrobiom jelitowy, butyrat, regulacja epigenetyczna, sekwencjonowanie pojedynczych komórek