Clear Sky Science · ar
تسلسل متعدد الأومكس على مستوى الخلية الواحدة يكشف ملفات نسخ وجينومية محددة للخلايا في تعديل الألم الناجم عن البيوتيرات المنتج من ميكروبيوم الأمعاء
لماذا قد يكون لأمعائك دور في ألم الفك
غالبًا ما يعاني الأشخاص المصابون باضطرابات المفصل الصدغي الفكي (TMJ) من ألم عنيد في الفك يعيق الكلام والأكل والنوم. كثير من العلاجات الحالية تقدم راحة جزئية أو مؤقتة فقط وقد تصاحبها آثار جانبية، خاصة عند الاعتماد على مسكنات الألم مثل الأفيونات. تستكشف هذه الدراسة متعاونًا غير متوقع في البحث عن علاجات أكثر أمانًا: جزيئات صغيرة تصنعها بكتيريا الأمعاء. من خلال النظر بعمق داخل خلايا دماغية مفردة، يوضح الباحثون كيف يمكن لمادة مشتقة من الأمعاء تُسمى البيوتيرات أن تُخفض ألم TMJ وتوجه نحو علاجات مستقبلية غير أفيونية.
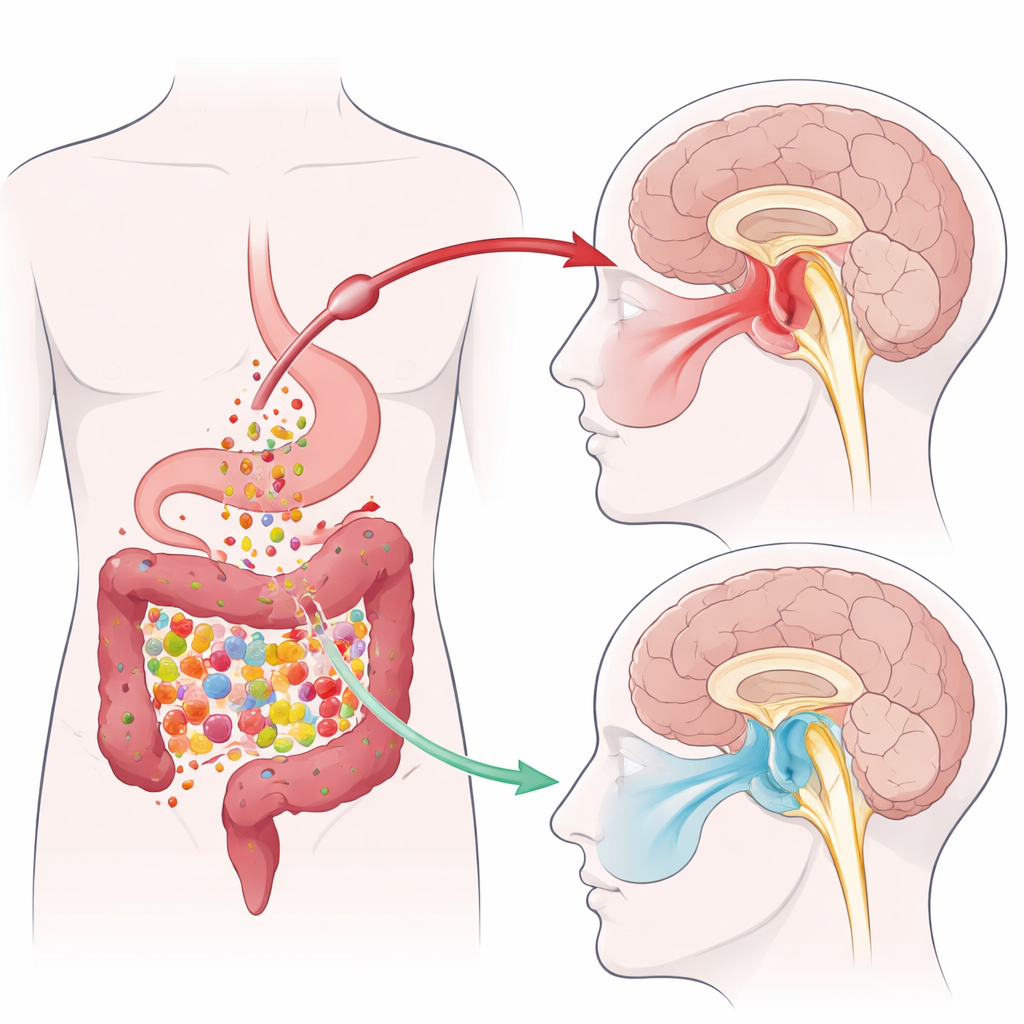
من بكتيريا الأمعاء إلى تخفيف ألم الفك
استخدم الفريق نموذجًا فأريًا لألم TMJ الالتهابي تم إنشاؤه بحقن مادة مهيجة في مفصل الفك. جعل هذا الإجراء الحيوانات أكثر حساسية للمس على جانب الوجه المتصل بالمفصل المصاب. أظهرت أعمال سابقة من نفس المجموعة أن التهاب TMJ يخفض مستويات الأحماض الدهنية قصيرة السلسلة المنتجة بواسطة ميكروبات الأمعاء، وخصوصًا البيوتيرات. في هذه الدراسة، أعطى العلماء للفئران تريبيوتيرين، وهو مركب مستقر يتحلل إلى بيوتيرات في الأمعاء، عن طريق الفم لمدة 10 أيام. رفعت هذه المعالجة عتبات الألم لدى الحيوانات على الجانب المتأثر من الوجه، مما يعني أنها تفاعلت بشكل أقل مع التحفيز الميكانيكي، بينما تركت الجانب المقابل دون تغيير. أظهرت قياسات البراز والدم ومنطقة في جذع الدماغ تسمى النواة الثلاثية الشوكية الذيلية (Sp5C) أن التهاب TMJ خفض مستوى البيوتيرات في أنحاء الجسم—وأن التريبيوتيرين أعاده إلى الطبيعي.
رسم خريطة بوابة الألم في جذع الدماغ
تعمل Sp5C كمحطة رئيسية لتمرير إشارات ألم الوجه، بما في ذلك الإشارات من TMJ. لفهم ما يحدث هناك أثناء الألم والتعافي، استخدم الباحثون نهجًا قويًا «متعدد الأومكس على مستوى الخلية الواحدة». عزلوا النوى من نسيج Sp5C، ولكل خلية مفردة قاسوا أي الجينات معبّرة ومدى انفتاح الحمض النووي المحيط—وهو علامة على سهولة تفعيل الجينات. أتاح لهم ذلك تحديد 12 نوعًا خلويًا مميزًا، بما في ذلك عدة أنواع من الخلايا العصبية والخلايا المناعية وخلايا داعمة تسمى الدبق، ورؤية كيف استجاب كل نوع لالتهاب TMJ والتريبيوتيرين. ومن المثير أن التركيبة العامة لأنواع الخلايا لم تتغير كثيرًا؛ بل غيّرت الحالة المؤلمة والعلاج بشكل أساسي كيفية استخدام الخلايا الموجودة للجينات الخاصة بها.
مفاتيح تشغيل رئيسية يقلبها الألم ويعيد ضبطها البيوتيرات
بمقارنة فئران سليمة وفئران مصابة بألم TMJ وفئران عولجت بالتريبيوتيرين، حدّد الفريق جينات معينة تغير نشاطها باستمرار بفعل الألم ثم أعاد البيوتيرات ضبطها. عبر عدة مجموعات من الخلايا العصبية والخلايا السلفية، أبرَزوا خمسة جينات—Nop14 وMatk وIdh3b وNdst2 وTomm6—كمكوّنات مركزية. غيّر التهاب TMJ كلًا من نشاط هذه الجينات وانفتاح مناطق الحمض النووي المجاورة، بينما عكس التريبيوتيرين هذه التحولات. ثم ركز الباحثون على Nop14 في فئة من الخلايا تُسمى الخلايا العصبية الببتيدية، التي أظهرت تغيّرات قوية بشكل خاص. استخدموا تحليلات إضافية لرسم كيفية تفاعل عناصر التحكم المحلية في الحمض النووي والبروتينات المنظِمة لتعزيز أو قمع هذا الجين أثناء الألم وبعد العلاج.
كيف يربط تغليف الجينات بإشارات الألم
نظرًا لأن البيوتيرات معروف بتأثيره على مدى إحكام لف الحمض النووي حول بروتينات التاريخون، فحص الباحثون أيضًا أسيتلة الهستون، وهي وسم كيميائي مرتبط بنشاط جيني أكثر سماحًا. خفض التهاب TMJ إجمالي أسيتلة الهستون في Sp5C، بينما أعاد التريبيوتيرين هذا المؤشر نحو الطبيعي. في الوقت نفسه، أصبحت منطقة محددة قريبة من جين Nop14 أكثر انفتاحًا وأكثر أسيتلة خلال الألم، وهو ما يتوافق مع زيادة نشاط الجين. عندما استخدم الفريق طريقة معتمدة على فيروسات لتقليل مستويات Nop14 مباشرة في Sp5C، لاحظوا تأثيرين: عادت أسيتلة الهستون في هذه المنطقة نحو الخط الأساسي، وانخفضت استجابات الحيوانات لألم TMJ. وهذا يشير إلى أن Nop14 يقع في مفترق حاسم حيث يمكن لتغيرات في تغليف الجينات، الناتجة عن فقدان أو استعادة البيوتيرات، أن تضخّم أو تهدئ مسارات الألم.
مسار جديد نحو علاجات غير أفيونية للألم
عمومًا، تربط الدراسة بين البيوتيرات المشتق من الأمعاء وتخفيف ألم TMJ عبر تغييرات دقيقة ومحددة على مستوى الخلية في تنظيم الجينات داخل محور ألم في جذع الدماغ. بدلاً من مجرد تخدير إشارات الألم، يبدو أن التريبيوتيرين يصحّح الاختلالات الجزيئية التي يسببها التهاب TMJ في خلايا عصبية وداعمة معينة، مع بروز Nop14 كهدف واعد. بالنسبة للمرضى، لا تُترجم هذه النتائج بعد إلى علاج فوري، لكنها تدعم فكرة أن تعديل مستويات نواتج التمثيل الغذائي المعوية—أو استهداف مفاتيح الجينات نفسها التي تتحكم بها—قد يقدم علاجات مستقبلية غير أفيونية لاضطرابات TMJ وربما لأشكال أخرى من الألم الالتهابي المزمن.
الاستشهاد: Tao, R., Liu, S., Crawford, J. et al. Single-cell multi-omics sequencing reveals cell-specific transcriptomic and chromatin accessibility profiles in gut microbiome metabolite butyrate-produced pain modulation. Int J Oral Sci 18, 37 (2026). https://doi.org/10.1038/s41368-026-00432-9
الكلمات المفتاحية: ألم المفصل الصدغي الفكي, ميكروبيوم الأمعاء, البيوتيرات, التنظيم فوق الجيني, تسلسل خلية واحدة