Clear Sky Science · ru
Секвенирование мультиомики отдельных клеток выявляет клеточно‑специфические транскриптомные и профили доступности хроматина в модуляции боли, вызванной бутиратом, произведённым микробиотой кишечника
Почему ваш кишечник может влиять на боль в челюсти
Люди с нарушениями височно‑нижнечелюстного сустава (ВНЧС) часто страдают от упорной боли в челюсти, которая затрудняет разговор, приём пищи и сон. Многие существующие методы лечения дают лишь частичное или временное облегчение и могут иметь побочные эффекты, особенно при использовании обезболивающих, таких как опиоиды. В этом исследовании изучается неожиданный союзник в поиске безопасных терапий: крошечные молекулы, производимые кишечными бактериями. Глубоко изучив отдельные клетки мозга, учёные показали, как вещество, происходящее из кишечника и называемое бутиратом, может ослаблять боль при ВНЧС и указывать путь к будущим безопиоидным методам лечения.
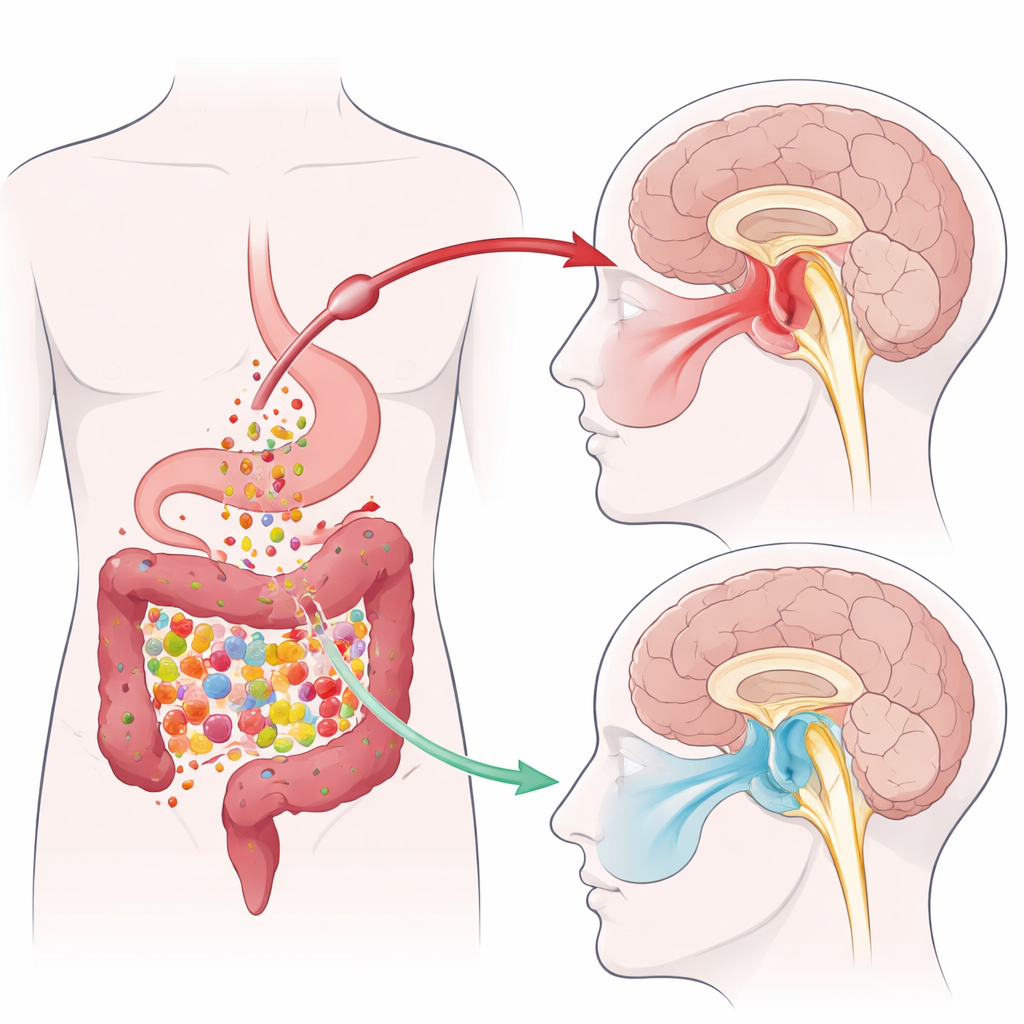
От кишечных бактерий к облегчению боли в челюсти
Команда использовала модель мышей с воспалительной болью ВНЧС, полученную путем введения раздражителя в сустав челюсти. Эта процедура делала животных более чувствительными к прикосновению на той стороне лица, которая связана с поражённым суставом. Ранее та же группа показала, что воспаление ВНЧС снижает уровни короткоцепочечных жирных кислот, производимых кишечными микробами, особенно бутирата. В этом исследовании учёные в течение 10 дней давали мышам трибутирин — стабильное соединение, которое в кишечнике распадается до бутирата — перорально. Лечение повышало болевой порог у животных на поражённой стороне лица, то есть они слабее реагировали на механическую стимуляцию, в то время как противоположная сторона оставалась без изменений. Измерения в фекалиях, крови и в участке ствола мозга, называемом хвостатым тройничным ядром (Sp5C), показали, что воспаление ВНЧС снижало уровень бутирата по всему организму — и что трибутирин восстанавливал его до нормы.
Картирование «ворот боли» в стволе мозга
Sp5C служит ключевой релейной станцией для лицевой боли, включая сигналы от ВНЧС. Чтобы понять, что там происходит при боли и восстановлении, исследователи использовали мощный подход «мультиомика отдельных клеток». Они выделили ядра из ткани Sp5C и для каждой отдельной клетки измеряли и то, какие гены активны, и насколько открыт окружающий их ДНК — признак того, насколько легко гены могут быть активированы. Это позволило им идентифицировать 12 различных типов клеток, включая несколько видов нейронов, иммунных клеток и поддерживающих глиальных клеток, и увидеть, как каждая из них реагировала на воспаление ВНЧС и на приём трибутирина. Любопытно, что общий состав типов клеток сильно не изменялся; вместо этого боль и лечение в основном меняли то, как существующие клетки используют свои гены.
Ключевые переключатели, включаемые болью и сбрасываемые бутиратом
Сравнивая здоровых мышей, животных с болью ВНЧС и животных, получавших трибутирин, команда выделила конкретные гены, активность которых последовательно нарушалась при боли и затем восстанавливалась бутиратом. В нескольких группах нейронов и в клетках‑предшественниках они выделили пять генов — Nop14, Matk, Idh3b, Ndst2 и Tomm6 — как центральные участники. Воспаление ВНЧС меняло как активность этих генов, так и открытость соседних регионов ДНК, в то время как трибутирин обращал эти сдвиги вспять. Исследователи затем подробно сосредоточились на Nop14 в классе клеток, называемых нейропептидными нейронами, которые проявляли особенно сильные изменения. Они использовали дополнительные анализы, чтобы картировать, как локальные элементы контроля ДНК и регуляторные белки взаимодействуют для усиления или подавления этого гена в условиях боли и после лечения.
Как упаковка генов связана с болевыми сигналами
Поскольку известно, что бутират влияет на то, насколько плотно ДНК обвивается вокруг гистонов, учёные также исследовали ацетилирование гистонов — химическую метку, связанную с более «разрешённой» активностью генов. Воспаление ВНЧС снижало общий уровень ацетилирования гистонов в Sp5C, тогда как трибутирин возвращал его к норме. Одновременно специфический участок рядом с геном Nop14 становился более открытым и сильнее ацетилировался во время боли, что согласуется с повышенной активностью гена. Когда команда использовала вирусный метод для снижения уровня Nop14 непосредственно в Sp5C, они наблюдали два эффекта: ацетилирование гистонов в этом регионе сместилось обратно к исходному уровню, и болевая реакция животных на ВНЧС уменьшилась. Это указывает на то, что Nop14 занимает важный узловой пункт, где изменения упаковки генов, вызванные потерей или восстановлением бутирата, могут усиливать или успокаивать болевые пути.
Новый путь к безопиоидным методам лечения боли
В целом исследование связывает кишечный бутират с облегчением боли при ВНЧС через точечные, клеточно‑специфические изменения регуляции генов в болевом узле ствола мозга. Вместо простого притупления болевых сигналов, трибутирин по‑видимому корректирует молекулярные дисбалансы, которые создаёт воспаление ВНЧС в отдельных нейронах и поддерживающих клетках, а Nop14 выступает многообещающей мишенью. Для пациентов эта работа ещё не переводится в немедленную терапию, но она поддерживает идею о том, что манипуляция кишечными метаболитами — или прямое воздействие на те же генетические переключатели, которые они контролируют — может предложить будущие безопиоидные методы лечения нарушений ВНЧС и, возможно, других форм хронической воспалительной боли.
Цитирование: Tao, R., Liu, S., Crawford, J. et al. Single-cell multi-omics sequencing reveals cell-specific transcriptomic and chromatin accessibility profiles in gut microbiome metabolite butyrate-produced pain modulation. Int J Oral Sci 18, 37 (2026). https://doi.org/10.1038/s41368-026-00432-9
Ключевые слова: височно-нижнечелюстной сустав болевые синдромы, микробиота кишечника, бутират, эпигенетическая регуляция, секвенирование отдельных клеток