Clear Sky Science · sv
VAP1 främjar hjärtfibros genom att möjliggöra PDGFR‑signalering i myofibroblaster
Varför ärrbildning i hjärtat spelar roll
Hjärtinsufficiens drabbar miljontals människor och utvecklas ofta när hjärtat gradvis fylls med stel ärrvävnad. Denna ärrbildningsprocess, kallad fibros, gör det svårare för hjärtat att slappna av och pumpa blod. Studien bakom denna artikel undersöker hur vissa stödceller i hjärtat omvandlas till aggressiva ärrbildande celler och identifierar ett ytligt molekylärt protein, VAP1, som hjälper till att driva denna förvandling. Att förstå denna omkoppling öppnar möjligheter att sakta ner eller till och med vända skadlig ärrbildning vid hjärtsjukdom.
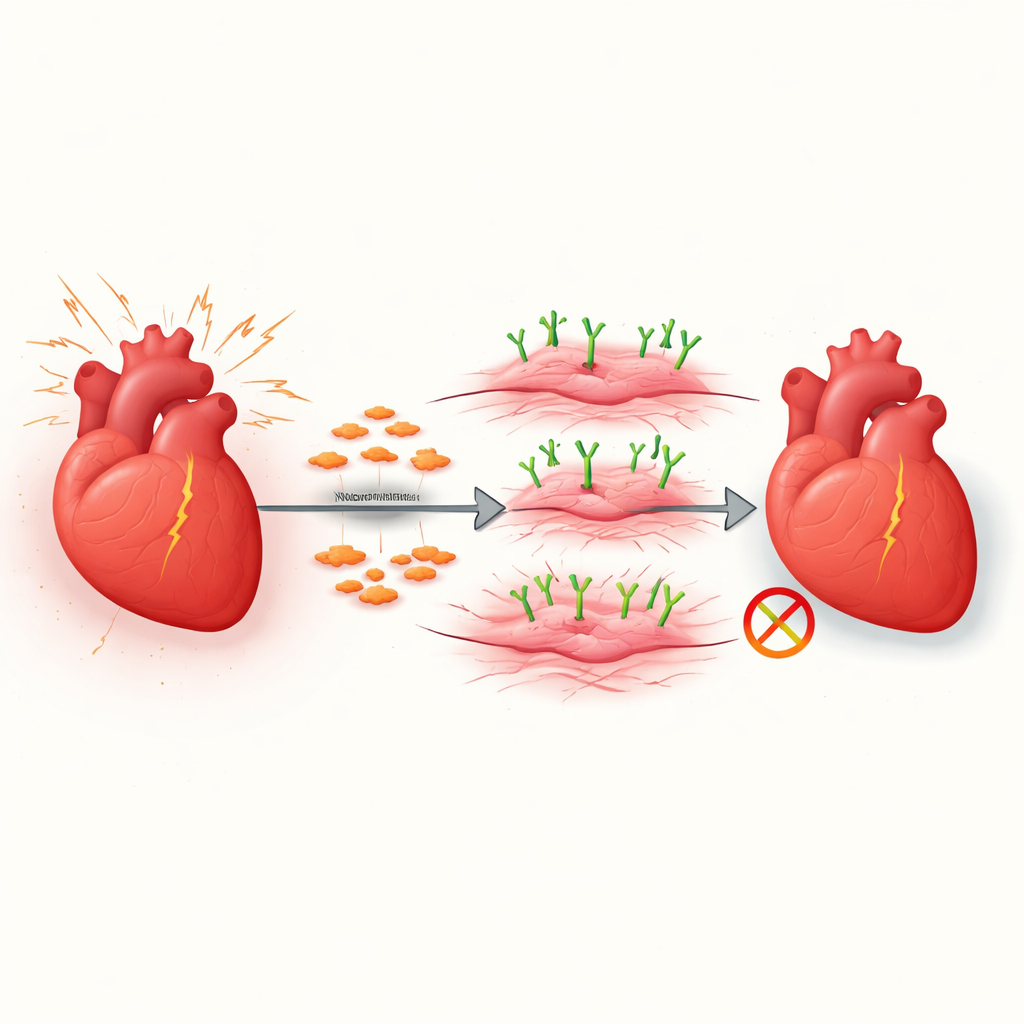
Från tysta hjälpare till överaktiva byggare
Det friska hjärtat innehåller många fibroblaster, tysta stödceller som upprätthåller vävnadens struktur. När hjärtat skadas eller utsätts för långvarigt tryck omvandlas en del av dessa fibroblaster till myofibroblaster, som är mycket aktiva byggherrar av ärrvävnad. I korta omgångar kan detta svar vara skyddande, men när det fortsätter okontrollerat fyller det hjärtmuskelfibernas vägg med tuffa fibrer som begränsar dess rörelse. Forskarna fokuserade på hur skiftet från fibroblast till myofibroblast styrs, särskilt i en vanlig modell för trycköverbelastning som efterliknar former av mänsklig hjärtsvikt.
En ytportvakt kallad VAP1
Genom storskaliga analyser av genaktivitet fann teamet att ett ytprotein, VAP1, ökade kraftigt när en huvudregulator för ärrbildning, proteinet MKL1, aktiverades. VAP1 är i andra sammanhang känt för att hjälpa vita blodkroppar att fästa vid blodkärl, men dess roll i hjärtat var tidigare otydlig. I hjärtfibroblaster odlade i laboratoriet minskade nedreglering av VAP1 kännetecken för myofibroblaster, såsom celltillväxt, rörlighet och förmåga att kontrahera och dra i sin omgivning. Ökad VAP1 gav motsatt effekt och drev fibroblasterna tydligare mot det aktiva, ärrbildande tillståndet.
Test av VAP1 i levande hjärtan
För att se hur VAP1 beter sig i en hel organism konstruerade forskarna möss där VAP1 kunde tas bort enbart i hjärtfibroblaster. När dessa möss utsattes för långvarigt tryck på huvudartären ut ur hjärtat utvecklade de betydligt mindre fibrös ärrbildning än normala möss, trots att den totala hjärtutvidgningen var likartad. Mätningar av hjärtats pumpfunktion bevarades också bättre. Att ta bort VAP1 specifikt från redan aktiverade myofibroblaster gav en liknande minskning av ärrvävnad och förbättring av funktionen, vilket visar att VAP1 är viktigt både när fibroblasterna aktiveras och när de förblir aktiva.
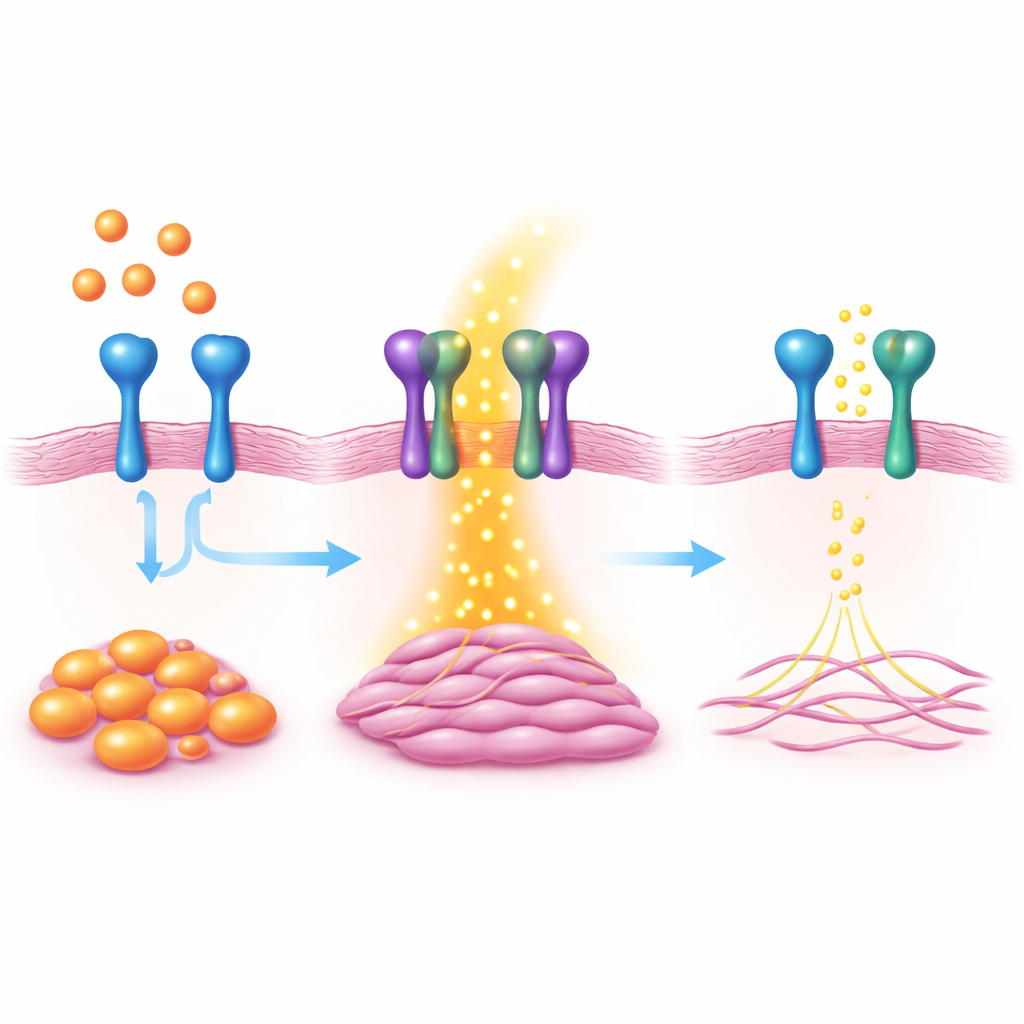
Hur VAP1 förstärker pro‑ärrsignaler
För att utröna hur VAP1 fungerar kombinerade teamet genaktivitetsanalyser med proteinstudier. De upptäckte att VAP1 fysiskt interagerar med ett annat ytprotein, PDGFRβ, en receptor som känner av tillväxtsignaler kända för att utlösa fibros. När VAP1 saknades blev PDGFRβ mindre aktiv och en rad nedströms signalvägar som uppmuntrar celltillväxt, rörlighet och kollagenproduktion försvagades. En del av VAP1‑proteinet som sitter utanför cellmembranet var tillräcklig för att återställa den förlorade signalen när den tillsattes, vilket tyder på att det fysiska samarbetet mellan VAP1 och PDGFRβ på cellytan är avgörande.
Blockera VAP1 med en liten molekyl
Eftersom VAP1 också fungerar som ett enzym testade forskarna en läkemedelsliknande förening som blockerar dess aktivitet. I hjärtfibroblaster i petriskålar minskade denna hämmare myofibroblastmarkörer och dämpade deras förmåga att dela sig, migrera och kontrahera. När föreningen gavs till möss med trycköverbelastning hindrade den inte hjärtat från att växa, men den minskade markant ärrbildningen och förbättrade mått på hjärtats pumpfunktion. Dessa resultat tyder på att farmakologisk blockering av VAP1 kan dämpa ärrbildningssvaret utan att rubba alla aspekter av hjärtats anpassning till stress.
Vad detta betyder för personer med hjärtsvikt
Tillsammans visar fynden att VAP1 fungerar som en avgörande hjälpare för signaler som driver hjärtats stödceller in i ett stelt, ärrbildande tillstånd. Genom att nedtona VAP1, antingen genetiskt i fibroblaster eller med en hämmare, utvecklar hjärtat mindre stel kollagen och bibehåller bättre funktion under stress. Även om mer arbete krävs i ytterligare djurmodeller och mänsklig vävnad positionerar studien VAP1 som ett lovande mål för framtida terapier som syftar till att begränsa skadlig hjärtfibros och lindra bördan av hjärtsvikt.
Citering: Huang, S., Zhao, Q., Shao, T. et al. VAP1 promotes cardiac fibrosis by enabling PDGFR signaling in myofibroblasts. Exp Mol Med 58, 1284–1296 (2026). https://doi.org/10.1038/s12276-026-01690-7
Nyckelord: hjärtfibros, hjärtinsufficiens, fibroblaster, VAP1, PDGFR‑signalering