Clear Sky Science · ar
يحفّز VAP1 تليّف القلب من خلال تمكين إشارة PDGFR في الميوفيبروبلاست
لماذا يهم تندّب القلب
يؤثر فشل القلب على ملايين الأشخاص وغالباً ما يتطوّر مع تراكم تدريجي لأنسجة ندبية جامدة في القلب. تُسمى هذه العملية بالتليّف، وهي تجعل من الصعب على القلب أن يرتخِي ويضخ الدم. تستقصي الدراسة خلف هذا المقال كيف تتحول خلايا دعم معيّنة في القلب إلى خلايا ميوفيبروبلاست نشطة في تشكيل الندوب، وتحدد جزيئاً سطحياً، VAP1، يساهم في دفع هذا التحوّل. فهم هذا التحوّل يفتح الباب أمام استراتيجيات جديدة لإبطاء أو حتى عكس التندّب الضار في أمراض القلب. 
من مساعدين هادئين إلى بنّائين مفرطين
يحتوي القلب السليم على العديد من الخلايا الليفية، وهي خلايا دعم هادئة تحافظ على بنية النسيج. عندما يتعرض القلب لإصابة أو لضغط طويل الأمد، يتحوّل بعض هذه الخلايا الليفية إلى ميوفيبروبلاست، وهي خلايا بنّاءة نشطة للغاية تشكّل نسيج الندبة. في طفرات قصيرة قد يكون هذا التفاعل حمائياً، لكن عندما يستمر دون رقابة يملأ جدار القلب بألياف قوية تحدّ من حركته. ركّز الباحثون على كيفية تنظيم هذا التحوّل من خلية ليفية إلى ميوفيبروبلاست، لا سيما في نموذج شائع لزيادة الضغط يحاكي أنماط فشل القلب البشري.
حارس سطحي يُدعى VAP1
باستخدام شاشات واسعة النطاق لنشاط الجينات، وجد الفريق أن بروتيناً سطحياً يُدعى VAP1 يزداد بشكل حاد عندما يُشغّل مفتاح رئيسي للتليّف، وهو البروتين MKL1. وVAP1 معروف بمساعدته خلايا الدم البيضاء على الالتصاق بالأوعية الدموية، لكن دوره داخل القلب لم يكن واضحاً. في خلايا ليفية قلبية مزروعة في المختبر، أدى إضعاف VAP1 إلى تقليل السمات المميزة للميوفيبروبلاست، مثل تكاثر الخلايا، وحركتها، وقدرتها على الانقباض وجذب محيطها. أما تعزيز VAP1 فكان له التأثير المعاكس، إذ دفع الخلايا الليفية نحو الحالة النشطة المكوّنة للندوب بشكل أقوى. 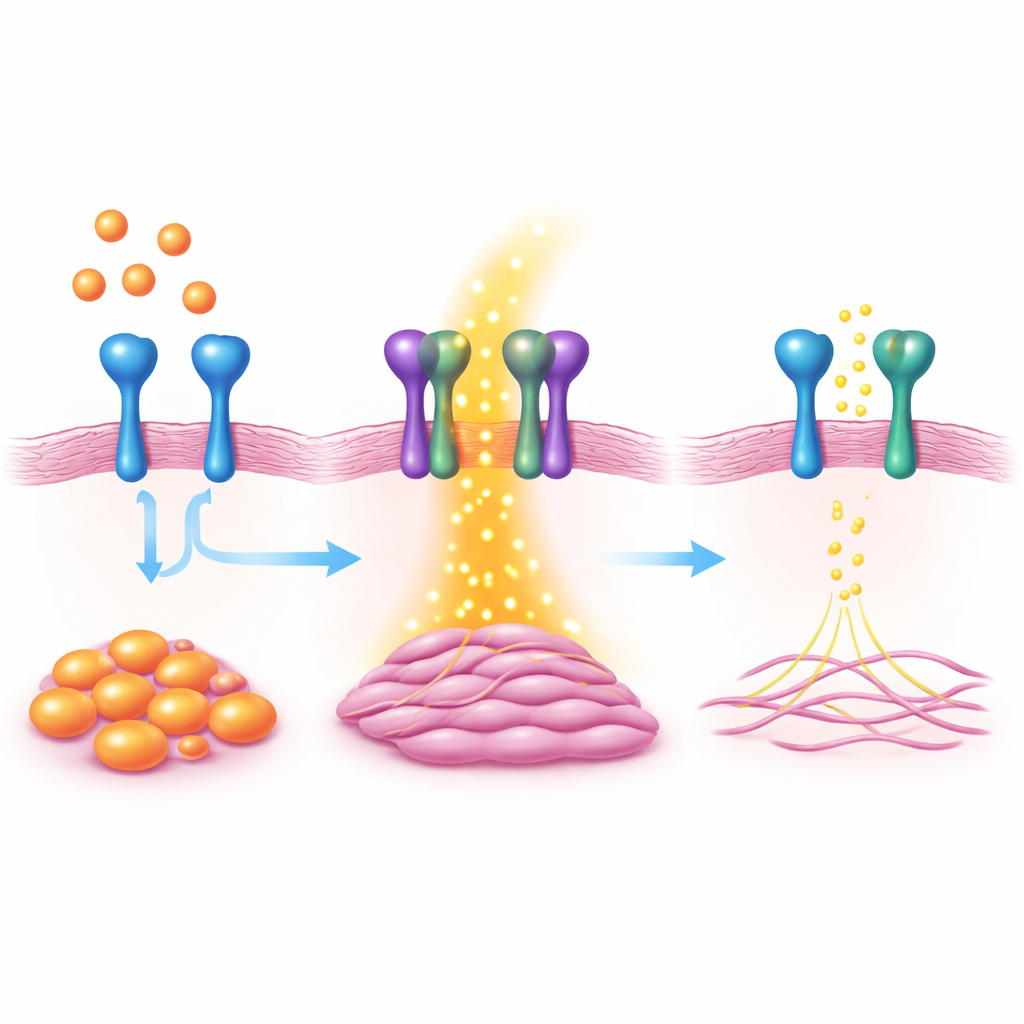
اختبار VAP1 في قلوب حية
لمعرفة كيف يتصرف VAP1 في كائن حي كامل، مهندَس العلماء فئراناً يمكن إزالة VAP1 منها فقط في الخلايا الليفية القلبية. عندما تعرّضت هذه الفئران لضغط طويل على الشريان الرئيسي الخارج من القلب، طوّرت ندباً ليفية أقل بكثير من الفئران الطبيعية، رغم أن تضخّم القلب العام كان مشابهاً. كما حافظت مقاييس وظيفة الضخ على أداء أفضل. وأدى إزالة VAP1 تحديداً من الميوفيبروبلاست المنشطة بالفعل إلى تقليل مماثل في التندّب وتحسن في الوظيفة، مما يبيّن أن VAP1 مهم سواء عند تحويل الخلايا الليفية أو أثناء بقائها نشطة.
كيف يعزّز VAP1 إشارات مؤيدة للندوب
لفكّ كيفية عمل VAP1، جمع الفريق تحليل نشاط الجينات مع مسوحات للبروتينات. اكتشفوا أن VAP1 يتفاعل جسدياً مع بروتين سطحي آخر يُدعى PDGFRβ، وهو مستقبل يستشعر إشارات نمو معروفة بإثارتها للتليّف. عندما غاب VAP1، أصبح PDGFRβ أقل نشاطاً وضعفت سلسلة من المسارات الإشارية اللاحقة التي تشجّع تكاثر الخلايا وحركتها وإنتاج الكولاجين. وكان جزء من بروتين VAP1 الموجود خارج غشاء الخلية كافياً لاستعادة هذه الإشارة المفقودة عندما أُعيد، مما يوحي أن الشراكة الفيزيائية بين VAP1 وPDGFRβ على سطح الخلية هي أمر محوري.
حجب VAP1 بجزيء صغير
لأن VAP1 يعمل أيضاً كإنزيم، اختبر الباحثون مركباً شبيهاً بدواء يحجب نشاطه. في الخلايا الليفية القلبية في الأطباق، قلّل هذا المانع علامات الميوفيبروبلاست وكبح قدرتها على الانقسام والهجرة والانقباض. وعند إعطائه لفئران تعاني من زيادة الضغط، لم يمنع المركب نمو القلب، لكنه خفّف بشكل ملحوظ من تراكم الندوب وحسّن مقاييس قدرة القلب على الضخ. تشير هذه النتائج إلى أن الحجب الدوائي لـ VAP1 يمكن أن يلين استجابة التليّف دون تعطيل كل جوانب تكيف القلب مع الضغط.
ماذا يعني هذا للناس المصابين بفشل القلب
تُظهر النتائج مجتمعة أن VAP1 يعمل كمساعد حاسم للإشارات التي تدفع خلايا الدعم القلبية إلى وضع جامد مكوّن للندوب. من خلال تخفيف نشاط VAP1، وراثياً في الخلايا الليفية أو باستخدام مثبط، ينتج القلب كمية أقل من الكولاجين الصلب ويحتفظ بوظيفة أفضل تحت الضغط. وبينما هناك حاجة لمزيد من العمل في نماذج حيوانية إضافية وأنسجة بشرية، تضع الدراسة VAP1 كهدف واعد لعلاجات مستقبلية تهدف إلى الحدّ من التليّف القلبي الضار وتخفيف عبء فشل القلب.
الاستشهاد: Huang, S., Zhao, Q., Shao, T. et al. VAP1 promotes cardiac fibrosis by enabling PDGFR signaling in myofibroblasts. Exp Mol Med 58, 1284–1296 (2026). https://doi.org/10.1038/s12276-026-01690-7
الكلمات المفتاحية: تليّف قلبي, فشل القلب, الخلايا الليفية, VAP1, إشارة PDGFR