Clear Sky Science · pt
VAP1 promove fibrose cardíaca ao permitir o sinal PDGFR em miofibroblastos
Por que a cicatrização do coração importa
A insuficiência cardíaca afeta milhões de pessoas e frequentemente se desenvolve à medida que o coração lentamente se enche de tecido cicatricial rígido. Esse processo de cicatrização, chamado fibrose, dificulta a capacidade do coração de relaxar e bombear sangue. O estudo por trás deste artigo investiga como certas células de suporte no coração se transformam em células agressivas formadoras de cicatriz e identifica uma molécula de superfície, VAP1, que ajuda a impulsionar essa mudança. Entender esse mecanismo abre caminho para novas formas de retardar ou mesmo reverter cicatrizes prejudiciais em doenças cardíacas. 
De ajudantes silenciosos a construtores hiperativos
O coração saudável contém muitos fibroblastos, células de suporte discretas que mantêm a estrutura do tecido. Quando o coração é lesionado ou submetido a pressão crônica, alguns desses fibroblastos se convertem em miofibroblastos, que são construtores de tecido cicatricial altamente ativos. Em respostas curtas, esse processo pode ser protetor, mas quando continua sem controle, preenche a parede cardíaca com fibras resistentes que limitam seu movimento. Os pesquisadores focaram em como essa transição de fibroblasto para miofibroblasto é controlada, especialmente em um modelo comum de sobrecarga de pressão que imita formas de insuficiência cardíaca humana.
Um porteiro de superfície chamado VAP1
Usando triagens abrangentes de atividade gênica, a equipe descobriu que uma proteína de superfície chamada VAP1 aumentou fortemente quando um interruptor mestre da cicatrização, a proteína MKL1, foi ativado. O VAP1 é conhecido por ajudar leucócitos a aderirem aos vasos sanguíneos, mas seu papel dentro do coração era incerto. Em fibroblastos cardíacos cultivados em laboratório, reduzir a expressão de VAP1 diminuiu características marcantes de miofibroblastos, como proliferação celular, migração e capacidade de contrair e puxar o ambiente. Aumentar VAP1 teve o efeito oposto, empurrando os fibroblastos mais fortemente para o estado ativo formador de cicatriz. 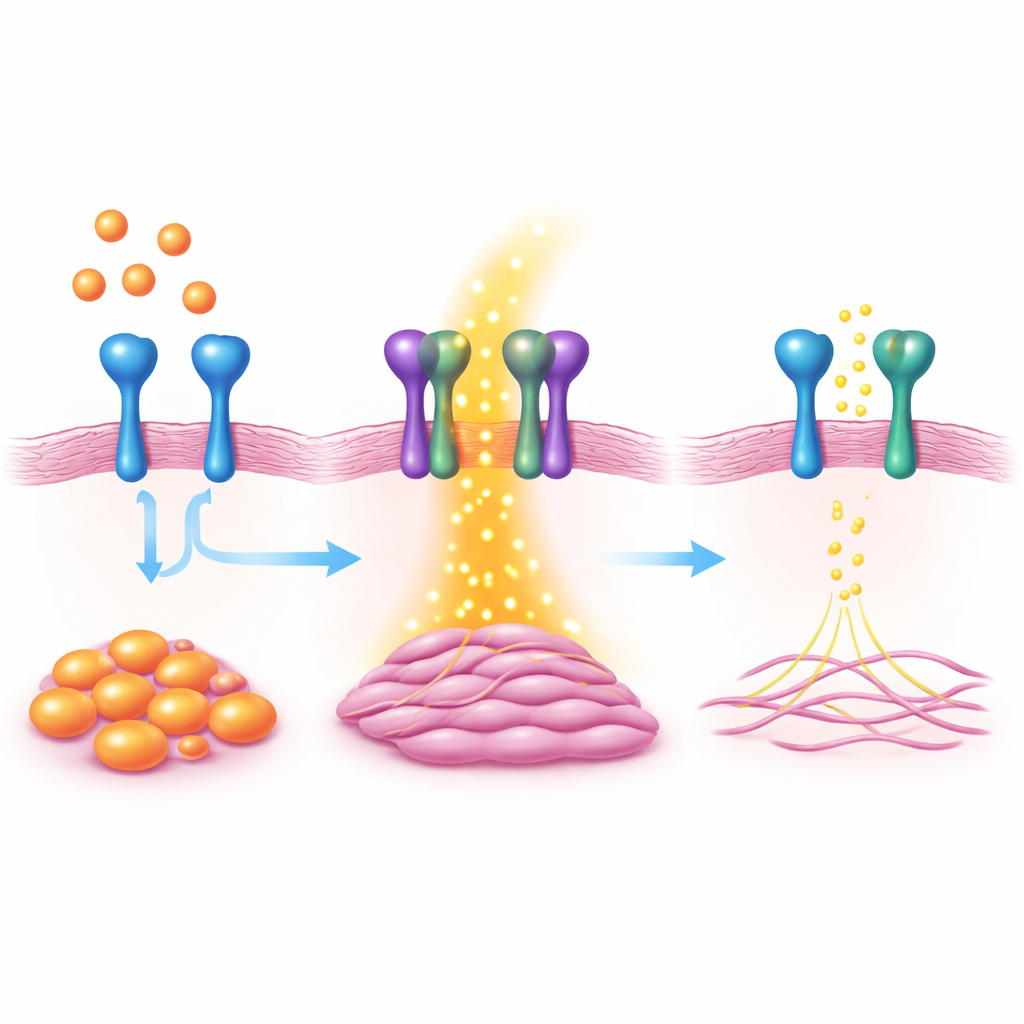
Testando VAP1 em corações vivos
Para ver como o VAP1 se comporta em um organismo completo, os cientistas criaram camundongos nos quais o VAP1 podia ser removido apenas dos fibroblastos cardíacos. Quando esses animais foram submetidos a sobrecarga de pressão prolongada na principal artéria que sai do coração, desenvolveram bem menos cicatrizes fibrosas do que camundongos normais, embora o aumento geral do coração tenha sido semelhante. Medidas da função de bombeamento do coração também foram melhor preservadas. Remover o VAP1 especificamente de miofibroblastos já ativados produziu uma redução semelhante na cicatrização e melhora na função, mostrando que o VAP1 é importante tanto na ativação inicial dos fibroblastos quanto na manutenção de seu estado ativo.
Como VAP1 potencializa sinais pró-cicatriz
Para descobrir como o VAP1 funciona, a equipe combinou análise de atividade gênica com levantamentos proteicos. Eles descobriram que o VAP1 interage fisicamente com outra proteína de superfície chamada PDGFRβ, um receptor que detecta sinais de crescimento conhecidos por desencadear fibrose. Quando o VAP1 estava ausente, o PDGFRβ tornava-se menos ativo e uma série de vias de sinalização a jusante que incentivam proliferação celular, migração e produção de colágeno foi enfraquecida. Uma porção do VAP1 que fica fora da membrana celular foi suficiente para restaurar esse sinal ausente quando adicionada de volta, sugerindo que a parceria física entre VAP1 e PDGFRβ na superfície celular é fundamental.
Bloqueando VAP1 com uma pequena molécula
Como o VAP1 também funciona como uma enzima, os pesquisadores testaram um composto com características de fármaco que bloqueia sua atividade. Em fibroblastos cardíacos em placas, esse inibidor reduziu marcadores de miofibroblastos e conteve sua capacidade de dividir-se, migrar e contrair. Quando administrado a camundongos com sobrecarga de pressão, o composto não impediu o crescimento cardíaco, mas reduziu de forma marcante o acúmulo de cicatriz e melhorou medidas de quão bem o coração bombeava sangue. Esses resultados sugerem que o bloqueio farmacológico do VAP1 pode suavizar a resposta de cicatrização sem atrapalhar todos os aspectos da adaptação do coração ao estresse.
O que isso significa para pessoas com insuficiência cardíaca
Em conjunto, os achados mostram que o VAP1 atua como um ajudante crucial para sinais que empurram as células de suporte do coração a um modo rígido e formador de cicatriz. Ao reduzir o VAP1, seja geneticamente nos fibroblastos ou com um inibidor, o coração desenvolve menos colágeno rígido e mantém melhor função sob estresse. Embora sejam necessários mais estudos em outros modelos animais e em tecido humano, o trabalho posiciona o VAP1 como um alvo promissor para futuras terapias destinadas a limitar a fibrose cardíaca prejudicial e aliviar o fardo da insuficiência cardíaca.
Citação: Huang, S., Zhao, Q., Shao, T. et al. VAP1 promotes cardiac fibrosis by enabling PDGFR signaling in myofibroblasts. Exp Mol Med 58, 1284–1296 (2026). https://doi.org/10.1038/s12276-026-01690-7
Palavras-chave: fibrose cardíaca, insuficiência cardíaca, fibroblastos, VAP1, sinalização PDGFR