Clear Sky Science · he
VAP1 מקדם פיברוזה של הלב על‑ידי אפשרות איתות PDGFR במיופיברובלסטים
למה צלקות בלב חשובות
אי־ספיקת לב פוגעת במיליוני אנשים ובדרך כלל מתפתחת כשהלב מתמלא בהדרגה ברקמת צלקת קשה. תהליך הצלקת הזה, שנקרא פיברוזה, מקשה על הלב להירגע ולשאוב דם. המחקר המתואר כאן בוחן כיצד תאי תמיכה מסוימים בלב הופכים לתאים אגרסיביים שיוצרים צלקות ומזהה מולקולת פני שטח, VAP1, שעוזרת להניע את השינוי הזה. הבנת המתג הזה פותחת פתח לשיטות חדשות להאטה או אפילו להפיכה של צלקות מזיקות במחלות לב. 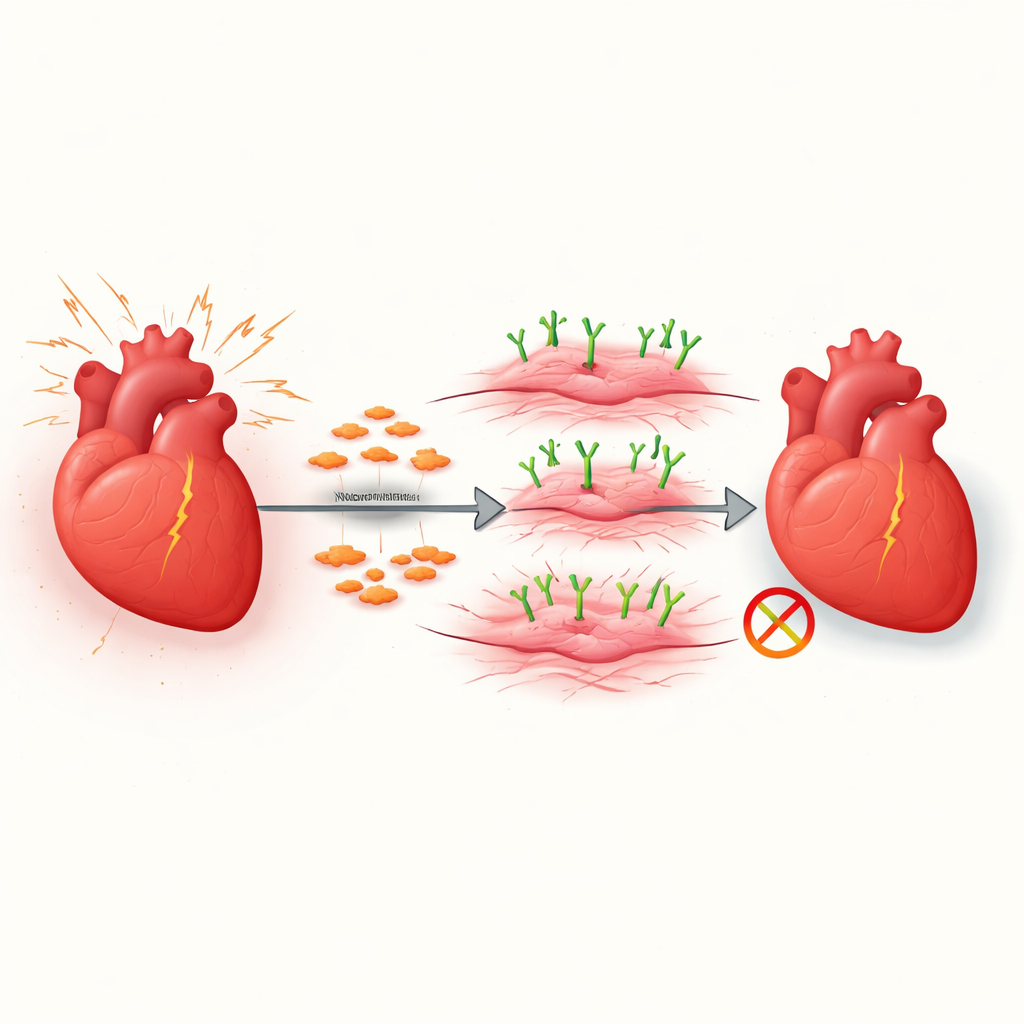
מסייעים שקטים לבוני־יתר
בלב בריא יש הרבה פיברובלסטים — תאי תמיכה שקטים המשמרים את מבנה הרקמה. כאשר הלב ניזוק או נתון ללחץ ממושך, חלק מהפיברובלסטים עוברים שינוי למיופיברובלסטים, שהם בוני־צלקת פעילים מאוד. בתגובות קצרות זה יכול להיות מגן, אך כאשר המצב נמשך ללא בקרה הוא ממלא את דופן הלב בסיבים קשים שמגבילים את תנועתו. החוקרים התמקדו באופן שבו נשלט המעבר מפיברובלסט למיופיברובלסט, במיוחד במודל נפוץ של עומס לחץ המדמה צורות של אי־ספיקת לב בבני אדם.
שומר גבול על־המשטח בשם VAP1
באמצעות סריקות פעילות גנים בהיקף גדול מצאו החוקרים כי חלבון פני שטח בשם VAP1 עולה בצורה חדה כאשר מתעורר מתג ראשי לפיברוזה, החלבון MKL1. VAP1 מוכר כמשפר הדבקה של תאי דם לבנים לכלי דם, אך תפקידו בלב לא היה ברור. בפיברובלסטים לבביים המטופחים במעבדה — הורדת רמות VAP1 צמצמה תכונות מפתח של מיופיברובלסטים, כגון חלוקה, ניידות ויכולת להתכווץ ולמשוך את סביבתם. הגברה של VAP1 עשתה את ההפך ודחפה פיברובלסטים לעבר המצב הפעיל היוצר צלקת. 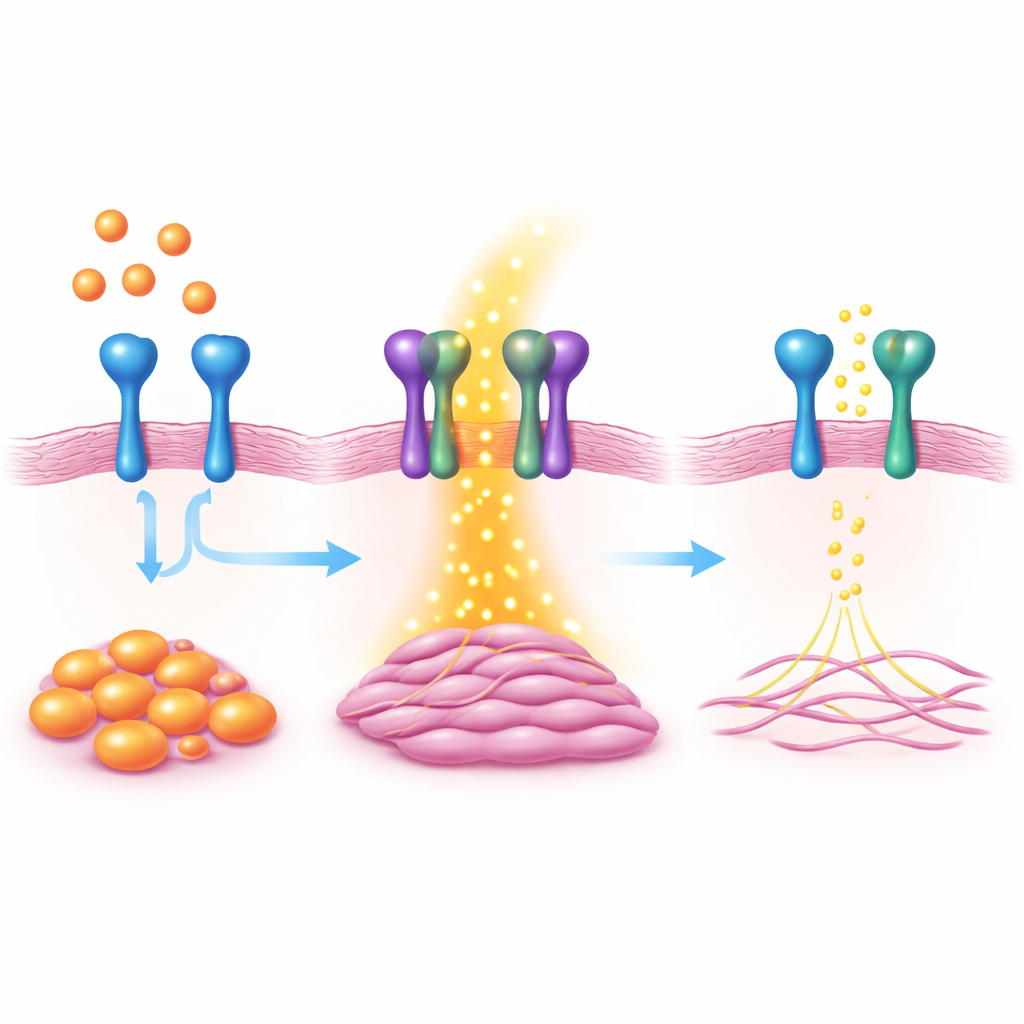
בדיקת VAP1 בלב חי
כדי לבדוק כיצד VAP1 פועל באורגניזם שלם, המדענים הנדסו עכברים שבהם ניתן היה להסיר VAP1 רק מפיברובלסטים לבביים. כאשר עכברים אלה הוטלו תחת עומס לחץ ממושך בעורק הראשי היוצא מהלב, הם פיתחו פחות צלקת סיבית בהשוואה לעכברים רגילים, למרות שהגדלת הלב הכוללת הייתה דומה. מדדי פונקציית השאיבה של הלב נשמרו גם הם טוב יותר. הסרה של VAP1 באופן ספציפי ממיופיברובלסטים שכבר הופעלו הובילה להקטנה דומה בצלקת ולשיפור בתפקוד, והראתה כי VAP1 חשוב הן בזמן ההפעלה והן כשהתאים נשארים פעילים.
כיצד VAP1 מחזק אותות פרו‑צלקת
כדי לגלות כיצד VAP1 פועל שילבו החוקרים ניתוח פעילות גנים וסקרי חלבונים. הם גילו כי VAP1 מתקשר פיזית עם חלבון פני שטח נוסף בשם PDGFRβ, קולטן החושף אותות גדילה הידועים כמפעילים פיברוזה. כשה‑VAP1 נעדר, PDGFRβ הפך לפחות פעיל וסדרה של מסלולי אותות מטה שגורמים לחלוקה, ניידות וייצור קולגן הוחלשו. מקטע מ‑VAP1 שנמצא מחוץ לממברנת התא מספיק לשחזר את האות החסר כאשר הוסף חזרה, מה שמרמז כי השותפות הפיזית בין VAP1 ל‑PDGFRβ על פני המשטח היא המפתח.
חסימת VAP1 בעזרת מולקולה קטנה
מכיוון ש‑VAP1 משמש גם כאנזים, החוקרים בחנו תרכובת דמוי‑תרופה החוסמת את פעילותו. בפיברובלסטים לבביים בתרבית, מעכב זה הוריד סמני מיופיברובלסט וצמצם את יכולתם להתחלק, לנוע ולהתכווץ. במתן לעכברים תחת עומס לחץ, התרכובת לא עצרה את הגדילה ההיקפית של הלב, אך צמצמה במידה ניכרת את הצטברות הצלקת ושיפרה מדדים של תפקוד השאיבה. ממצאים אלה מציעים כי חסימה פרמקולוגית של VAP1 יכולה להקל את תגובת הצלקת מבלי להפריע לכל היבטי ההתאמה של הלב ללחץ.
מה משמעות הדבר לאנשים עם אי‑ספיקת לב
לסיכום, התוצאות מראות כי VAP1 פועל כעוזר מרכזי לאותות הדוחפים תאי תמיכה של הלב למצב קשיח ויוצר צלקת. על‑ידי השתקת VAP1, הן גנטית בפיברובלסטים והן בעזרת מעכב, הלב מפתח פחות קולגן קשיח ומשמר תפקוד טוב יותר תחת לחץ. למרות שיש צורך בעבודות נוספות במודלים חייתיים נוספים וברקמה אנושית, המחקר מציב את VAP1 כמטרה מבטיחה לטיפולים עתידיים שמטרתם להגביל פיברוזה לבבית מזיקה ולהקל על העומס של אי‑ספיקת לב.
ציטוט: Huang, S., Zhao, Q., Shao, T. et al. VAP1 promotes cardiac fibrosis by enabling PDGFR signaling in myofibroblasts. Exp Mol Med 58, 1284–1296 (2026). https://doi.org/10.1038/s12276-026-01690-7
מילות מפתח: פיברוזה לבבית, אי ספיקת לב, פיברובלסטים, VAP1, איתות PDGFR