Clear Sky Science · nl
VAP1 bevordert cardiale fibrose door PDGFR-signaalgeving in myofibroblasten mogelijk te maken
Waarom littekening van het hart ertoe doet
Hartfalen treft miljoenen mensen en ontstaat vaak doordat het hart langzaam volloopt met stijf littekenweefsel. Dit proces, fibrose genoemd, bemoeilijkt het ontspannen en het pompen van bloed door het hart. De studie achter dit artikel onderzoekt hoe bepaalde steuncellen in het hart veranderen in agressieve littekenvormende cellen en identificeert een oppervlakte-molecuul, VAP1, dat deze verandering helpt aansturen. Het inzicht in deze omschakeling opent de deur naar nieuwe manieren om schadelijke littekening bij hartziekten te vertragen of zelfs terug te draaien. 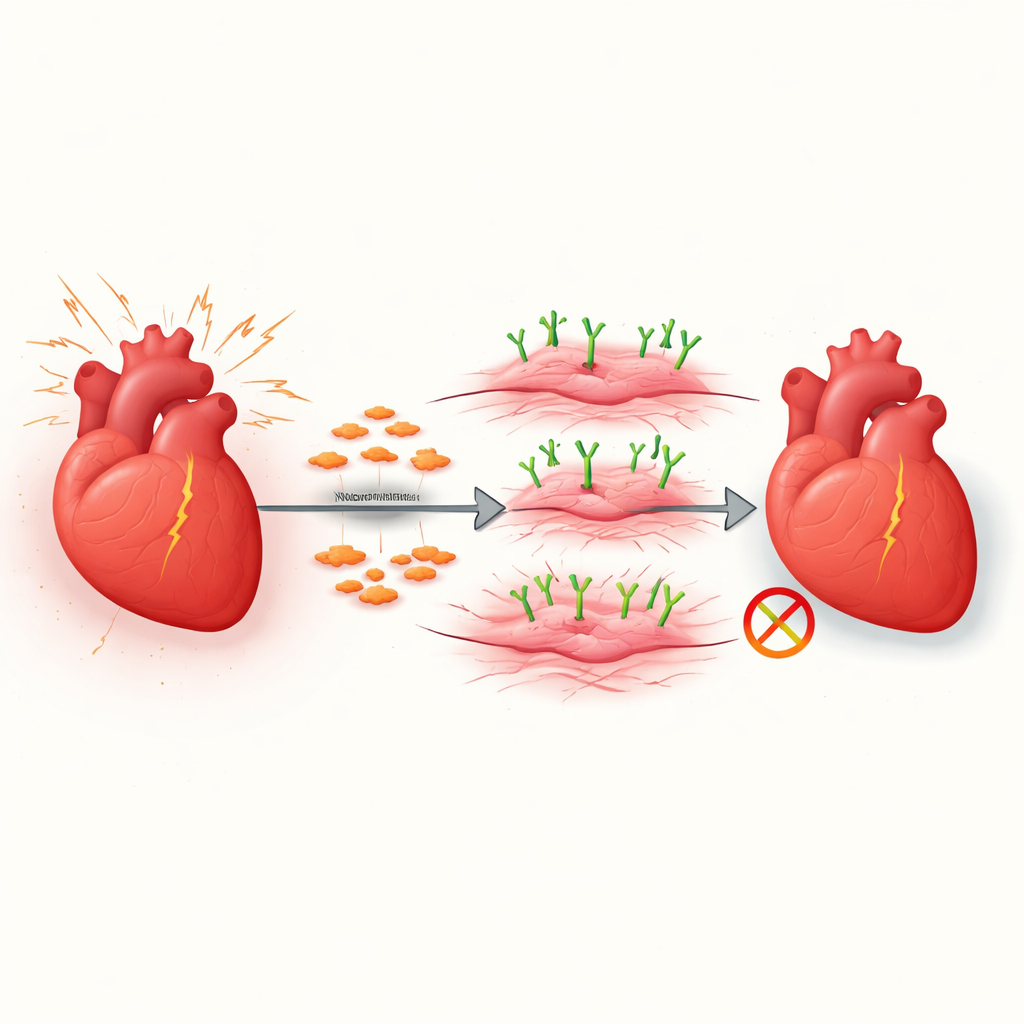
Van rustige helpers naar overactieve bouwers
Het gezonde hart bevat veel fibroblasten, rustige steuncellen die de structuur van het weefsel in stand houden. Wanneer het hart beschadigd is of langdurig onder druk staat, schakelen sommige van deze fibroblasten over naar myofibroblasten, die zeer actief littekenweefsel bouwen. In korte episodes kan deze reactie beschermend zijn, maar wanneer ze ongecontroleerd doorgaat vult ze de hartwand met taaie vezels die de beweeglijkheid beperken. De onderzoekers concentreerden zich op hoe deze omschakeling van fibroblast naar myofibroblast wordt gereguleerd, speciaal in een veelgebruikt model van drukoverbelasting dat vormen van menselijk hartfalen nabootst.
Een oppervlakte-sluithouder genaamd VAP1
Met grootschalige genactiviteitsscreening vonden de onderzoekers dat een oppervlakte-eiwit met de naam VAP1 sterk toenam wanneer een meesterregelaar voor littekening, het eiwit MKL1, werd geactiveerd. VAP1 is op zich bekend om witte bloedcellen te helpen zich aan bloedvaten te hechten, maar de rol ervan in het hart was onduidelijk. In in vitro gekweekte hartfibroblasten leidde het verlagen van VAP1 tot minder kenmerkende eigenschappen van myofibroblasten, zoals celgroei, migratie en het vermogen samen te trekken en te trekken aan hun omgeving. Het verhogen van VAP1 had het tegengestelde effect en duwde fibroblasten sterker naar de actieve, littekenvormende staat. 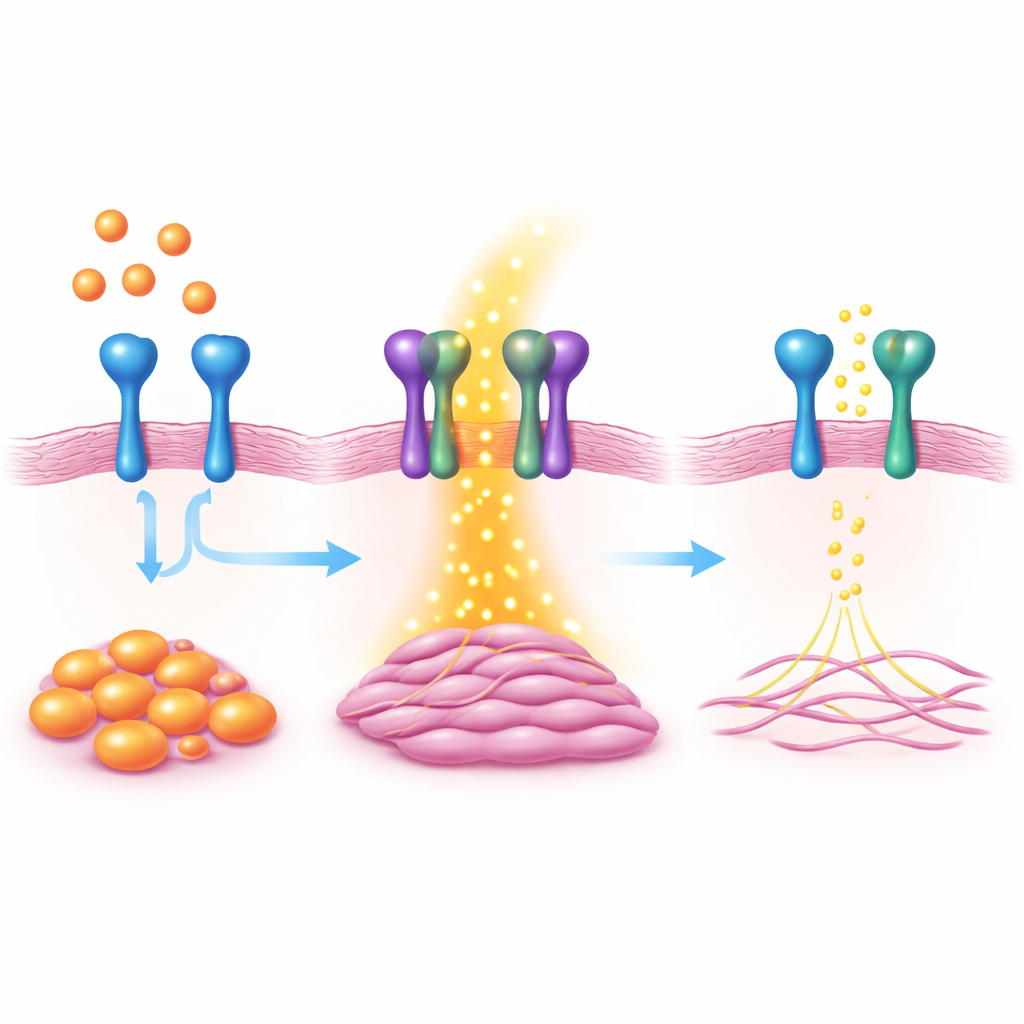
VAP1 testen in levende harten
Om te zien hoe VAP1 zich in een volledig organisme gedraagt, maakten de wetenschappers muizen waarbij VAP1 alleen uit hartfibroblasten verwijderd kon worden. Toen deze muizen langdurige druk op de hoofdslagader uit het hart kregen, ontwikkelden ze veel minder vezelig littekenweefsel dan normale muizen, hoewel de algemene vergroting van het hart vergelijkbaar bleef. Metingen van de pompfunctie van het hart bleven ook beter behouden. Het specifiek verwijderen van VAP1 uit reeds geactiveerde myofibroblasten resulteerde in een vergelijkbare vermindering van littekening en verbetering van de functie, wat aantoont dat VAP1 belangrijk is zowel bij het inschakelen van fibroblasten als bij het in stand houden van hun activiteit.
Hoe VAP1 pro-litteken signalen versterkt
Om te achterhalen hoe VAP1 werkt, combineerde het team genactiviteitsanalyse met eiwitonderzoeken. Ze ontdekten dat VAP1 fysiek samenwerkt met een ander oppervlakte-eiwit, PDGFRβ, een receptor die groeisignalen opvangt die bekendstaan om fibrose te stimuleren. Wanneer VAP1 ontbrak, werd PDGFRβ minder actief en werden een reeks downstream-signaleringsroutes die celgroei, migratie en collageenproductie bevorderen verzwakt. Een deel van het VAP1-eiwit dat buiten de celmembraan zit was voldoende om het ontbrekende signaal te herstellen wanneer het werd toegevoegd, wat suggereert dat de fysieke samenwerking tussen VAP1 en PDGFRβ op het celoppervlak cruciaal is.
VAP1 blokkeren met een klein molecuul
Aangezien VAP1 ook als enzym functioneert, testten de onderzoekers een geneesmiddelachtig bestanddeel dat zijn activiteit remt. In hartfibroblasten in kweekverminderde deze remmer myofibroblast-markers en remde hij hun vermogen om zich te delen, te migreren en samen te trekken. Bij toediening aan muizen met drukoverbelasting stopte de verbinding de vergroting van het hart niet, maar verminderde hij duidelijk de opbouw van littekenweefsel en verbeterde hij metingen van de hartpompfunctie. Deze resultaten suggereren dat farmacologische blokkade van VAP1 de littekenreactie kan verzachten zonder alle aspecten van de hartaanpassing aan stress te verstoren.
Wat dit betekent voor mensen met hartfalen
Samen laten de bevindingen zien dat VAP1 fungeert als een cruciale helper voor signalen die steuncellen van het hart in een starre, littekenvormende modus duwen. Door VAP1 te dempen, zowel genetisch in fibroblasten als met een remmer, ontwikkelt het hart minder stijf collageen en behoudt het onder stress een betere functie. Hoewel aanvullend werk in extra diermodellen en menselijk weefsel nodig is, plaatst de studie VAP1 als een veelbelovend doelwit voor toekomstige therapieën gericht op het beperken van schadelijke cardiale fibrose en het verlichten van de last van hartfalen.
Bronvermelding: Huang, S., Zhao, Q., Shao, T. et al. VAP1 promotes cardiac fibrosis by enabling PDGFR signaling in myofibroblasts. Exp Mol Med 58, 1284–1296 (2026). https://doi.org/10.1038/s12276-026-01690-7
Trefwoorden: cardiale fibrose, hartfalen, fibroblasten, VAP1, PDGFR-signaalgeving