Clear Sky Science · ru
Вклад TLR2, TLR8 и TLR3 в прямое и опосредованное антителами усиление инфекции денге серотипа 2
Почему это исследование важно
Лихорадка денге — это переносимое комарами заболевание, которое может варьироваться от тяжёлой гриппоподобной болезни до опасных для жизни кровотечений и шока. Люди, заразившиеся денге повторно, подвержены повышенному риску тяжёлого течения, особенно когда уже имеющиеся антитела вместо защиты способствуют проникновению вируса в клетки иммунной системы. В этом исследовании выявлены ключевые молекулы на иммунных клетках, которые делают возможным такое опасное «усиление» инфекции и воспаления, и обозначены новые подходы для предотвращения наиболее серьёзных форм денге.
Когда полезные антитела становятся вредными
После первичной инфекции денге организм сохраняет антитела, способные распознавать вирус. При последующей инфекции другим серотипом эти антитела могут не нейтрализовать возбудителя полностью. Вместо этого они покрывают вирус и направляют его в определённые лейкоциты через рецепторы к антителам — процесс, называемый антителозависимым усилением. Авторы применили экспериментальную систему на основе человеческих кровяных клеток, чтобы сравнить такое усиленное инфицирование с обычной инфекцией вирусом денге типа 2. В фокусе были моноциты — тип иммунных клеток, который как служит хозяином для вируса, так и выделяет провоспалительные вещества, способные повреждать кровеносные сосуды.
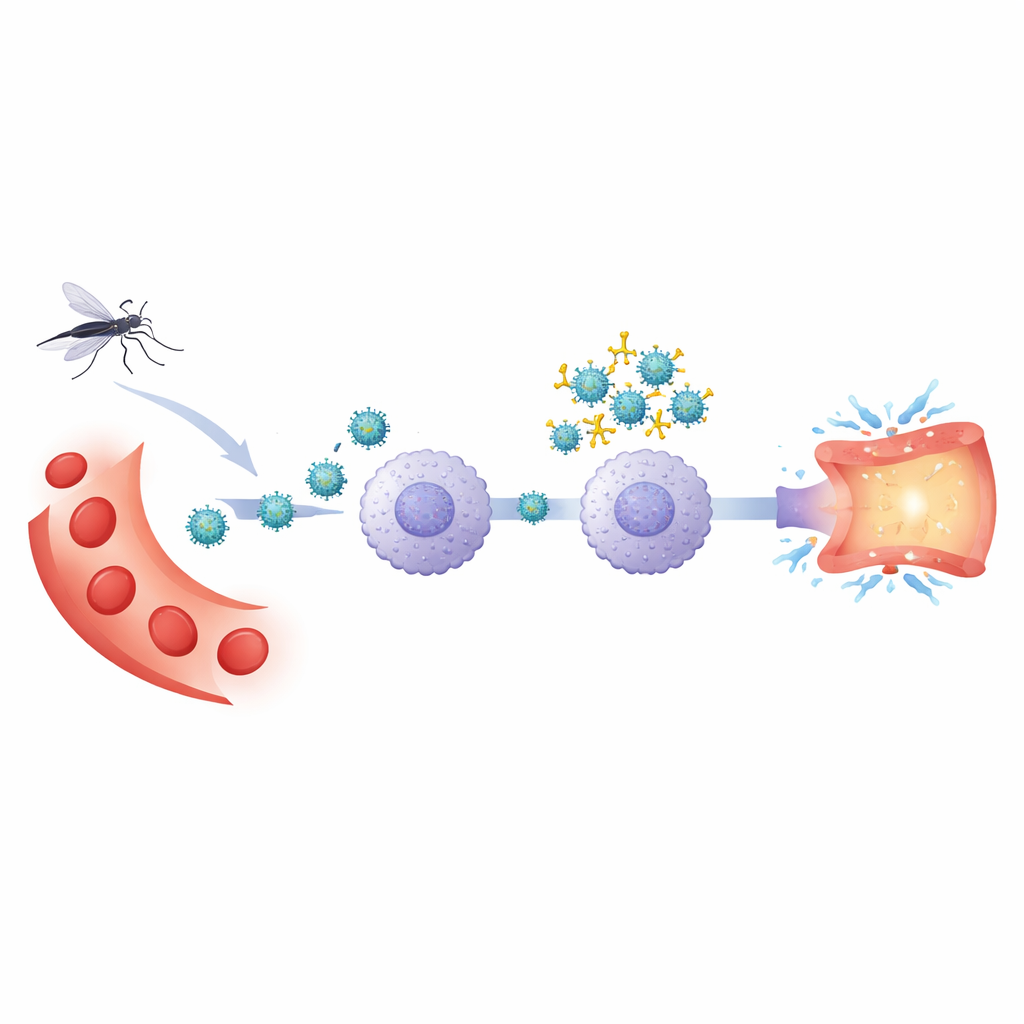
Ключевые «шлюзы» на иммунных клетках
Команда исследовала несколько рецепторов — молекулярных «стоянок» на моноцитах. Один из них — CD32, рецептор, распознающий антитела, связанные с вирусом. Другие — сенсоры, обычно улавливающие патогены: TLR2 на поверхности клетки и TLR3 и TLR8 в внутриклеточных компартментах, а также сигнальный фермент SYK, связывающий рецепторы с последующими реакциями. Селективно блокируя эти молекулы антителами или малыми ингибиторами, авторы проверяли, какие из них действительно необходимы для проникновения вируса и последующего всплеска воспаления.
TLR2 как незаменимый помощник при входе
Эксперименты показали, что при антителозависимом проникновении вируса блокада CD32 или SYK снижала уровень инфекции до того, что наблюдался без антител. Поразительно, что блокада TLR2 давала ещё более выраженный эффект: она почти полностью предотвращала инфекцию как в условиях с антителами, так и без них. Это указывает на то, что TLR2 — не только сенсор тревоги, но и ключевой помощник, необходимый вирусу для попадания в моноциты при любых условиях. Молекула CD14 содействовала этому процессу, тогда как другие предполагаемые со‑рецепторы, такие как TLR1, TLR6, CD36 или LILRB1, в этой модели роли не играли.
От проникновения вируса до повреждения сосудов
Тяжёлое течение денге сопровождается повышенной проницаемостью сосудов. Чтобы связать события в моноцитах с эффектами на сосуды, исследователи собрали среду из инфицированных культур кровяных клеток и нанесли её на выращенные в лаборатории эндотелиальные клетки вен человека. Эти сосудистые клетки реагировали включением на поверхности маркеров, способствующих воспалению и утечке, но только при обработке веществами, выделенными инфицированными моноцитами, а не при контакте лишь с комплексами вирус–антитело. При антителозависимом усилении моноциты вырабатывали ещё больше таких активирующих сигналов, чем при прямой инфекции. Блокада CD32, SYK или TLR2 в кровяных клетках резко снижала эту активацию эндотелия и уменьшала уровни противовирусных и провоспалительных молекул, таких как интерфероны и TNF‑альфа.
Скрытая вирусная РНК вызывает бурю
Чтобы выяснить, что именно запускает воспалительную бурю, команда проверила, могут ли неинфекционные вирусные частицы активировать моноциты. Когда вирусный генетический материал разрушали УФ‑облучением, частицы не вызывали образование сосудисто‑активирующих сигналов, хоть TLR2 и мог с ними взаимодействовать. Это указывало на вирусную РНК как ключевой триггер. Действительно, при блокаде внутренних РНК‑сенсоров TLR3 и особенно TLR8 моноциты вырабатывали значительно меньше провоспалительных и противовирусных веществ, особенно в условиях антителозависимого усиления, при этом число инфицированных клеток не уменьшалось. Это предполагает двухступенчатый механизм: сначала TLR2 помогает доставить комплексы вирус–антитело внутрь клетки, а после обнажения вирусной РНК внутри клетки TLR3 и TLR8 распознают её и запускают вредный иммунный ответ, при этом SYK выступает общим сигнальным узлом.
Что это значит для борьбы с тяжёлым денге
В совокупности исследование предлагает ясную цепочку событий, связывающую вторичную инфекцию денге с развитием тяжёлого заболевания. Антитела от предыдущей инфекции могут переносить вирус денге в моноциты через CD32, но успешная инфекция в этих клетках также зависит от TLR2. Попав внутрь, вирус обнажает свою РНК, которую обнаруживают TLR3 и TLR8; совместно с SYK они запускают мощную противовирусную и провоспалительную программу, активирующую и нарушающую целостность сосудов. Идентификация TLR2, TLR3, TLR8 и SYK как центральных звеньев как входа вируса, так и вредного воспаления подчёркивает потенциальные лекарственные мишени, которые в будущем могут помочь предотвратить прогрессирование лёгкой формы денге в её опасные, угрожающие жизни варианты.
Цитирование: ter Ellen, B.M., Punekar, M., Castillo, J.A. et al. The contributions of TLR2, TLR8 and TLR3 to direct and antibody-dependent enhancement of dengue virus serotype 2 infection. npj Viruses 4, 24 (2026). https://doi.org/10.1038/s44298-026-00190-9
Ключевые слова: вирус денге, антителозависимое усиление, врожденный иммунитет, рецепторы типа Toll, утечка из сосудов