Clear Sky Science · es
Las contribuciones de TLR2, TLR8 y TLR3 a la potenciación directa y dependiente de anticuerpos de la infección por dengue serotipo 2
Por qué esta investigación importa
El dengue es una enfermedad transmitida por mosquitos que puede ir desde una afección similar a una gripe severa hasta hemorragias y shock potencialmente mortales. Las personas que contraen dengue por segunda vez tienen un mayor riesgo de enfermedad grave, especialmente cuando sus anticuerpos preexistentes, en lugar de protegerlas, facilitan que el virus infecte las células inmunitarias. Este estudio descubre moléculas clave en las células inmunitarias que hacen posible este peligroso “aumento” de la infección y la inflamación, y apunta a nuevas formas de prevenir las formas más graves del dengue.
Cuando los anticuerpos útiles se vuelven dañinos
Tras una primera infección por dengue, el organismo conserva anticuerpos que pueden reconocer el virus. Durante una infección posterior con un tipo distinto de dengue, estos anticuerpos pueden no neutralizar totalmente al invasor. En cambio, pueden recubrir el virus y guiarlo hacia ciertos glóbulos blancos a través de receptores de anticuerpos, un proceso llamado potenciación dependiente de anticuerpos. Los autores emplearon un sistema experimental basado en células sanguíneas humanas para comparar esta infección potenciada con la infección ordinaria por el virus del dengue tipo 2. Se centraron en los monocitos, un tipo de célula inmunitaria que hospeda al virus y libera sustancias inflamatorias que pueden dañar los vasos sanguíneos.
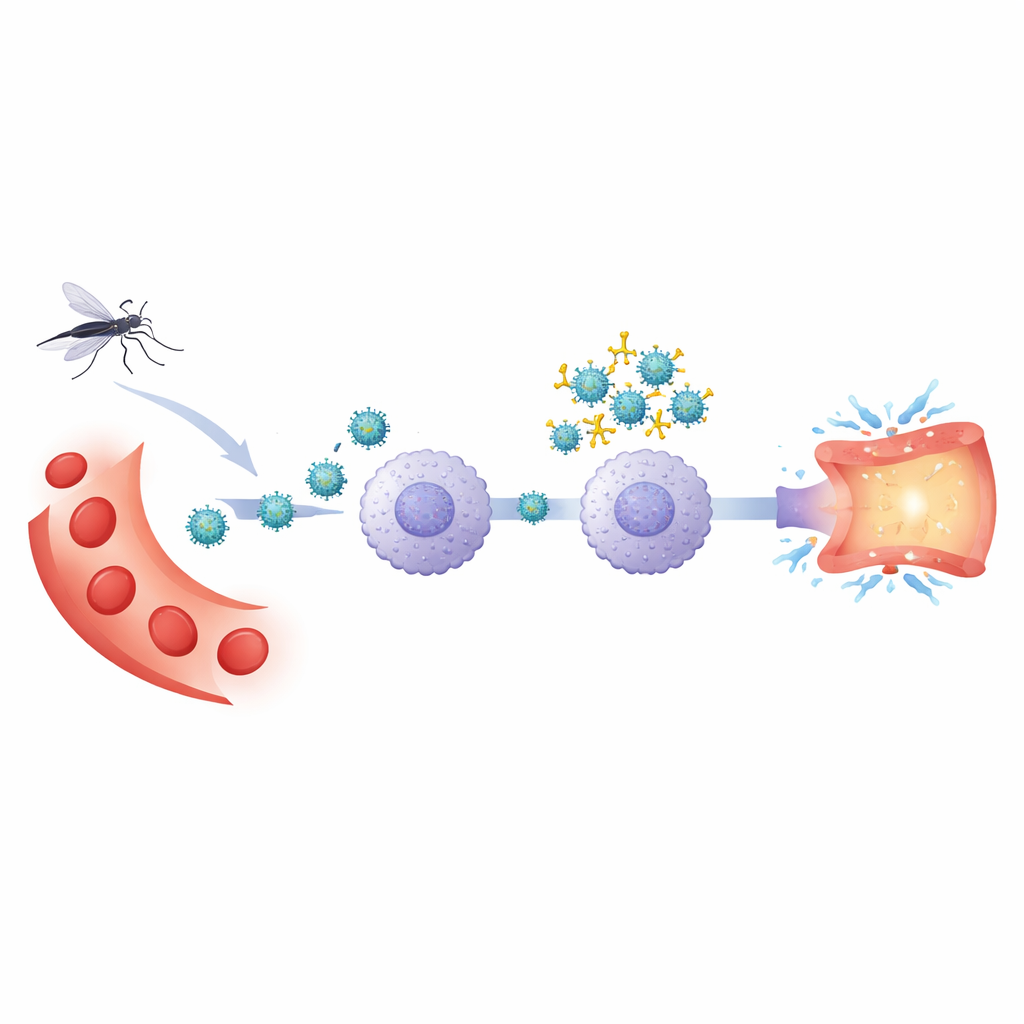
Guardianes clave en las células inmunitarias
El equipo examinó varios receptores—“estaciones de atraque” moleculares—en los monocitos. Uno fue CD32, un receptor que reconoce anticuerpos unidos al virus. Otros fueron sensores que típicamente detectan gérmenes, incluyendo TLR2 en la superficie celular y TLR3 y TLR8 dentro de compartimentos celulares, así como una enzima de señalización llamada SYK que enlaza los receptores con las reacciones posteriores. Bloqueando selectivamente estas moléculas con anticuerpos o pequeños inhibidores, preguntaron cuáles eran verdaderamente necesarias para la entrada del virus y para la explosión inflamatoria que sigue.
TLR2 como ayudante esencial de entrada
Los experimentos mostraron que cuando el virus del dengue entraba en las células con la ayuda de anticuerpos, bloquear CD32 o SYK reducía la infección hasta el nivel observado sin anticuerpos. De forma notable, bloquear TLR2 fue aún más efectivo: casi impidió por completo la infección, tanto con anticuerpos como sin ellos. Esto indica que TLR2 no es solo un sensor de alarma, sino que también actúa como un ayudante crucial para que el virus entre en los monocitos en todas las condiciones. Otra molécula, CD14, apoyó este proceso, mientras que otros correceptores propuestos como TLR1, TLR6, CD36 o LILRB1 no desempeñaron un papel detectable en este modelo.
De la entrada viral al daño vascular
El dengue grave se caracteriza por vasos sanguíneos filtrantes. Para conectar los eventos en los monocitos con efectos sobre los vasos, los investigadores recogieron el fluido de cultivos de células sanguíneas infectadas y lo aplicaron a células endoteliales de venas humanas cultivadas en laboratorio. Estas células vasculares respondieron activando marcadores de superficie que promueven inflamación y fuga, pero solo cuando fueron expuestas a sustancias liberadas por monocitos infectados, no a las mezclas de virus y anticuerpos por sí solas. La infección potenciada por anticuerpos hizo que los monocitos produjeran aún más de estas señales activadoras que la infección directa. Bloquear CD32, SYK o TLR2 en las células sanguíneas redujo fuertemente esta activación endotelial y también disminuyó los niveles de moléculas antivirales e inflamatorias como interferones y TNF‑alfa.
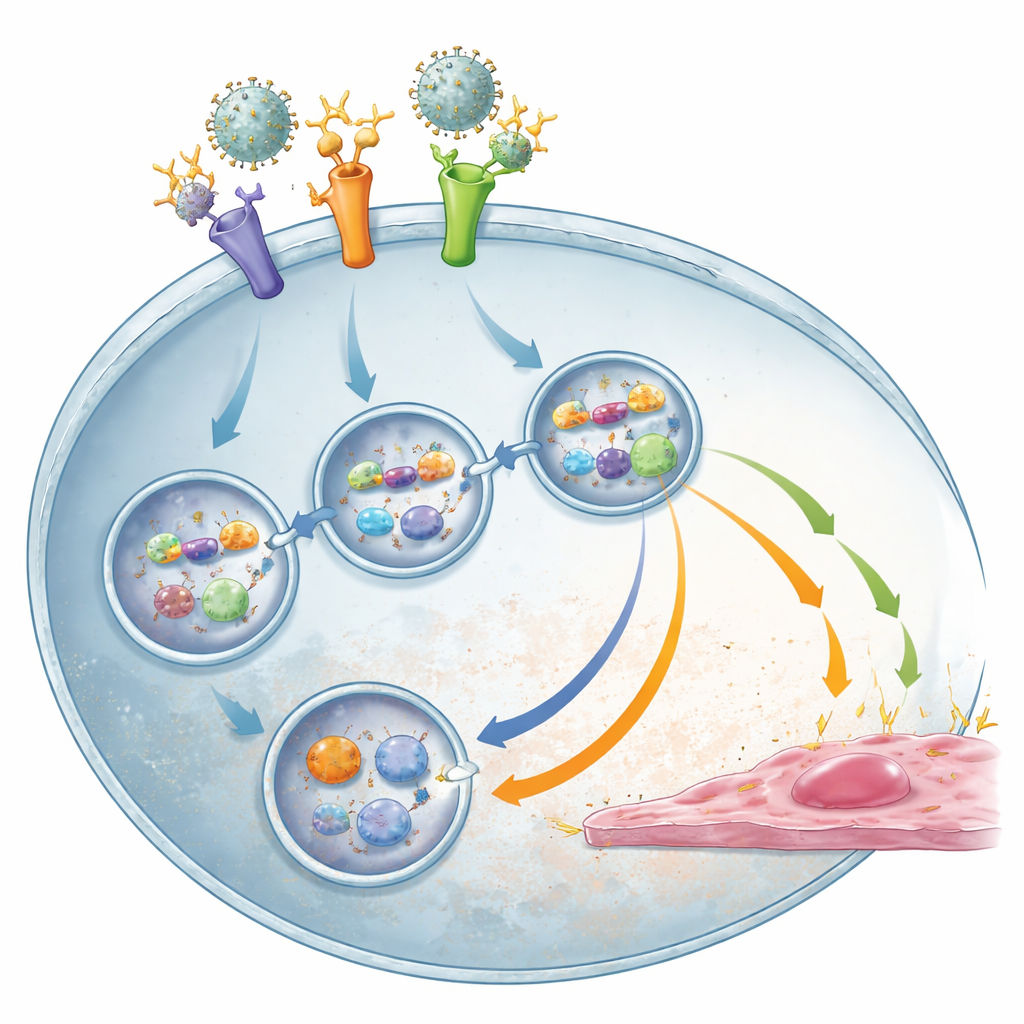
El ARN viral oculto desencadena la tormenta
Para averiguar qué desencadena realmente la tormenta inflamatoria, el equipo probó si las partículas virales no infecciosas aún podían activar los monocitos. Cuando el material genético viral fue destruido por tratamiento con ultravioleta, las partículas no indujeron señales activadoras de los vasos, aunque TLR2 seguía pudiendo unirse a ellas. Esto apuntó al ARN viral como el desencadenante clave. En efecto, cuando se bloquearon los sensores internos de ARN TLR3 y sobre todo TLR8, los monocitos produjeron mucho menos sustancias inflamatorias y antivirales, particularmente en condiciones de potenciación por anticuerpos, sin reducir el número de células infectadas. Esto sugiere un proceso en dos pasos: TLR2 primero ayuda a introducir los complejos virus–anticuerpo en la célula, y una vez expuesto el ARN viral en el interior, TLR3 y TLR8 lo detectan y conducen la respuesta inmunitaria dañina, con SYK actuando como un centro de señalización compartido.
Qué significa esto para combatir el dengue grave
En conjunto, el estudio propone una cadena clara de eventos que conecta la infección secundaria por dengue con la enfermedad grave. Los anticuerpos de una infección previa pueden transportar el virus del dengue hacia los monocitos a través de CD32, pero la infección exitosa en estas células también depende de TLR2. Una vez dentro, el virus expone su ARN a TLR3 y TLR8 que, junto con SYK, encienden un potente programa inflamatorio y antiviral que activa y daña los vasos sanguíneos. Al identificar a TLR2, TLR3, TLR8 y SYK como actores centrales tanto en la entrada viral como en la inflamación nociva, este trabajo destaca posibles dianas farmacológicas que podrían, en el futuro, ayudar a prevenir que un dengue leve progrese a sus formas más peligrosas y potencialmente mortales.
Cita: ter Ellen, B.M., Punekar, M., Castillo, J.A. et al. The contributions of TLR2, TLR8 and TLR3 to direct and antibody-dependent enhancement of dengue virus serotype 2 infection. npj Viruses 4, 24 (2026). https://doi.org/10.1038/s44298-026-00190-9
Palabras clave: virus del dengue, potenciación dependiente de anticuerpos, inmunidad innata, receptores tipo Toll, fuga vascular