Clear Sky Science · it
I contributi di TLR2, TLR8 e TLR3 all’infezione da virus della dengue sierotipo 2 diretta e potenziata da anticorpi
Perché questa ricerca è importante
La febbre dengue è una malattia trasmessa dalle zanzare che può variare da una forte sindrome simil-influenzale a emorragie e shock potenzialmente letali. Chi contrae la dengue per la seconda volta è a maggior rischio di forme gravi, soprattutto quando gli anticorpi preesistenti, invece di proteggere, facilitano l’ingresso del virus nelle cellule immunitarie. Questo studio individua molecole chiave sulle cellule immunitarie che rendono possibile questo pericoloso “potenziamento” dell’infezione e dell’infiammazione e indica nuove vie per prevenire le forme più gravi di dengue.
Quando gli anticorpi utili diventano nocivi
Dopo una prima infezione da dengue, l’organismo conserva anticorpi in grado di riconoscere il virus. In una successiva infezione con un tipo diverso di dengue, questi anticorpi potrebbero non neutralizzare completamente l’invasore. Invece, possono rivestire il virus e guidarlo in particolari globuli bianchi attraverso i recettori per gli anticorpi, un processo chiamato potenziamento dipendente da anticorpi. Gli autori hanno usato un sistema sperimentale basato su cellule del sangue umano per confrontare questa infezione potenziata con l’infezione ordinaria da virus della dengue tipo 2. Si sono concentrati sui monociti, un tipo di cellula immunitaria che sia ospita il virus sia rilascia sostanze infiammatorie in grado di danneggiare i vasi sanguigni.
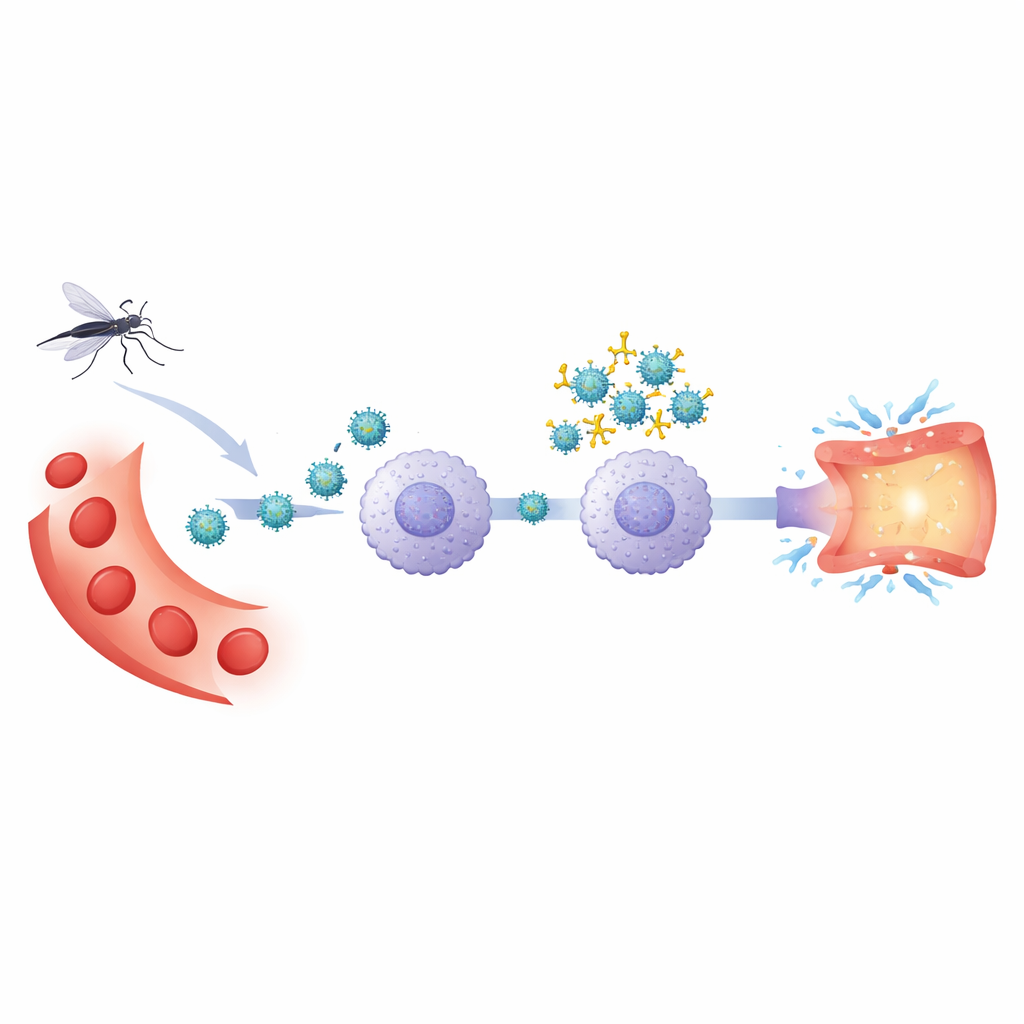
Portieri chiave sulle cellule immunitarie
Il gruppo ha esaminato diversi recettori — vere e proprie “stazioni di attracco” molecolari — sui monociti. Uno era CD32, un recettore che riconosce gli anticorpi legati al virus. Altri erano sensori che normalmente rilevano i germi, compresi TLR2 sulla superficie cellulare e TLR3 e TLR8 all’interno dei compartimenti cellulari, oltre a un enzima di segnalazione chiamato SYK che collega i recettori alle reazioni a valle. Bloccando selettivamente queste molecole con anticorpi o piccoli inibitori, hanno chiesto quali fossero davvero necessarie per l’ingresso del virus e per l’esplosione infiammatoria che ne consegue.
TLR2 come essenziale facilitatore dell’ingresso
Gli esperimenti hanno mostrato che quando il virus della dengue entrava nelle cellule con l’aiuto degli anticorpi, bloccare CD32 o SYK riduceva l’infezione al livello osservato senza anticorpi. Colpisce che il blocco di TLR2 andasse oltre: ha quasi completamente impedito l’infezione, sia con che senza anticorpi. Ciò indica che TLR2 non è solo un sensore d’allarme ma agisce anche come un aiuto cruciale per il virus per entrare nei monociti in tutte le condizioni. Un’altra molecola, CD14, ha supportato questo processo, mentre altri co-recettori proposti come TLR1, TLR6, CD36 o LILRB1 non hanno avuto un ruolo rilevabile in questo modello.
Dall’ingresso virale al danno vascolare
La dengue grave è caratterizzata da vasi sanguigni permeabili. Per collegare gli eventi nei monociti agli effetti sui vasi, i ricercatori hanno raccolto il fluido delle colture di cellule del sangue infette e lo hanno applicato a cellule endoteliali venose umane coltivate in laboratorio. Queste cellule vascolari hanno risposto accendendo marcatori di superficie che promuovono infiammazione e perdita di barriera, ma solo quando sono state esposte a sostanze rilasciate dai monociti infetti, non ai soli complessi virus–anticorpo. L’infezione potenziata da anticorpi ha indotto i monociti a produrre ancora più segnali attivanti rispetto all’infezione diretta. Bloccare CD32, SYK o TLR2 nelle cellule del sangue ha ridotto fortemente questa attivazione endoteliale e ha anche abbassato i livelli di molecole antivirali e infiammatorie come interferoni e TNF‑alfa.
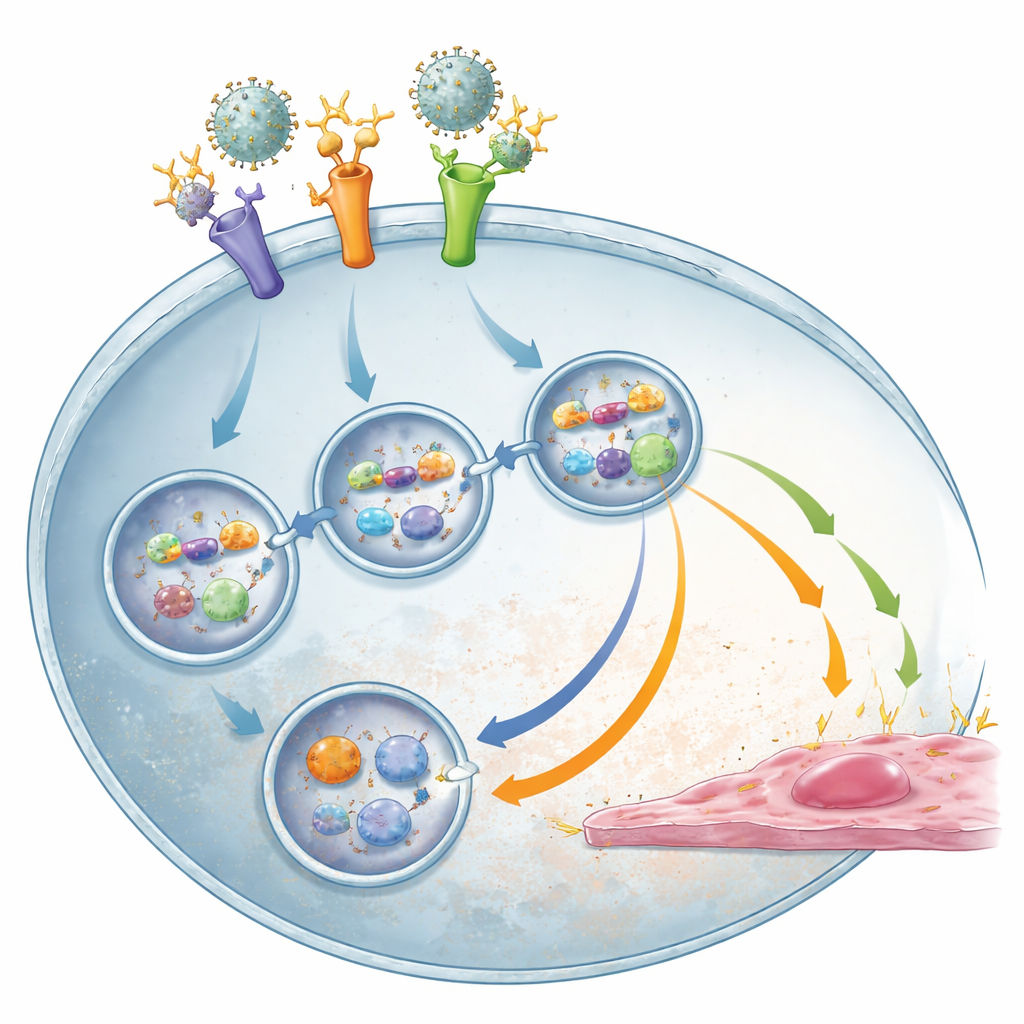
RNA virale nascosto dà il via alla tempesta
Per capire cosa scatena realmente la tempesta infiammatoria, il gruppo ha testato se particelle virali non infettive potevano comunque attivare i monociti. Quando il materiale genetico virale è stato distrutto tramite trattamento con ultravioletti, le particelle non hanno più indotto segnali in grado di attivare i vasi, pur essendo ancora riconoscibili da TLR2. Questo ha indicato l’RNA virale come il principale innesco. Infatti, quando i sensori interni dell’RNA, TLR3 e soprattutto TLR8, sono stati bloccati, i monociti hanno prodotto molto meno sostanze infiammatorie e antivirali, in particolare nelle condizioni di infezione potenziata da anticorpi, senza però ridurre la percentuale di cellule infette. Ciò suggerisce un processo in due fasi: TLR2 aiuta prima a introdurre i complessi virus–anticorpo nella cellula e, una volta che l’RNA virale viene esposto all’interno, TLR3 e TLR8 lo rilevano e guidano la risposta immunitaria dannosa, con SYK che agisce come un hub di segnalazione condiviso.
Cosa significa per la lotta alla dengue grave
Complessivamente, lo studio propone una catena di eventi chiara che collega l’infezione secondaria da dengue alla malattia grave. Gli anticorpi di una precedente infezione possono trasportare il virus della dengue nei monociti tramite CD32, ma la riuscita dell’infezione in queste cellule dipende anche da TLR2. Una volta all’interno, il virus espone il suo RNA a TLR3 e TLR8 che, insieme a SYK, innescano un potente programma infiammatorio e antivirale che attiva e danneggia i vasi sanguigni. Identificando TLR2, TLR3, TLR8 e SYK come attori centrali sia nell’ingresso virale sia nell’infiammazione dannosa, questo lavoro mette in luce potenziali bersagli farmacologici che potrebbero un giorno aiutare a prevenire che una dengue lieve progredisca verso le sue forme più pericolose e potenzialmente letali.
Citazione: ter Ellen, B.M., Punekar, M., Castillo, J.A. et al. The contributions of TLR2, TLR8 and TLR3 to direct and antibody-dependent enhancement of dengue virus serotype 2 infection. npj Viruses 4, 24 (2026). https://doi.org/10.1038/s44298-026-00190-9
Parole chiave: virus della dengue, potenziamento dipendente da anticorpi, immunità innata, recettori Toll-like, perdita vascolare