Clear Sky Science · pt
As contribuições de TLR2, TLR8 e TLR3 para a potencialização direta e dependente de anticorpos da infecção por dengue sorotipo 2
Por que esta pesquisa importa
A dengue é uma doença transmitida por mosquitos que pode variar de um quadro gripal intenso a hemorragias e choque potencialmente fatais. Pessoas que contraem dengue pela segunda vez têm maior risco de doença grave, especialmente quando seus anticorpos existentes, em vez de protegê‑las, acabam ajudando o vírus a infectar células imunes. Este estudo revela moléculas-chave em células imunes que tornam possível essa perigosa “potencialização” da infecção e da inflamação e aponta novas formas de prevenir as manifestações mais graves da dengue.
Quando anticorpos úteis se tornam prejudiciais
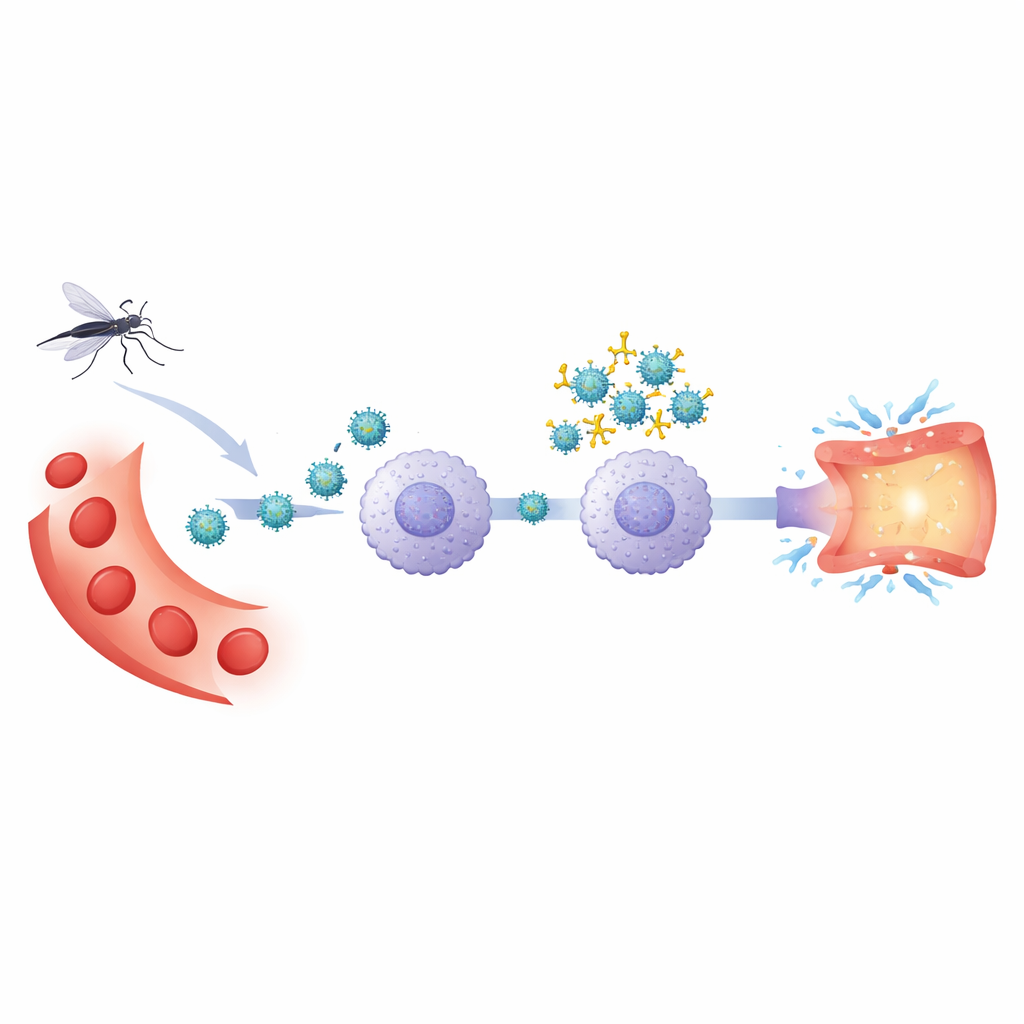
Após uma primeira infecção por dengue, o corpo mantém anticorpos que reconhecem o vírus. Durante uma infecção posterior por um tipo diferente de dengue, esses anticorpos podem não neutralizar completamente o invasor. Em vez disso, podem revestir o vírus e conduzi‑lo a certos glóbulos brancos por meio de receptores de anticorpos, um processo chamado potencialização dependente de anticorpos. Os autores usaram um sistema experimental baseado em células sanguíneas humanas para comparar essa infecção potencializada com a infecção comum pelo vírus da dengue tipo 2. Eles se concentraram em monócitos, um tipo de célula imune que tanto abriga o vírus quanto libera substâncias inflamatórias que podem danificar os vasos sanguíneos.
Guardas-chave nas células imunes
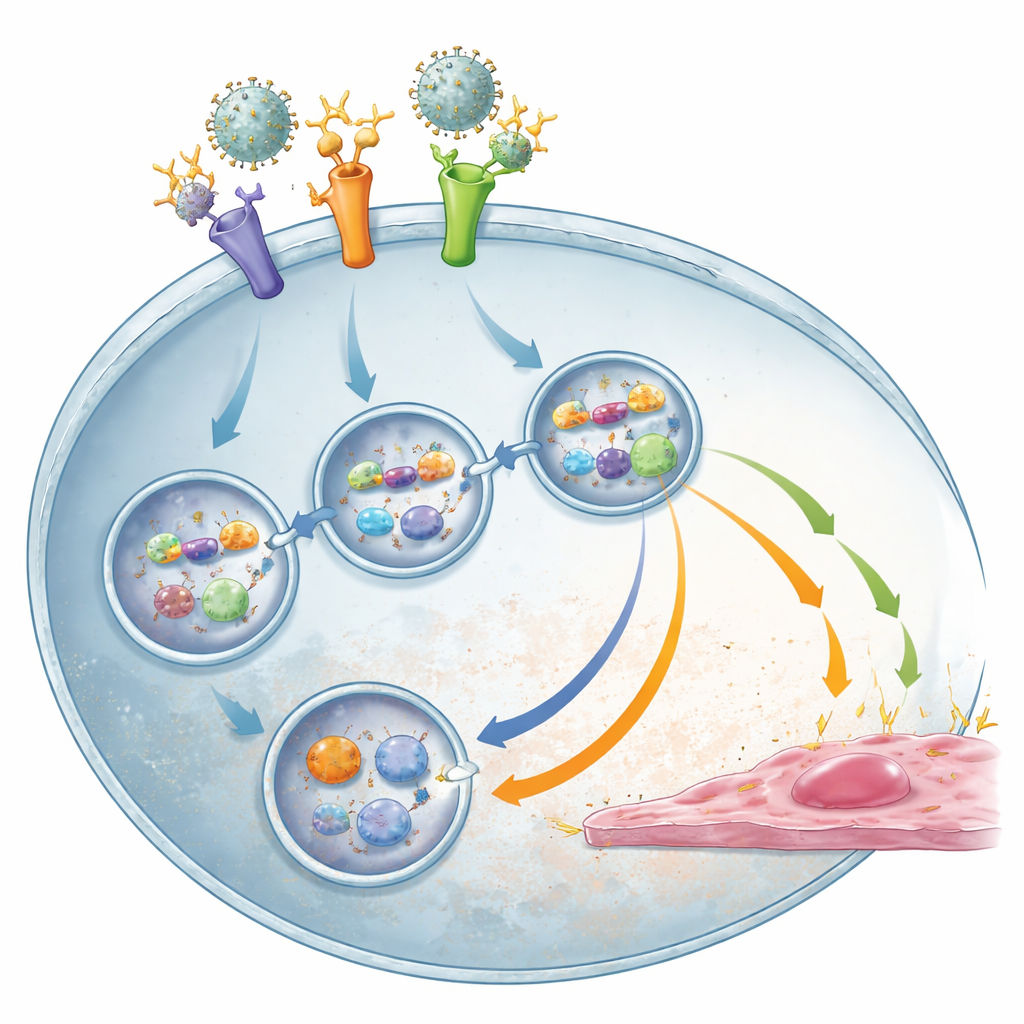
A equipe examinou vários receptores — “estações de atracação” moleculares — nos monócitos. Um deles foi CD32, um receptor que reconhece anticorpos ligados ao vírus. Outros foram sensores que normalmente detectam germes, incluindo TLR2 na superfície celular e TLR3 e TLR8 em compartimentos intracelulares, além de uma enzima de sinalização chamada SYK que liga os receptores a reações a jusante. Ao bloquear seletivamente essas moléculas com anticorpos ou pequenos inibidores, eles investigaram quais eram realmente necessárias para a entrada do vírus e para o surto inflamatório subsequente.
TLR2 como um facilitador essencial da entrada
Os experimentos mostraram que, quando o vírus da dengue entrava nas células com a ajuda de anticorpos, bloquear CD32 ou SYK reduzia a infecção de volta ao nível observado sem anticorpos. De forma marcante, bloquear TLR2 foi ainda mais eficaz: praticamente impediu a infecção, tanto com quanto sem anticorpos. Isso indica que TLR2 não é apenas um sensor de alarme, mas também atua como um ajudante crucial para o vírus entrar nos monócitos em todas as condições. Outra molécula, CD14, apoiou esse processo, enquanto outros co‑receptores propostos, como TLR1, TLR6, CD36 ou LILRB1, não desempenharam um papel detectável neste modelo.
Da entrada viral ao dano aos vasos
A dengue grave é marcada por vasos sanguíneos permeáveis. Para conectar os eventos nos monócitos aos efeitos sobre os vasos, os pesquisadores coletaram o fluido de culturas de células sanguíneas infectadas e o aplicaram a células endoteliais de veia humana cultivadas em laboratório. Essas células vasculares responderam ligando marcadores de superfície que promovem inflamação e permeabilidade, mas somente quando expostas a substâncias liberadas por monócitos infectados, não a misturas de vírus e anticorpos isoladas. A infecção potencializada por anticorpos fez com que os monócitos produzissem ainda mais desses sinais ativadores do que a infecção direta. Bloquear CD32, SYK ou TLR2 nas células sanguíneas reduziu fortemente essa ativação endotelial e também diminuiu os níveis de moléculas antivirais e inflamatórias, como interferons e TNF‑alfa.
RNA viral oculto desencadeia a tempestade
Para descobrir o que realmente desencadeia a tempestade inflamatória, a equipe testou se partículas virais não infecciosas ainda podiam ativar monócitos. Quando o material genético viral foi destruído por tratamento com ultravioleta, as partículas não induziram sinais ativadores dos vasos, embora TLR2 ainda pudesse se ligar a elas. Isso apontou o RNA viral como o gatilho-chave. De fato, quando os sensores internos de RNA TLR3 e, especialmente, TLR8 foram bloqueados, os monócitos produziram muito menos substâncias inflamatórias e antivirais, particularmente em condições de infecção potencializada por anticorpos, sem reduzir a porcentagem de células infectadas. Isso sugere um processo em duas etapas: TLR2 primeiro ajuda a levar os complexos vírus–anticorpo para dentro da célula e, uma vez exposto o RNA viral no interior, TLR3 e TLR8 o detectam e impulsionam a resposta imune danosa, com SYK atuando como um ponto de convergência de sinalização.
O que isso significa para combater a dengue grave
Em conjunto, o estudo propõe uma cadeia clara de eventos que liga a infecção secundária por dengue à doença grave. Anticorpos de uma infecção prévia podem transportar o vírus da dengue para monócitos via CD32, mas a infecção bem‑sucedida nessas células também depende de TLR2. Uma vez dentro, o vírus expõe seu RNA a TLR3 e TLR8 que, junto com SYK, desencadeiam um poderoso programa inflamatório e antiviral que ativa e perturba os vasos sanguíneos. Ao identificar TLR2, TLR3, TLR8 e SYK como protagonistas centrais tanto na entrada viral quanto na inflamação prejudicial, este trabalho destaca alvos farmacológicos potenciais que, no futuro, podem ajudar a impedir que a dengue leve evolua para suas formas mais perigosas e com risco de vida.
Citação: ter Ellen, B.M., Punekar, M., Castillo, J.A. et al. The contributions of TLR2, TLR8 and TLR3 to direct and antibody-dependent enhancement of dengue virus serotype 2 infection. npj Viruses 4, 24 (2026). https://doi.org/10.1038/s44298-026-00190-9
Palavras-chave: vírus da dengue, potencialização dependente de anticorpos, imunidade inata, receptores tipo Toll, vazamento vascular