Clear Sky Science · pl
Rola TLR2, TLR8 i TLR3 w bezpośrednim i przeciwciałowo wzmacnianym zakażeniu dengi serotypu 2
Dlaczego to badanie ma znaczenie
Denga to choroba przenoszona przez komary, której przebieg może się wahać od silnego, grypopodobnego złego samopoczucia do zagrażających życiu krwawień i wstrząsu. Osoby, które przechodzą dengę po raz drugi, są bardziej narażone na ciężki przebieg choroby, zwłaszcza gdy istniejące przeciwciała zamiast chronić, ułatwiają wirusowi zakażenie komórek odpornościowych. To badanie ujawnia kluczowe cząsteczki na komórkach odpornościowych, które umożliwiają to niebezpieczne „wzmocnienie” zakażenia i stanu zapalnego, i wskazuje nowe możliwości zapobiegania najcięższym postaciom dengi.
Kiedy pomocne przeciwciała stają się szkodliwe
Po pierwszym zakażeniu denga organizm zachowuje przeciwciała rozpoznające wirusa. Przy późniejszym zakażeniu innym typem dengi te przeciwciała mogą nie neutralizować w pełni patogenu. Zamiast tego mogą pokryć wirusa i sprowadzić go do określonych białych krwinek przez receptory przeciwciał — proces zwany przeciwciałowo zależnym wzmocnieniem. Autorzy zastosowali system eksperymentalny oparty na ludzkich komórkach krwi, aby porównać takie wzmocnione zakażenie z typowym zakażeniem wirusem dengi typu 2. Skoncentrowali się na monocytach, rodzaju komórek odpornościowych, które są zarówno siedliskiem wirusa, jak i źródłem substancji zapalnych mogących uszkadzać naczynia krwionośne.
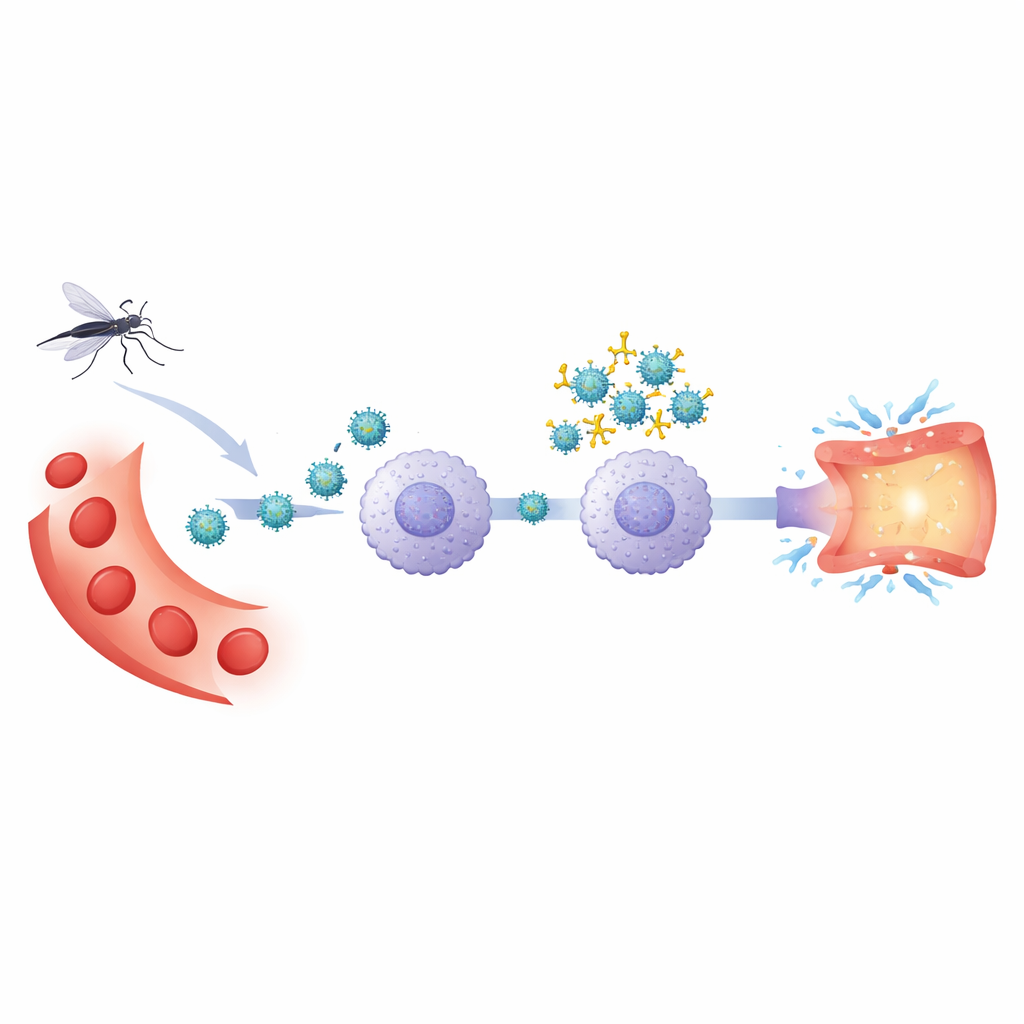
Kluczowe strażniki na komórkach odpornościowych
Zespół badał kilka receptorów — molekularnych „stacji dokujących” — na monocytach. Jednym z nich był CD32, receptor rozpoznający przeciwciała związane z wirusem. Inne to czujniki zwykle wykrywające drobnoustroje, w tym TLR2 na powierzchni komórki oraz TLR3 i TLR8 w przedziałach komórkowych, a także enzym sygnałowy SYK, łączący receptory z dalszymi reakcjami. Poprzez selektywne blokowanie tych cząsteczek za pomocą przeciwciał lub małych inhibitorów badali, które z nich są rzeczywiście niezbędne do wejścia wirusa i do następującej po nim eksplozji zapalnej.
TLR2 jako niezbędny pomocnik wejścia
Eksperymenty wykazały, że gdy wirus dengi wchodził do komórek z pomocą przeciwciał, blokada CD32 lub SYK zmniejszała zakażenie do poziomu obserwowanego bez przeciwciał. Co godne uwagi, zablokowanie TLR2 posunęło się jeszcze dalej: niemal całkowicie zapobiegało zakażeniu zarówno w warunkach z przeciwciałami, jak i bez nich. Wskazuje to, że TLR2 nie jest jedynie czujnikiem alarmowym, lecz także pełni kluczową rolę pomocnika umożliwiającego wirusowi wejście do monocytów w obu sytuacjach. Inna cząsteczka, CD14, wspierała ten proces, podczas gdy inne proponowane koreceptory, takie jak TLR1, TLR6, CD36 czy LILRB1, nie wykazały roli wykrywalnej w tym modelu.
Od wejścia wirusa do uszkodzenia naczyń
Ciężka denga charakteryzuje się nieszczelnymi naczyniami krwionośnymi. Aby powiązać zdarzenia w monocytach z efektami na naczynia, badacze zebrali płyn z zakażonych hodowli komórek krwi i zastosowali go na ludzkich komórkach śródbłonka żyły hodowanych in vitro. Komórki naczyniowe odpowiedziały włączeniem markerów powierzchniowych sprzyjających zapaleniu i przeciekaniu, ale tylko gdy były wystawione na substancje uwolnione przez zakażone monocyty, a nie na same mieszaniny wirus–przeciwciała. Zakażenie wzmacniane przez przeciwciała sprawiało, że monocyty produkowały jeszcze więcej tych sygnałów aktywujących niż zakażenie bezpośrednie. Blokada CD32, SYK lub TLR2 w komórkach krwi silnie zmniejszała tę aktywację śródbłonka i obniżała poziomy cząsteczek przeciwwirusowych i zapalnych, takich jak interferony i TNF‑alfa.
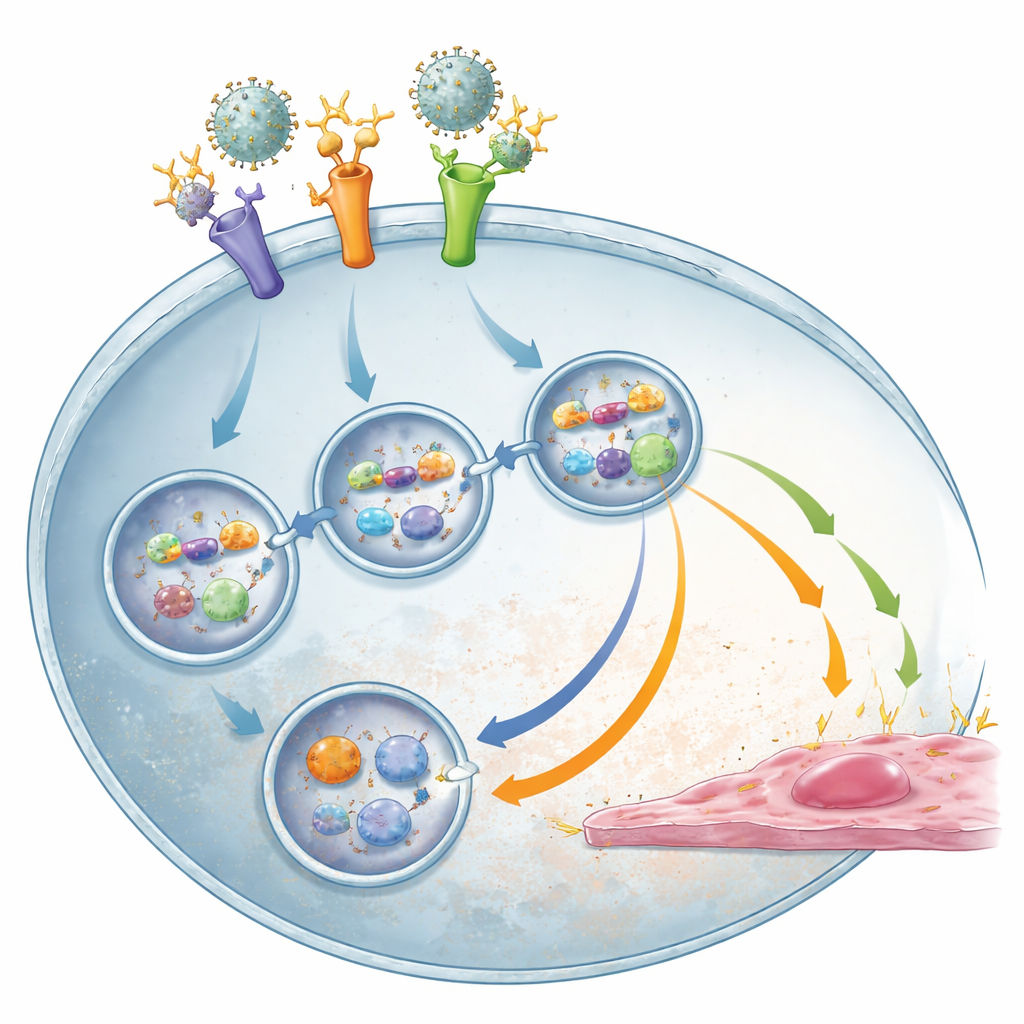
Ukryty RNA wirusa wywołuje burzę
Aby ustalić, co faktycznie uruchamia burzę zapalną, zespół sprawdził, czy cząstki wirusa pozbawione zakaźności nadal mogą aktywować monocyty. Gdy materiał genetyczny wirusa został zniszczony przez naświetlenie ultrafioletem, cząstki nie wywoływały sygnałów aktywujących naczynia, mimo że TLR2 nadal mógł się z nimi wiązać. Wskazywało to na RNA wirusa jako kluczowy wyzwalacz. Rzeczywiście, gdy zablokowano wewnętrzne czujniki RNA — TLR3, a szczególnie TLR8 — monocyty produkowały znacznie mniej substancji zapalnych i przeciwwirusowych, zwłaszcza w warunkach wzmocnionych przez przeciwciała, bez zmniejszenia odsetka zakażonych komórek. Sugeruje to dwustopniowy proces: TLR2 najpierw pomaga wprowadzić kompleksy wirus–przeciwciało do komórki, a gdy RNA wirusa zostaje odsłonięte wewnątrz, TLR3 i TLR8 je wykrywają i napędzają szkodliwą odpowiedź immunologiczną, przy czym SYK działa jako wspólne centrum sygnałowe.
Co to oznacza dla walki z ciężką dengą
Podsumowując, badanie proponuje jasny ciąg zdarzeń łączący wtórne zakażenie dengi z ciężką postacią choroby. Przeciwciała z wcześniejszego zakażenia mogą transportować wirusa dengi do monocytów przez CD32, ale pomyślne zakażenie tych komórek zależy również od TLR2. Po wejściu wirus odsłania swoje RNA przed TLR3 i TLR8, które wraz z SYK uruchamiają silny program zapalny i przeciwwirusowy aktywujący i zaburzający pracę naczyń krwionośnych. Identyfikując TLR2, TLR3, TLR8 i SYK jako kluczowych graczy zarówno w wejściu wirusa, jak i w szkodliwym zapaleniu, praca ta wskazuje potencjalne cele leków, które mogłyby w przyszłości pomóc zapobiegać przejściu łagodnej dengi w jej najgroźniejszą, zagrażającą życiu postać.
Cytowanie: ter Ellen, B.M., Punekar, M., Castillo, J.A. et al. The contributions of TLR2, TLR8 and TLR3 to direct and antibody-dependent enhancement of dengue virus serotype 2 infection. npj Viruses 4, 24 (2026). https://doi.org/10.1038/s44298-026-00190-9
Słowa kluczowe: wirus dengi, przeciwciałowo zależne wzmocnienie, odporność wrodzona, receptory Toll‑podobne, przeciekanie naczyń