Clear Sky Science · nl
De bijdragen van TLR2, TLR8 en TLR3 aan directe en antistof‑afhankelijke versterking van denguevirus serotype 2‑infectie
Waarom dit onderzoek ertoe doet
Denguekoorts is een door muggen overgedragen ziekte die kan variëren van een ernstige griepachtige aandoening tot levensbedreigende bloedingen en shock. Mensen die een tweede keer dengue krijgen lopen een hoger risico op ernstige ziekte, vooral wanneer hun bestaande antistoffen — in plaats van bescherming te bieden — het virus juist helpen immuuncellen te infecteren. Deze studie onthult belangrijke moleculen op immuuncellen die deze gevaarlijke "versterking" van infectie en ontsteking mogelijk maken en wijst op nieuwe manieren om de ernstigste vormen van dengue te voorkomen.
Wanneer behulpzame antistoffen schadelijk worden
Na een eerste dengueinfectie houdt het lichaam antistoffen aan die het virus herkennen. Bij een latere infectie met een ander dengue‑type neutraliseren deze antistoffen de indringer mogelijk niet volledig. In plaats daarvan kunnen ze het virus omhullen en het via antistofreceptoren naar bepaalde witte bloedcellen loodsen, een proces dat antistof‑afhankelijke versterking wordt genoemd. De auteurs gebruikten een experimenteel systeem gebaseerd op menselijk bloed om deze versterkte infectie te vergelijken met gewone infectie door denguevirus type 2. Ze concentreerden zich op monocyten, een type immuuncel dat zowel gastheer voor het virus is als ontstekingsstoffen vrijgeeft die bloedvaten kunnen beschadigen.
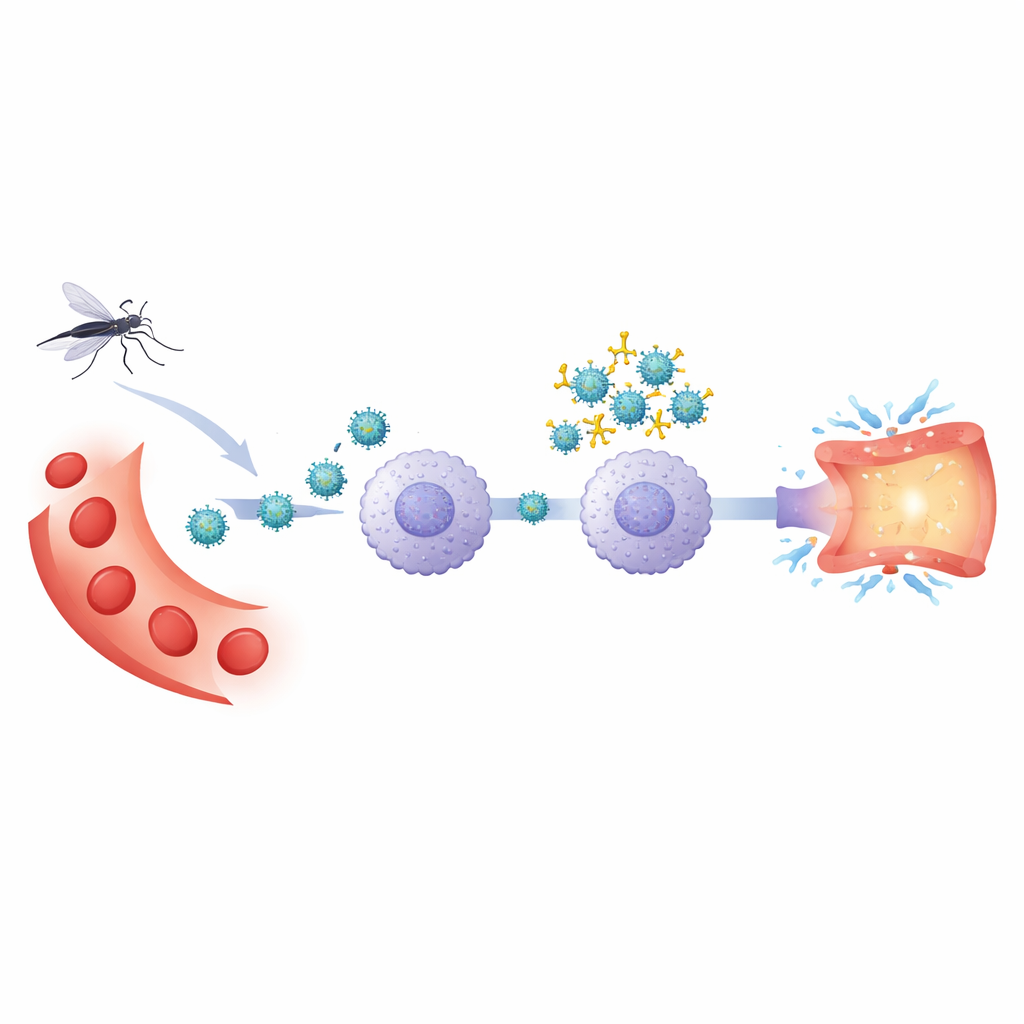
Sleutelpoorten op immuuncellen
Het team onderzocht verschillende receptoren — moleculaire "aanmeerpalen" — op monocyten. Eén was CD32, een receptor die antistoffen herkent die aan het virus gebonden zijn. Andere waren sensoren die doorgaans ziekteverwekkers detecteren, waaronder TLR2 op het celoppervlak en TLR3 en TLR8 in intracellulaire compartimenten, evenals een signaalenzym genaamd SYK dat receptoren met downstreamreacties verbindt. Door deze moleculen selectief te blokkeren met antistoffen of kleine remmers stelden ze vast welke werkelijk noodzakelijk waren voor virusbinnenkomst en voor de daaropvolgende ontstekingsuitbarsting.
TLR2 als essentiële hulp bij binnendringen
De experimenten toonden aan dat wanneer denguevirus cellen binnendrong met hulp van antistoffen, het blokkeren van CD32 of SYK de infectie terugbracht tot het niveau zonder antistoffen. Opmerkelijk was dat het blokkeren van TLR2 nog verder ging: het verhinderde de infectie bijna volledig, zowel met als zonder antistoffen. Dit wijst erop dat TLR2 niet slechts een waarschuwingssensor is maar ook fungeert als een cruciale hulp voor het virus om monocyten binnen te dringen onder alle omstandigheden. Een ander molecuul, CD14, ondersteunde dit proces, terwijl andere voorgestelde co‑receptoren zoals TLR1, TLR6, CD36 of LILRB1 in dit model geen detecteerbare rol leken te spelen.
Van virale binnenkomst naar vaatbeschadiging
Ernstige dengue wordt gekenmerkt door lekke bloedvaten. Om gebeurtenissen in monocyten te koppelen aan effecten op bloedvaten, verzamelden de onderzoekers de vloeistof uit geïnfecteerde bloedcelculturen en brachten deze aan op menselijke aderendotheelcellen die in het laboratorium gekweekt waren. Deze vaatcellen reageerden door oppervlakte markers aan te zetten die ontsteking en lekkage bevorderen, maar alleen wanneer ze werden blootgesteld aan stoffen die door geïnfecteerde monocyten werden vrijgegeven, niet aan virus‑antistofmengsels alleen. Antistof‑versterkte infectie deed monocyten nog meer van deze activerende signalen produceren dan directe infectie. Het blokkeren van CD32, SYK of TLR2 in de bloedcellen verminderde deze endotheelactivatie sterk en verlaagde ook niveaus van antivirale en ontstekingsmoleculen zoals interferonen en TNF‑alfa.
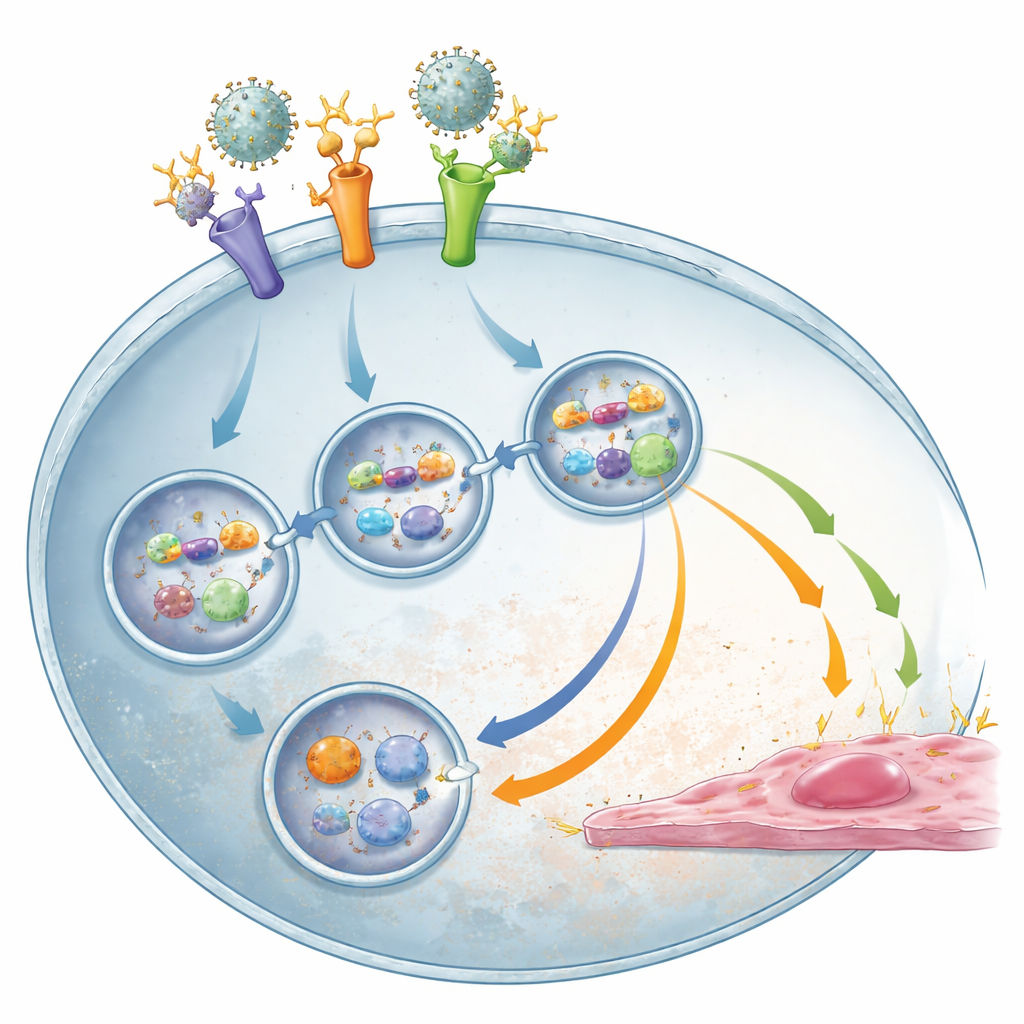
Verborgen viraal RNA ontsteekt de storm
Om te achterhalen wat de ontstekingsstorm daadwerkelijk triggert, testte het team of niet‑infectieuze virusdeeltjes monocyten konden activeren. Toen het virale genetische materiaal door ultravioletbehandeling werd vernietigd, faalden de deeltjes erin vaat‑activerende signalen te veroorzaken, ook al kon TLR2 ze nog steeds binden. Dit wees op viraal RNA als de sleuteltrigger. Inderdaad, toen de interne RNA‑sensoren TLR3 en vooral TLR8 werden geblokkeerd, produceerden monocyten veel minder ontstekings‑ en antivirale stoffen, met name onder antistof‑versterkte omstandigheden, zonder het aantal geïnfecteerde cellen te verminderen. Dit suggereert een tweestapsproces: TLR2 helpt eerst virus‑antistofcomplexen de cel binnen te brengen, en zodra viraal RNA binnen wordt blootgelegd, detecteren TLR3 en TLR8 het en drijven ze de schadelijke immuunreactie aan, met SYK als gedeelde signaalhub.
Wat dit betekent voor het bestrijden van ernstige dengue
Samengevat stelt de studie een duidelijke keten van gebeurtenissen voor die secundaire dengueinfectie koppelt aan ernstige ziekte. Antistoffen van een eerdere infectie kunnen denguevirus via CD32 naar monocyten transporteren, maar succesvolle infectie in deze cellen hangt ook af van TLR2. Eenmaal binnen stelt het virus zijn RNA bloot aan TLR3 en TLR8 die, samen met SYK, een krachtige ontstekings‑ en antivirale respons ontketenen die bloedvaten activeert en verstoort. Door TLR2, TLR3, TLR8 en SYK te identificeren als centrale spelers in zowel virusbinnenkomst als schadelijke ontsteking, benadrukt dit werk potentiële medicijntargets die op termijn kunnen helpen voorkomen dat milde dengue uitgroeit tot de meest gevaarlijke, levensbedreigende vormen.
Bronvermelding: ter Ellen, B.M., Punekar, M., Castillo, J.A. et al. The contributions of TLR2, TLR8 and TLR3 to direct and antibody-dependent enhancement of dengue virus serotype 2 infection. npj Viruses 4, 24 (2026). https://doi.org/10.1038/s44298-026-00190-9
Trefwoorden: denguevirus, antistof‑afhankelijke versterking, aangeboren immuniteit, Toll‑achtige receptoren, vasculaire lekkage