Clear Sky Science · ru
Ренальная денервация ослабляет сердечный фиброз и улучшает функцию левого желудочка у крыс с инфарктом миокарда
Почему успокоение почечных нервов может защитить сердце
Инфаркты по-прежнему остаются одной из основных причин смерти и инвалидности, отчасти потому, что повреждённая сердечная мышца заживает образованием жёсткого рубца. Этот рубцевый процесс может ослаблять насосную функцию сердца и приводить к сердечной недостаточности. Описанное здесь исследование изучает неожиданный способ ограничить это повреждение: ослабить проводку «борьбы или бегства», разрежая или отключая нервы вокруг почек — процедуру, известную как ренальная денервация. У крыс такой подход, по-видимому, смягчил долгосрочный рубцевый ответ в сердце и сохранил его функцию, что указывает на новый путь лечения пациентов после инфаркта.
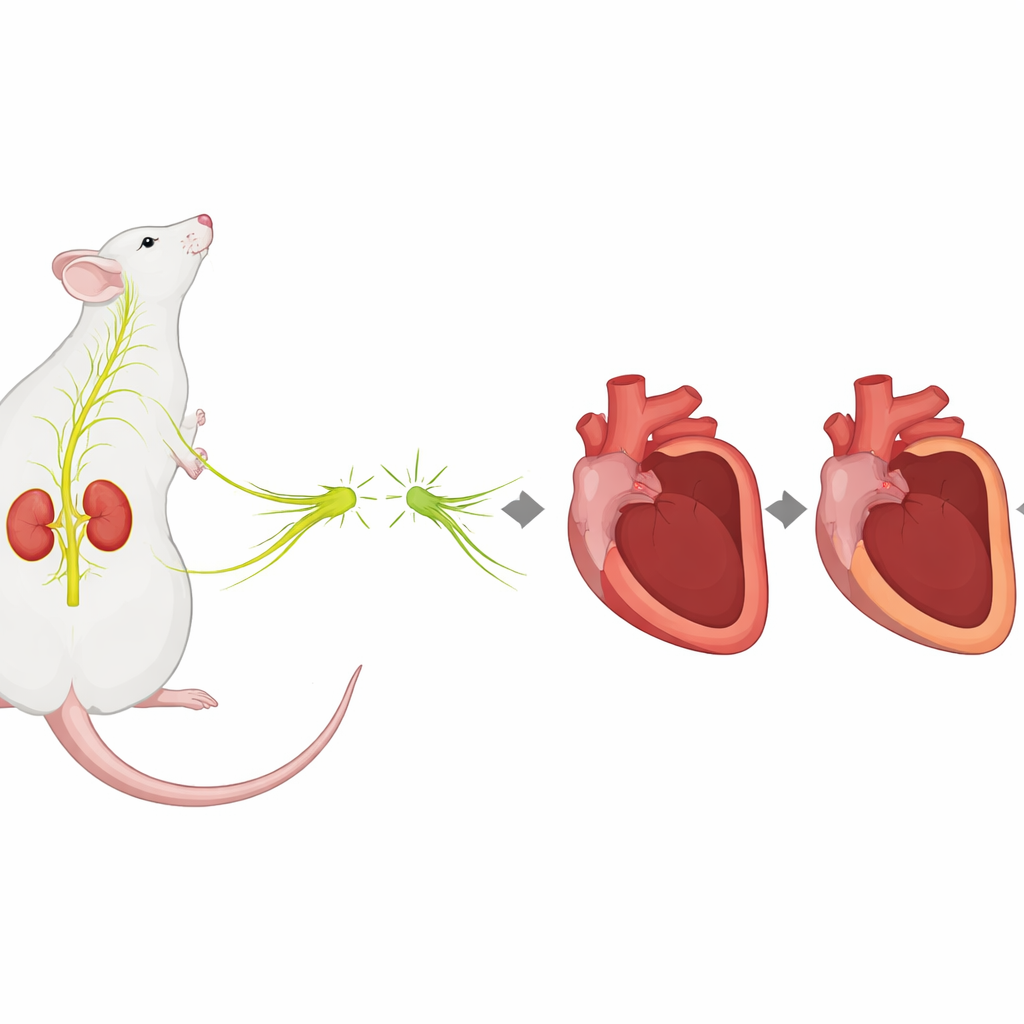
Путь стресса от почечных нервов к повреждению сердца
После инфаркта система стресса организма, управляемая симпатической нервной системой, включается на полную. Эта система выделяет химические мессенджеры, которые повышают частоту сердечных сокращений и кровяное давление, но она также разжигает воспаление и влияет на то, как заживает повреждённое сердце. Нервы, обвивающие почечные артерии, являются ключевым узлом в этой сети стресса, посылая сигналы, которые повышают уровни стрессового нейромедиатора норадреналина по всему организму. Ранее было показано, что перерезание или дезактивация этих почечных нервов может не только снижать кровяное давление, но и защищать сердце в других болезненных состояниях. В настоящем исследовании поставили вопрос, может ли ренальная денервация, выполненная до инфаркта у крыс, изменить способ ремоделирования и рубцевания сердца в последующие недели.
Испытание перерезания нервов в модели инфаркта у крыс
Исследователи разделили крыс на три группы: здоровые контрольные животные, крысы с индуцированным инфарктом и крысы, у которых провели ренальную денервацию за два дня до той же процедуры инфаркта. Через четыре недели они провели МРТ высокого разрешения, чтобы измерить, насколько эффективно левый желудочек качает кровь. У крыс с инфарктом без перерезания нервов наблюдалось заметное падение насосной функции, тогда как у тех, кому провели ренальную денервацию, фракция выброса оставалась значительно выше — их сердца сокращались эффективнее. Химические тесты почек подтвердили, что активность нервов и уровни стрессовых химических веществ были значительно снижены только у денервированных животных, что показало успешное подавление стрессового пути.
Меньше рубцевания и более спокойные сигналы восстановления в сердце
Чтобы понять, почему функция сердца сохранилась, команда изучила структуру и молекулярные сигналы в сердечной мышце. Окрашивание срезов сердца на коллаген, основной компонент рубцовой ткани, показало, что у крыс с перерезанными нервами площади рубцов были значительно меньше, чем у нетронутых животных с инфарктом. Генетическое «полнотранскриптомное» профилирование выявило широкие различия в активности сотен генов. При инфаркте без денервации включались программы, связанные с воспалением и строительством внешней опорной сети, которая превращается в рубцовую ткань. Напротив, эти же генные программы были явно подавлены при перерезании почечных нервов, что указывает на то, что вся среда заживления в сердце сместилась в менее фибротическую и менее воспалительную сторону.
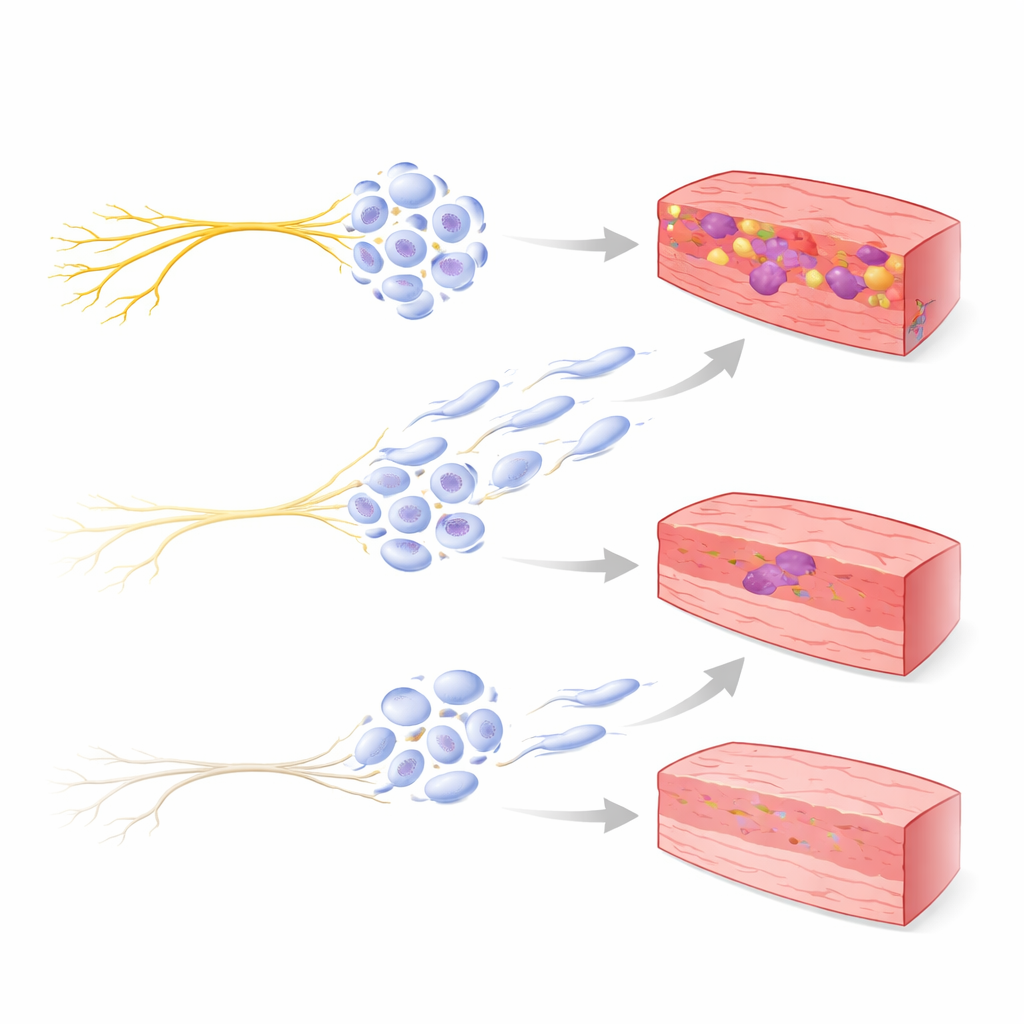
Иммунные клетки как связующее звено между стрессовыми сигналами и рубцеванием
Исследование также сосредоточилось на макрофагах — иммунных клетках, которые помогают очищать мёртвую ткань и направляют процессы восстановления после инфаркта. В группе с необработанным инфарктом исследователи наблюдали больше макрофагов и, в частности, более высокий уровень клеток, несущих маркер CD206, связанный с «рубцеобразующим», тканестроительным поведением. Чем больше таких CD206‑положительных клеток, тем сильнее был фиброз в сердце. В группе с перерезанными нервами и уровень CD206, и тяжесть рубцевания оказались ниже. Чтобы проверить эту связь, команда использовала культуру человеческой клеточной линии и подвергла макрофагоподобные клетки воздействию препарата, имитирующего стрессовые сигналы, действующие на бета‑адренергические рецепторы. Эти клетки сместились в сторону профибротического генного паттерна, но это смещение во многом блокировалось при добавлении блокады bета‑1 рецептора, что указывает на прямой путь от стрессовой сигнализации к фибротическому поведению иммунных клеток.
Что это может означать для будущей помощи при инфаркте
В совокупности эти результаты указывают, что снижение активности почечных стрессовых нервов до инфаркта может ограничивать долгосрочное повреждение, уменьшая вредный фиброз и сохраняя насосную силу сердца, по крайней мере у крыс. Работа подчёркивает роль макрофагов как ключевых посредников: при сильных стрессовых сигналах они толкают сердце к жёстким, богатым коллагеном рубцам, но при ослаблении этих сигналов они менее склонны стимулировать фиброз. Хотя ренальная денервация уже используется у некоторых пациентов с устойчивой артериальной гипертензией, её потенциальная роль после инфаркта у людей остаётся непроверенной. Это исследование закладывает основу для изучения того, может ли воздействие на стрессовые пути и их влияние на иммунные клетки однажды стать частью стандартной терапии, помогающей сердцам лучше восстанавливаться после повреждения.
Цитирование: Therre, M., Hohl, M., Aghagolzadeh, P. et al. Renal denervation attenuates cardiac fibrosis and improves left ventricular function in rats with myocardial infarction. Sci Rep 16, 13416 (2026). https://doi.org/10.1038/s41598-026-50195-w
Ключевые слова: ренальная денервация, инфаркт миокарда, сердечный фиброз, макрофаги, симпатическая нервная система