Clear Sky Science · fr
La dénervation rénale atténue la fibrose cardiaque et améliore la fonction ventriculaire gauche chez des rats ayant subi un infarctus du myocarde
Pourquoi calmer les nerfs rénaux pourrait protéger le cœur
Les infarctus restent une cause majeure de mortalité et d’incapacité, en partie parce que le muscle cardiaque endommagé cicatrise en formant une zone rigide. Cette cicatrisation peut affaiblir la capacité de pompage du cœur et conduire à une insuffisance cardiaque. L’étude décrite ici explore une façon surprenante de limiter ces dégâts : réduire l’activité du système de « combat ou fuite » en sectionnant les nerfs autour des reins, une procédure appelée dénervation rénale. Chez le rat, cette approche a semblé atténuer la réponse cicatricielle à long terme du cœur et préserver sa fonction, suggérant une nouvelle piste pour traiter les patients après un infarctus.
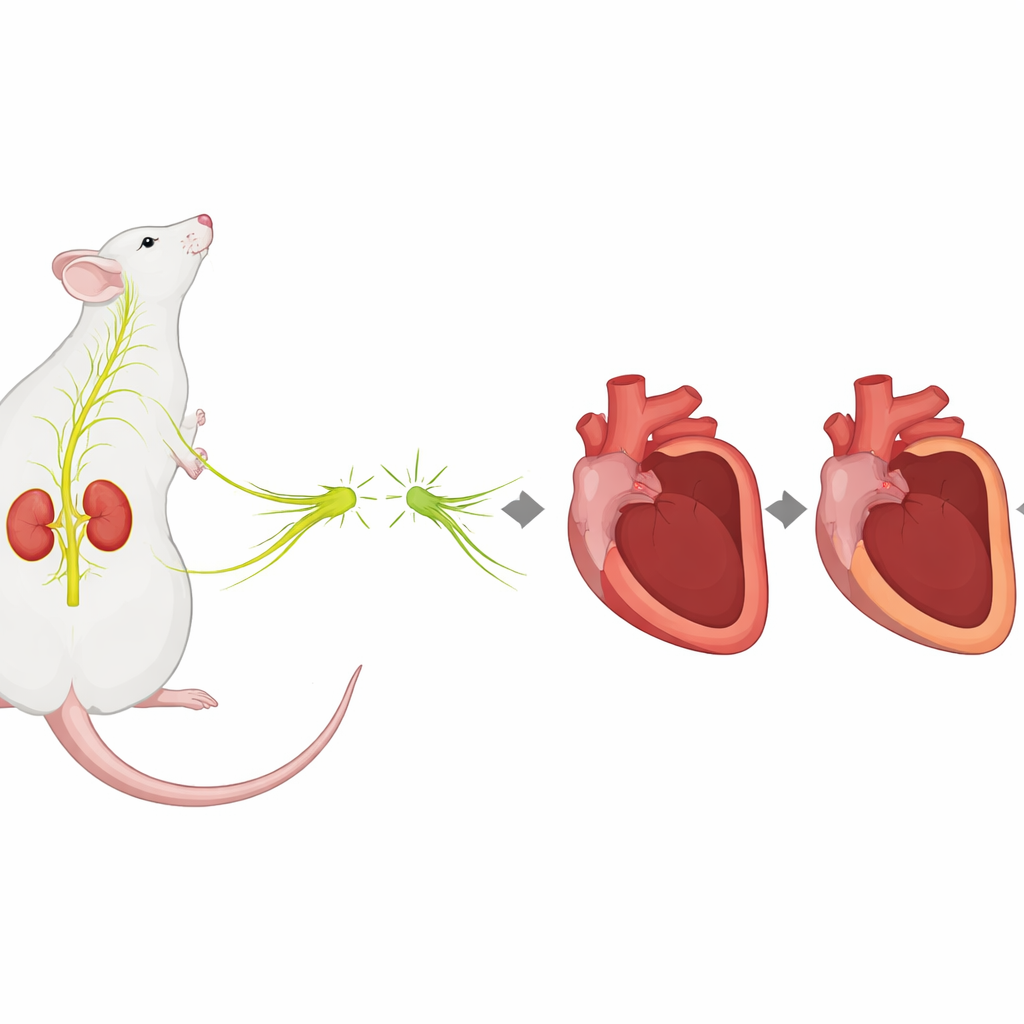
Une voie de stress reliant les nerfs rénaux aux lésions cardiaques
Après un infarctus, le système de stress de l’organisme, piloté par le système nerveux sympathique, passe en suractivité. Ce système libère des messagers chimiques qui augmentent la fréquence cardiaque et la pression artérielle, mais il stimule aussi l’inflammation et influence la façon dont le cœur lésé se répare. Les nerfs entourant les artères rénales constituent un nœud clé de ce réseau de stress, envoyant des signaux qui augmentent les niveaux de noradrénaline dans tout le corps. Des travaux antérieurs ont suggéré que couper ou désactiver ces nerfs rénaux peut non seulement abaisser la pression artérielle, mais aussi protéger le cœur dans d’autres contextes pathologiques. L’étude actuelle a cherché à savoir si effectuer une dénervation rénale avant un infarctus chez le rat pouvait modifier la manière dont le cœur se remodèle et cicatrise dans les semaines qui suivent.
Tester la section des nerfs dans un modèle de crise cardiaque chez le rat
Les chercheurs ont réparti les rats en trois groupes : témoins sains, rats avec infarctus induit et rats ayant subi une dénervation rénale deux jours avant la même procédure d’infarctus. Quatre semaines plus tard, ils ont utilisé des IRM haute résolution pour mesurer l’efficacité du ventricule gauche à éjecter le sang. Les rats ayant eu un infarctus sans dénervation montraient une baisse marquée de la fonction de pompage, tandis que ceux ayant reçu la dénervation rénale conservaient une fraction d’éjection beaucoup plus élevée, ce qui signifie que leur cœur se contractait plus efficacement. Des analyses chimiques des reins ont confirmé que l’activité nerveuse et les niveaux de médiateurs du stress étaient fortement réduits uniquement chez les animaux dénervés, montrant que la procédure avait bien atténué la voie de stress.
Moins de cicatrisation et des signaux de réparation apaisés dans le cœur
Pour comprendre pourquoi la fonction cardiaque était préservée, l’équipe a examiné la structure et les signaux moléculaires au sein du muscle cardiaque. La coloration de coupes cardiaques pour le collagène, composant principal du tissu cicatriciel, a révélé que les cœurs des rats dénervés présentaient des zones cicatricielles beaucoup plus réduites que celles des rats infarctés non traités. Un profilage génétique « transcriptomique global » a montré des différences larges dans l’activité de centaines de gènes. Un infarctus sans dénervation activait des programmes liés à l’inflammation et à la construction de la matrice extracellulaire qui deviendra la cicatrice. En revanche, ces mêmes programmes géniques étaient nettement atténués lorsque les nerfs rénaux avaient été sectionnés, suggérant que l’environnement de cicatrisation du cœur avait basculé vers un état moins fibrotique et moins inflammatoire.
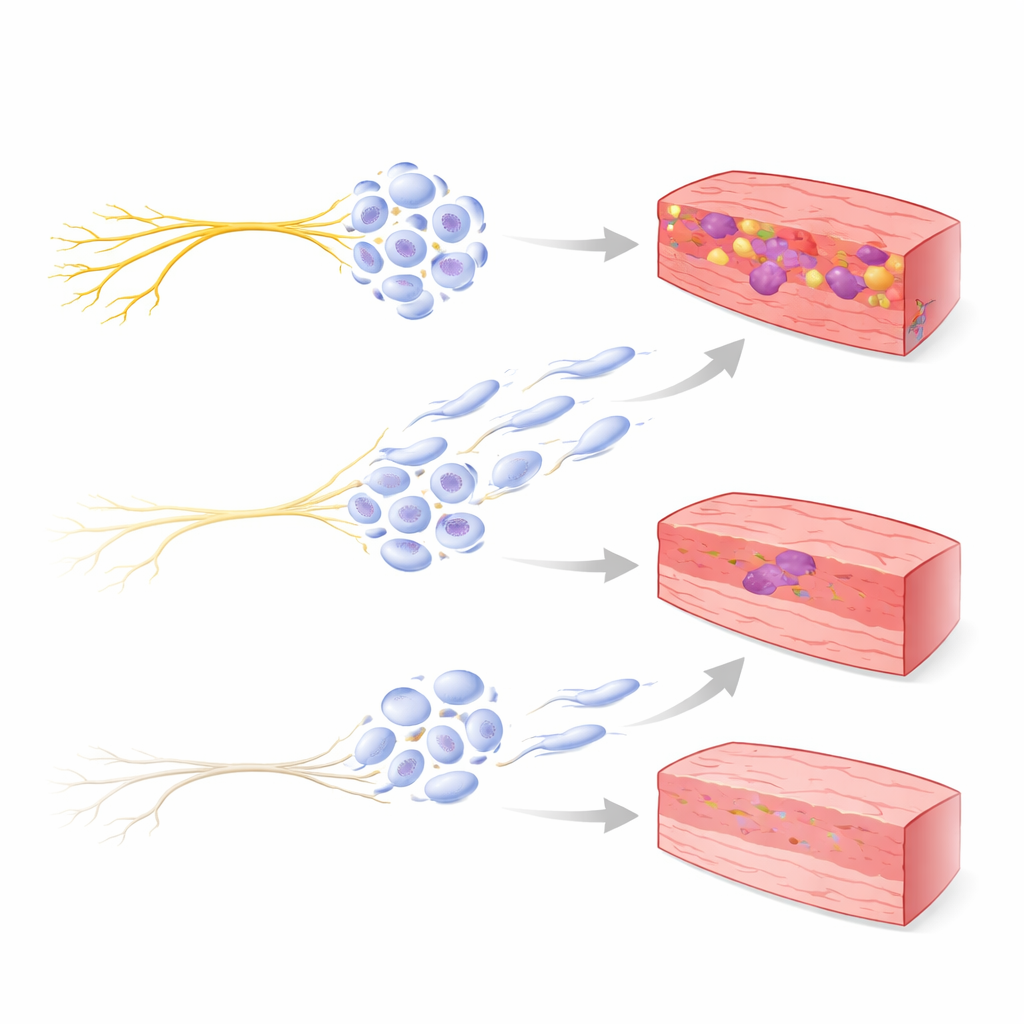
Les cellules immunitaires comme lien entre signaux de stress et fibrose
L’étude s’est aussi intéressée aux macrophages, cellules immunitaires qui aident à débarrasser les tissus morts et à guider la réparation après un infarctus. Dans le groupe infarctus non traité, les chercheurs ont observé plus de macrophages et, en particulier, un nombre plus élevé de cellules exprimant un marqueur appelé CD206, associé à un comportement pro‑fibrose et constructeur de tissu. Plus il y avait de ces cellules CD206‑positives, plus la fibrose cardiaque était importante. Dans le groupe dénervé, tant les niveaux de CD206 que la charge cicatricielle étaient réduits. Pour explorer ce lien, l’équipe a utilisé une lignée cellulaire humaine en laboratoire et a exposé des cellules de type macrophage à un médicament imitant les signaux de stress agissant sur les récepteurs bêta‑adrénergiques. Ces cellules ont basculé vers un profil génique pro‑cicatrice, mais ce basculement a été largement bloqué lorsque l’on a ajouté un bloqueur des récepteurs bêta‑1, indiquant une voie directe du signal de stress vers le comportement fibrotique des cellules immunitaires.
Ce que cela pourrait signifier pour la prise en charge future des infarctus
Pris ensemble, ces résultats suggèrent que réduire l’activité des nerfs rénaux liés au stress avant un infarctus peut limiter les dommages à long terme en réduisant la cicatrice nuisible et en préservant la puissance de pompage du cœur, du moins chez le rat. Le travail met en évidence les macrophages comme intermédiaires clés : exposés à des signaux de stress forts, ils orientent le cœur vers des cicatrices rigides et riches en collagène, mais lorsque ces signaux sont atténués, ils semblent moins enclins à promouvoir la fibrose. Si la dénervation rénale est déjà utilisée chez certains patients pour une hypertension résistante, son rôle potentiel après un infarctus n’a pas encore été testé chez l’humain. Cette étude établit les bases pour explorer si cibler les voies de stress et leur influence sur les cellules immunitaires pourrait un jour faire partie des soins standard pour aider le cœur à mieux guérir après une lésion.
Citation: Therre, M., Hohl, M., Aghagolzadeh, P. et al. Renal denervation attenuates cardiac fibrosis and improves left ventricular function in rats with myocardial infarction. Sci Rep 16, 13416 (2026). https://doi.org/10.1038/s41598-026-50195-w
Mots-clés: dénervation rénale, infarctus du myocarde, fibrose cardiaque, macrophages, système nerveux sympathique