Clear Sky Science · ru
Включаемый хинолиновый зонд для селективного обнаружения гипохлорита в живых клетках
Новый способ увидеть скрытое химическое вещество в наших клетках
Наши клетки постоянно производят и разрушают высоко реакционноспособные молекулы, которые помогают бороться с инфекциями, но при накоплении могут повреждать ткани. Одна из таких молекул — гипохлорит — тесно связана с воспалением, иммунной защитой и заболеваниями, связанными с оксидативным стрессом. В этом исследовании описана недавно разработанная малая красительная молекула, которая держится в «темноте», пока не встретит гипохлорит, после чего включается и ярко светится зеленым. Такое простое переключение значительно упрощает наблюдение за этой ускользающей молекулой в реальном времени внутри живых клеток.
Почему важно отслеживать агрессивный окислитель
Реактивные кислородные виды — это побочные продукты химических реакций при использовании кислорода в клетках. В нужных количествах они помогают лейкоцитам убивать микробы и служат сигналами, регулирующими нормальное поведение клеток. Но при избытке они атакуют ДНК, белки и липиды, способствуя развитию состояний от нейродегенерации до сердечно-сосудистых заболеваний. Гипохлорит — один из таких реактивных видов, продуцируемых иммунными клетками, и он относительно устойчив в тканях. Поскольку он одновременно полезен и потенциально вреден, учёным нужны инструменты, которые точно покажут, когда, где и в каком количестве гипохлорит присутствует в клетках.
Проектирование малой «умной» молекулы-переключателя света
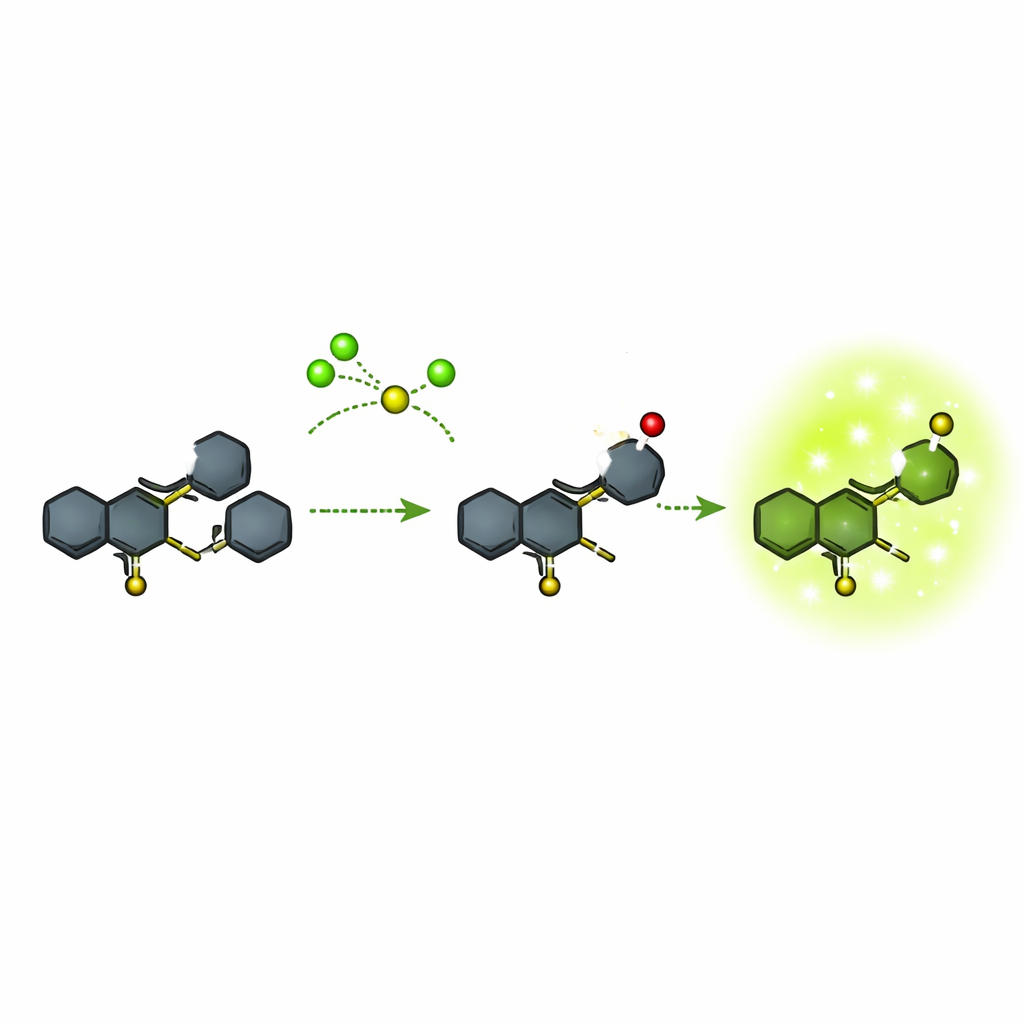
Многие существующие флуоресцентные зонды для гипохлорита относительно громоздки или требуют сложных цветовых изменений, затрудняющих точные измерения. Авторы сосредоточились на компактной химической основе, основанной на кольцевой системе хинолина, связанной с другой системой — фенотиазином. Они синтезировали эту структуру в несколько стадий из коммерчески доступных исходных материалов, тщательно контролируя каждую стадию с помощью ядерного магнитного резонанса, масс-спектрометрии и оптических измерений. Итоговый зонд, обозначенный как соединение 5, практически не светился сам по себе, но был сконструирован так, чтобы определённый атом серы мог избирательно атаковаться гипохлоритом. Эта реакция преобразует молекулу в новую форму (соединение 6), которая ярко флуоресцирует в зелёной области спектра.
От темноты к яркости за секунды и только для нужной цели
Команда проверила, насколько селективно и как быстро зонд реагирует на разные химические вещества. В растворе соединение 5 практически не флуоресцировало в широком диапазоне растворителей. При воздействии множества обычных ионов, малых серосодержащих молекул и других реактивных кислородных видов оно оставалось тёмным. Только гипохлорит вызвал сильное, резкое зелёное излучение около 523 нм, причём интенсивность росла пропорционально концентрации гипохлорита в полезном диапазоне. Реакция была быстрой: измеримое свечение появлялось примерно через 10 секунд и продолжало нарастать в течение нескольких минут. При очень высоких уровнях гипохлорита зонд мог претерпеть дальнейшую окислительную трансформацию в сульфон, который светился менее ярко, но это происходило вне основного рабочего диапазона. В целом предел обнаружения был чрезвычайно низким, заметно ниже одного микромоля, а сигнал был достаточно интенсивным, чтобы быть видимым невооружённым глазом.
Наблюдение гипохлорита внутри живых клеток
Чтобы проверить работоспособность этой химии в биологической среде, исследователи протестировали зонд в недавно выделенных клетках костного мозга мыши. При низкой дозе зонда, не вредящей клеткам, они отслеживали его поведение с помощью проточной цитометрии и флуоресцентной микроскопии. Клетки, обработанные только зондом, показали лишь небольшое увеличение зелёного свечения, что указывает на то, что нормальные внутренние уровни гипохлорита низки, но детектируемы. Когда те же клетки подвергали воздействию возрастающих количеств добавленного гипохлорита, значительная часть клеток ярко засветилась, причём сигнал масштабировался с дозой. Последующие тесты показали, что продукт свечения стабилен при непрерывном облучении как в растворе, так и в клетках, и что его оптические свойства особенно благоприятны в водных, биологически релевантных условиях.
Что это значит для изучения здоровья и болезней
В сумме эти результаты представляют компактный, быстро действующий и селективный «включаемый» зонд для гипохлорита, который работает при мягких условиях и надёжен в живых клетках. Вместо зависимости от тонких сдвигов цвета или громоздких красителей конструкция использует простое переключение от темного состояния к яркому зелёному свечению, непосредственно связанное с конкретным химическим изменением на одном атоме молекулы. Поскольку зонд может выделять клетки с повышенным уровнем гипохлорита, он предлагает практический инструмент для изучения того, как возникает оксидативный стресс при инфекции, воспалении и других заболеваниях, и может направить разработку более изящных сенсоров для других реактивных химических видов в будущем.
Цитирование: Olubiyo, F.F., Klu, S.Y.S., Burgess, R.J. et al. Turn-on quinoline probe for selective sensing of hypochlorite in live cells. Sci Rep 16, 10715 (2026). https://doi.org/10.1038/s41598-026-45327-1
Ключевые слова: обнаружение гипохлорита, флуоресцентные зонды, реактивные кислородные виды, микроскопия клеток, оксидативный стресс