Clear Sky Science · es
Sonda quinolina activable para la detección selectiva de hipoclorito en células vivas
Una nueva forma de ver un químico oculto en nuestras células
Nuestras células producen y degradan constantemente moléculas altamente reactivas que ayudan a combatir infecciones, pero que también pueden dañar los tejidos cuando se acumulan. Una de ellas, el hipoclorito, está estrechamente vinculada con la inflamación, la defensa inmune y enfermedades asociadas al estrés oxidativo. Este estudio describe una pequeña molécula colorante diseñada para permanecer apagada hasta encontrarse con hipoclorito, momento en el que se enciende con un brillante resplandor verde. Ese sencillo interruptor lumínico facilita mucho que los investigadores observen este químico esquivo en tiempo real dentro de células vivas.
Por qué importa seguir a un oxidante agresivo
Las especies reactivas de oxígeno son subproductos químicos formados cuando nuestras células usan oxígeno. En niveles adecuados ayudan a los glóbulos blancos a matar microbios y actúan como señales que guían el comportamiento celular normal. Pero cuando sus niveles son demasiado altos, atacan ADN, proteínas y lípidos, contribuyendo a afecciones que van desde la neurodegeneración hasta las enfermedades cardíacas. El hipoclorito es una de esas especies reactivas producidas por células inmunitarias y es inusualmente estable dentro de los tejidos vivos. Como es útil pero potencialmente dañino, los científicos necesitan herramientas que puedan revelar con precisión cuándo, dónde y en qué cantidad está presente el hipoclorito en las células.
Diseñar una pequeña molécula con un interruptor inteligente
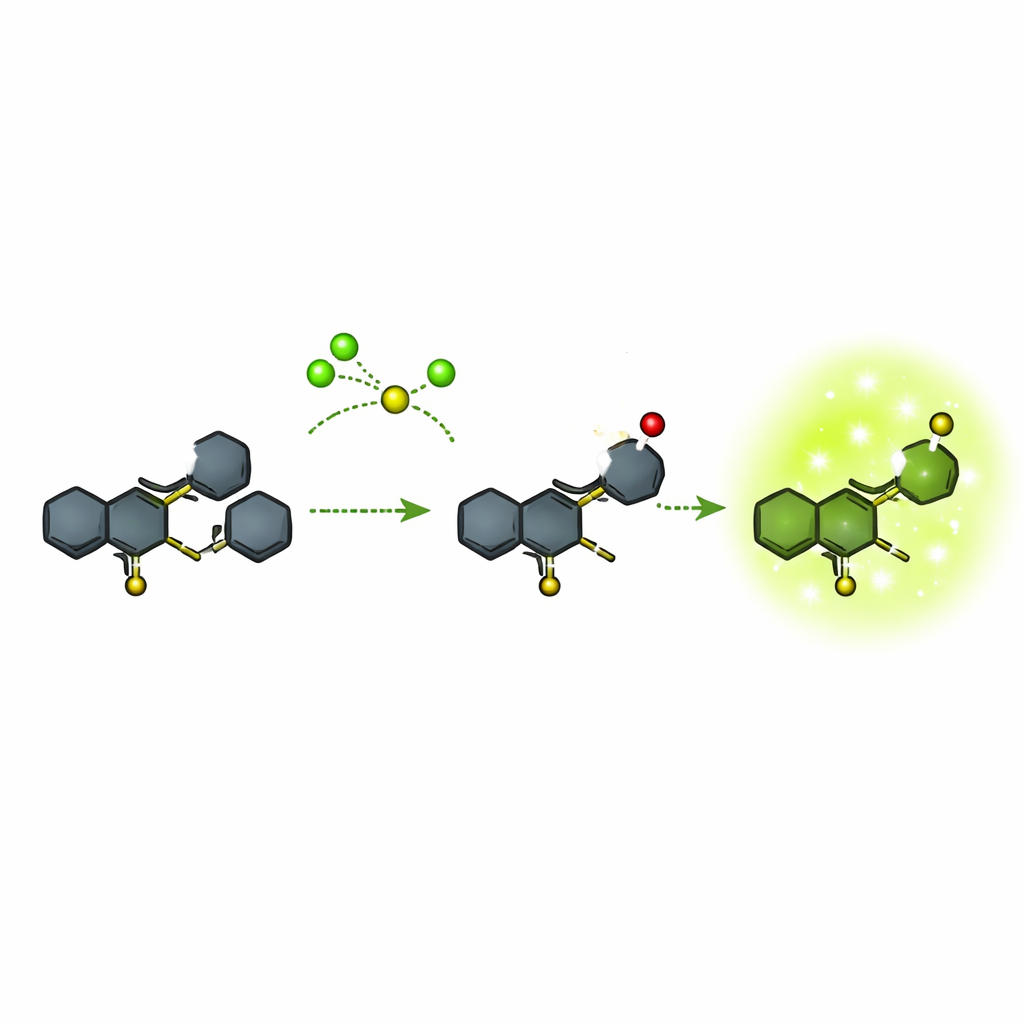
Muchas sondas fluorescentes existentes para hipoclorito son relativamente voluminosas o requieren cambios de color complicados que dificultan las medidas precisas. Los autores se centraron en un marco químico compacto basado en un sistema anular llamado quinolina, unido a otro sistema anular conocido como fenotiazina. Construyeron esta estructura en pocos pasos a partir de materiales comerciales, verificando rigurosamente cada etapa con resonancia magnética nuclear, espectrometría de masas y medidas ópticas. La sonda final, denominada compuesto 5, casi no emite luz por sí sola, pero está diseñada de manera que un átomo de azufre en particular puede ser atacado selectivamente por hipoclorito. Esa reacción transforma la molécula en una nueva forma (compuesto 6) que emite con intensidad en la región verde del espectro.
De oscura a brillante en segundos, y solo para el objetivo correcto
El equipo probó la especificidad y la rapidez de respuesta de la sonda frente a diferentes químicos. En solución, el compuesto 5 mostró esencialmente nula fluorescencia en una amplia gama de disolventes. Al exponerse a muchos iones comunes, pequeñas moléculas que contienen azufre y otras especies reactivas de oxígeno, permaneció apagada. Solo el hipoclorito provocó una emisión verde fuerte y nítida alrededor de 523 nanómetros, y el brillo aumentó en proporción a la concentración de hipoclorito dentro de un rango útil. La reacción fue rápida: la luz detectable apareció en aproximadamente 10 segundos y continuó aumentando durante minutos. A niveles muy altos de hipoclorito, la sonda podía oxidarse un paso más hasta una forma sobreoxidada (un sulfona) menos brillante, pero esto ocurría fuera del rango operativo principal. En conjunto, el límite de detección fue extremadamente bajo, muy por debajo de un micromolar, y la señal fue lo bastante intensa como para verse a simple vista.
Observando el hipoclorito dentro de células vivas
Para comprobar si esta química funcionaba en un entorno biológico, los investigadores probaron la sonda en células de médula ósea de ratón recién aisladas. Con una dosis baja de sonda que no dañó las células, emplearon citometría de flujo y microscopía de fluorescencia para seguir su comportamiento. Las células tratadas solo con la sonda mostraron un ligero aumento de la luz verde, lo que sugiere que los niveles internos normales de hipoclorito son bajos pero detectables. Cuando las mismas células se expusieron a cantidades crecientes de hipoclorito añadido, una gran fracción de células se iluminó intensamente, y la señal escaló con la dosis. Pruebas de seguimiento mostraron que el producto luminoso fue estable bajo iluminación continua tanto en solución como en células, y que sus propiedades ópticas eran especialmente favorables en condiciones acuosas relevantes biológicamente.
Qué implica esto para el estudio de la salud y la enfermedad
En conjunto, estos resultados presentan una sonda compacta, de acción rápida y selectiva que se activa para detectar hipoclorito bajo condiciones suaves y funciona de forma fiable en células vivas. En lugar de confiar en sutiles cambios de color o en estructuras de tintes voluminosas, este diseño usa un simple interruptor de oscuro a verde brillante ligado directamente a un cambio químico específico en un átomo de la molécula. Dado que la sonda puede resaltar células que experimentan niveles elevados de hipoclorito, ofrece una herramienta práctica para explorar cómo surge el estrés oxidativo durante la infección, la inflamación y otros estados patológicos, y podría guiar el desarrollo de sensores más refinados para otras especies reactivas en el futuro.
Cita: Olubiyo, F.F., Klu, S.Y.S., Burgess, R.J. et al. Turn-on quinoline probe for selective sensing of hypochlorite in live cells. Sci Rep 16, 10715 (2026). https://doi.org/10.1038/s41598-026-45327-1
Palabras clave: detección de hipoclorito, sondas fluorescentes, especies reactivas de oxígeno, imagen celular, estrés oxidativo