Clear Sky Science · fr
Sonde quinoléine activée pour la détection sélective de l’hypochlorite dans des cellules vivantes
Une nouvelle façon de voir un produit chimique caché dans nos cellules
Nos cellules produisent et dégradent en permanence des molécules très réactives qui aident à combattre les infections mais peuvent aussi endommager nos tissus lorsqu’elles s’accumulent. L’une d’elles, l’hypochlorite, est étroitement liée à l’inflammation, à la défense immunitaire et à des maladies associées au stress oxydatif. Cette étude décrit une petite molécule colorante nouvellement conçue qui reste éteinte jusqu’à sa rencontre avec l’hypochlorite, puis s’allume d’un vif vert. Cet interrupteur lumineux simple facilite grandement l’observation en temps réel de ce composé furtif à l’intérieur de cellules vivantes.
Pourquoi suivre un oxydant agressif est important
Les espèces réactives de l’oxygène sont des sous-produits chimiques formés lorsque nos cellules utilisent l’oxygène. À des concentrations appropriées, elles aident les globules blancs à tuer les microbes et servent de signaux guidant le comportement cellulaire normal. Mais lorsqu’elles sont en excès, elles attaquent l’ADN, les protéines et les lipides, contribuant à des affections allant de la neurodégénérescence aux maladies cardiovasculaires. L’hypochlorite est l’une de ces espèces réactives produites par les cellules immunitaires, et il est exceptionnellement stable dans les tissus vivants. Parce qu’il est à la fois utile et potentiellement nocif, les scientifiques cherchent des outils capables de révéler avec précision quand, où et en quelle quantité l’hypochlorite est présent dans les cellules.
Concevoir une petite molécule-interrupteur intelligente
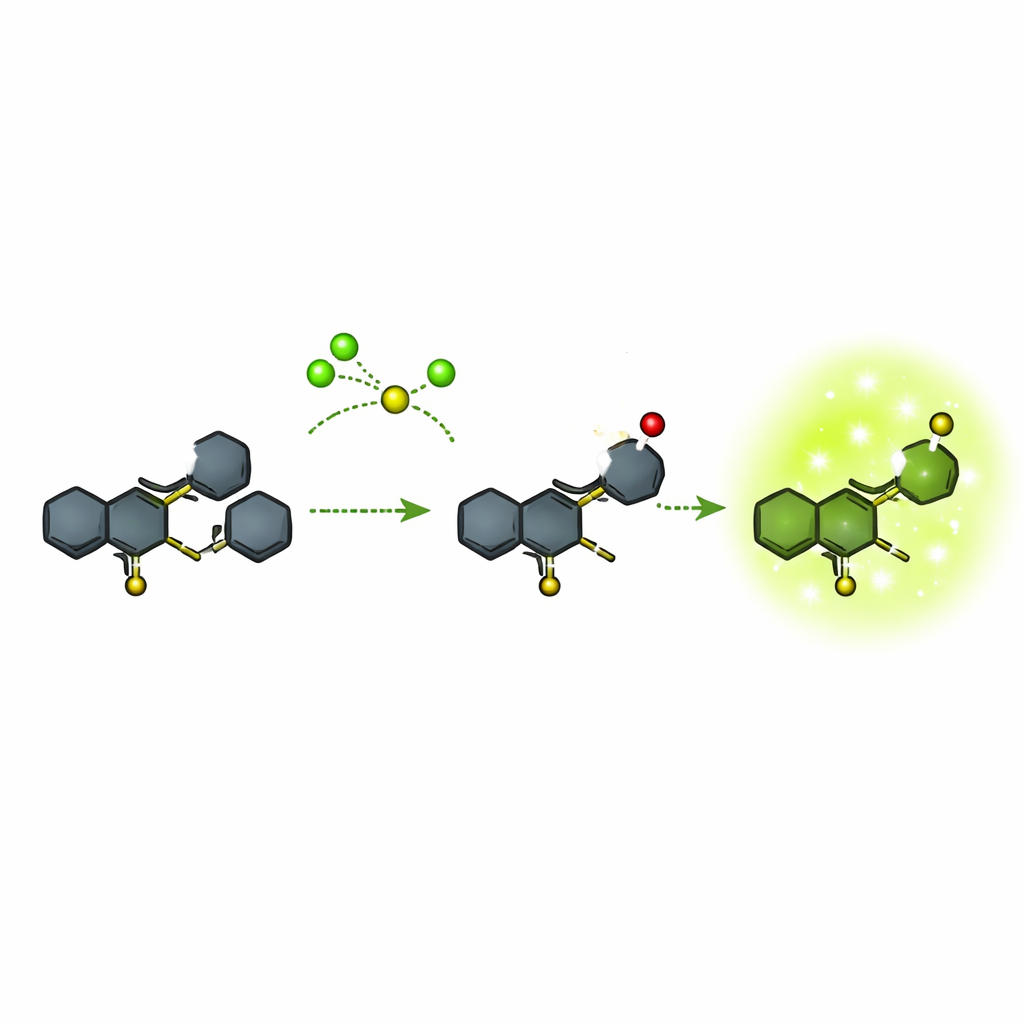
Beaucoup de sondes fluorescentes existantes pour l’hypochlorite sont relativement volumineuses ou nécessitent des changements de couleur complexes qui compliquent des mesures précises. Les auteurs se sont concentrés sur un cadre chimique compact basé sur un système d’anneau appelé quinoléine, lié à un autre système d’anneau connu sous le nom de phenothiazine. Ils ont construit cette structure en quelques étapes à partir de matières premières commerciales, contrôlant rigoureusement chaque étape par résonance magnétique nucléaire, spectrométrie de masse et mesures optiques. La sonde finale, appelée composé 5, est presque non lumineuse seule mais conçue de telle sorte qu’un atome de soufre particulier puisse être attaqué sélectivement par l’hypochlorite. Cette réaction transforme la molécule en une nouvelle forme (composé 6) qui émet fortement dans la région verte du spectre.
De l’obscurité à la brillance en quelques secondes, et uniquement pour la bonne cible
L’équipe a testé la spécificité et la rapidité de la réponse de la sonde à différents produits chimiques. En solution, le composé 5 ne montrait pratiquement aucune fluorescence dans une large gamme de solvants. Exposé à de nombreux ions courants, petites molécules soufrées et autres espèces réactives de l’oxygène, il restait éteint. Seul l’hypochlorite provoquait une émission verte nette autour de 523 nanomètres, et l’intensité augmentait en fonction de la concentration en hypochlorite sur une plage utile. La réaction était rapide : une lumière mesurable apparaissait en environ 10 secondes et continuait d’augmenter sur plusieurs minutes. À des niveaux très élevés d’hypochlorite, la sonde pouvait être oxydée un peu plus loin en une forme sur-oxydée (un sulfone) moins lumineuse, mais cela se produisait en dehors de la plage de travail principale. Globalement, la limite de détection était extrêmement basse, bien en dessous du micromolaire, et le signal était suffisamment intense pour être visible à l’œil nu.
Observer l’hypochlorite à l’intérieur de cellules vivantes
Pour vérifier si cette chimie fonctionnait en contexte biologique, les chercheurs ont testé la sonde sur des cellules de moelle osseuse de souris fraîchement isolées. À une faible dose de sonde qui n’endommageait pas les cellules, ils ont utilisé la cytométrie en flux et la microscopie de fluorescence pour suivre son comportement. Les cellules traitées uniquement avec la sonde montraient seulement une légère augmentation du signal vert, suggérant que les niveaux internes normaux d’hypochlorite sont faibles mais détectables. Lorsque les mêmes cellules ont ensuite été exposées à des quantités croissantes d’hypochlorite ajouté, une grande fraction des cellules s’est fortement illuminée, le signal augmentant avec la dose. Des tests complémentaires ont montré que le produit fluorescent était stable sous illumination continue, tant en solution que dans les cellules, et que ses propriétés optiques étaient particulièrement favorables dans des conditions aqueuses et biologiquement pertinentes.
Ce que cela implique pour l’étude de la santé et des maladies
Dans l’ensemble, ces résultats présentent une sonde « turn-on » compacte, rapide et sélective pour l’hypochlorite, opérant dans des conditions douces et fonctionnant de manière fiable dans des cellules vivantes. Plutôt que de s’appuyer sur des changements de couleur subtils ou des structures colorantes encombrantes, ce dessin utilise un simple passage de l’obscurité à un vert brillant lié directement à un changement chimique spécifique sur un atome de la molécule. Parce que la sonde peut mettre en évidence les cellules exposées à des niveaux élevés d’hypochlorite, elle offre un outil pratique pour explorer comment le stress oxydatif apparaît lors d’infections, d’inflammations et d’autres états pathologiques, et pourrait guider le développement de capteurs plus raffinés pour d’autres espèces réactives à l’avenir.
Citation: Olubiyo, F.F., Klu, S.Y.S., Burgess, R.J. et al. Turn-on quinoline probe for selective sensing of hypochlorite in live cells. Sci Rep 16, 10715 (2026). https://doi.org/10.1038/s41598-026-45327-1
Mots-clés: détection de l’hypochlorite, sondes fluorescentes, espèces réactives de l’oxygène, imagerie cellulaire, stress oxydatif