Clear Sky Science · pl
Wyzwalany sond quinolinowy do selektywnego wykrywania podchlorynu w żywych komórkach
Nowy sposób obserwacji ukrytego związku chemicznego w naszych komórkach
Nasze komórki nieustannie wytwarzają i rozkładają silnie reaktywne cząsteczki, które pomagają zwalczać infekcje, ale gdy się kumulują, mogą też uszkadzać tkanki. Jedną z takich cząsteczek jest podchloryn, ściśle powiązany z zapaleniem, obroną immunologiczną i chorobami związanymi ze stresem oksydacyjnym. W tej pracy opisano nowo zaprojektowaną małą cząsteczkę barwnika, która pozostaje nieświecąca, dopóki nie zetknie się z podchlorynem, a następnie włącza się, emitując jasne zielone światło. Ten prosty „wyłącznik świetlny” znacznie ułatwia badaczom obserwację tej ulotnej substancji w czasie rzeczywistym wewnątrz żywych komórek.
Dlaczego śledzenie silnego utleniacza ma znaczenie
Reaktywne formy tlenu to produkty uboczne chemicznych procesów zachodzących, gdy komórki wykorzystują tlen. W odpowiednich ilościach pomagają białym krwinkom zabijać drobnoustroje i pełnią rolę sygnałów kierujących prawidłowym działaniem komórek. Gdy ich poziomy stają się zbyt wysokie, atakują DNA, białka i lipidy, przyczyniając się do schorzeń od neurodegeneracji po choroby serca. Podchloryn to jedna z takich reaktywnych form wytwarzana przez komórki odpornościowe i cechuje się stosunkowo dużą trwałością w tkankach. Ponieważ jest zarówno użyteczny, jak i potencjalnie szkodliwy, naukowcy potrzebują narzędzi, które dokładnie pokażą, kiedy, gdzie i w jakiej ilości podchloryn występuje w komórkach.
Projektowanie małej, inteligentnej cząsteczki-wyłącznika światła
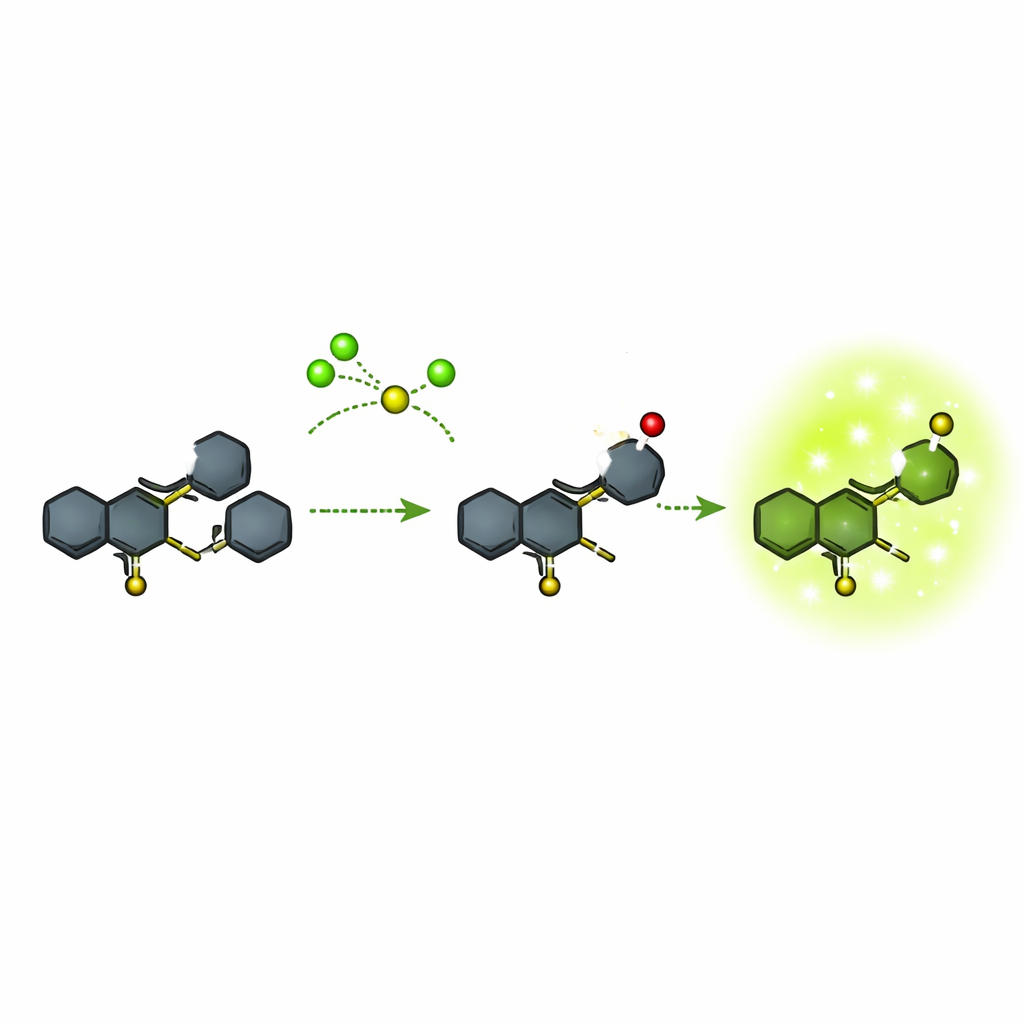
Wiele istniejących sond fluorescencyjnych do wykrywania podchlorynu jest stosunkowo masywnych lub wymaga skomplikowanych zmian barwy, co utrudnia precyzyjne pomiary. Autorzy skupili się na zwartej strukturze chemicznej opartej na systemie pierścieniowym zwanym chinoliną, sprzężonym z innym układem pierścieniowym znanym jako fenotiazyna. Zbudowali tę strukturę w kilku etapach z komercyjnie dostępnych substratów, rygorystycznie kontrolując każdy etap za pomocą spektroskopii rezonansu magnetycznego, spektrometrii mas i pomiarów optycznych. Końcowa sonda, nazwana związkiem 5, jest praktycznie nieświecąca sama w sobie, ale zaprojektowano ją tak, aby konkretny atom siarki mógł być selektywnie atakowany przez podchloryn. Ta reakcja przekształca cząsteczkę w nową formę (związek 6), która silnie emituje w zielonym obszarze widma.
Od ciemności do jasności w kilka sekund i tylko dla właściwego celu
Zespół sprawdził specyficzność i szybkość reakcji sondy na różne związki. W roztworze związek 5 wykazywał praktycznie brak fluorescencji w szerokim zakresie rozpuszczalników. Po wystawieniu na działanie wielu powszechnych jonów, małych związków zawierających siarkę i innych reaktywnych form tlenu, pozostawał ciemny. Tylko podchloryn wywołał silną, ostrą emisję zieloną wokół 523 nm, a intensywność rosła proporcjonalnie do stężenia podchlorynu w użytecznym zakresie. Reakcja była szybka: mierzalne światło pojawiało się w ciągu około 10 sekund i dalej narastało w ciągu minut. Przy bardzo wysokich poziomach podchlorynu sonda mogła ulec dalszemu utlenieniu do formy nadutlenionej (sulfonu), która była mniej jasna, ale zachodziło to poza głównym zakresem działania. Ogólnie granica detekcji była bardzo niska, znacznie poniżej jednego mikromolara, a sygnał na tyle intensywny, że był widoczny gołym okiem.
Obserwacja podchlorynu wewnątrz żywych komórek
Aby sprawdzić, czy ta chemia działa w warunkach biologicznych, badacze przetestowali sondę w świeżo izolowanych komórkach szpiku kostnego myszy. Przy niskiej dawce sondy, która nie szkodziła komórkom, zastosowali cytometrię przepływową i mikroskopię fluorescencyjną do monitorowania jej zachowania. Komórki traktowane tylko sondą wykazywały jedynie niewielki wzrost zielonego sygnału, co sugeruje, że wewnętrzne poziomy podchlorynu są niskie, lecz wykrywalne. Gdy te same komórki wystawiono na działanie coraz większych ilości dodanego podchlorynu, duża frakcja komórek silnie się rozświetliła, a sygnał nasilał się wraz z dawką. Badania uzupełniające wykazały, że rozświetlony produkt jest stabilny pod ciągłym oświetleniem zarówno w roztworze, jak i w komórkach, a jego właściwości optyczne są szczególnie korzystne w warunkach wodnych, istotnych biologicznie.
Co to oznacza dla badań nad zdrowiem i chorobami
W sumie wyniki przedstawiają zwartą, szybko działającą i selektywną sondę „włączającą się” do wykrywania podchlorynu, działającą w łagodnych warunkach i niezawodną w żywych komórkach. Zamiast polegać na subtelnych przesunięciach barwy czy masywnych strukturach barwników, ten projekt wykorzystuje prosty przełącznik od ciemności do jasnego zielonego światła powiązany bezpośrednio ze specyficzną zmianą chemiczną na jednym atomie w cząsteczce. Ponieważ sonda może wyróżniać komórki doświadczające podwyższonego poziomu podchlorynu, oferuje praktyczne narzędzie do badania, jak powstaje stres oksydacyjny podczas infekcji, zapalenia i innych stanów chorobowych, i może wskazać drogę do opracowania bardziej wyrafinowanych sensorów dla innych reaktywnych związków w przyszłości.
Cytowanie: Olubiyo, F.F., Klu, S.Y.S., Burgess, R.J. et al. Turn-on quinoline probe for selective sensing of hypochlorite in live cells. Sci Rep 16, 10715 (2026). https://doi.org/10.1038/s41598-026-45327-1
Słowa kluczowe: wykrywanie podchlorynu, sondy fluorescencyjne, reaktywne formy tlenu, obrazowanie komórek, stres oksydacyjny