Clear Sky Science · de
Quinolin-Aktivierungsfarbstoff zur selektiven Erkennung von Hypochlorit in lebenden Zellen
Eine neue Methode, eine verborgene Chemikalie in unseren Zellen sichtbar zu machen
Unsere Zellen erzeugen und bauen ständig hochreaktive Moleküle ab, die einerseits bei der Abwehr von Infektionen helfen, bei Anhäufung aber auch Gewebe schädigen können. Eines davon, Hypochlorit, steht in enger Verbindung mit Entzündung, Immunabwehr und Erkrankungen, die mit oxidativem Stress einhergehen. In dieser Studie wird ein neu entworfener, kleiner Farbstoff beschrieben, der dunkel bleibt, bis er auf Hypochlorit trifft, und dann mit einem hellen grünen Leuchten anschaltet. Dieser einfache Lichtschalter erleichtert es Forschern erheblich, dieses schwer fassbare Molekül in Echtzeit innerhalb lebender Zellen zu verfolgen.
Warum die Verfolgung eines starken Oxidationsmittels wichtig ist
Reaktive Sauerstoffspezies sind chemische Nebenprodukte, die entstehen, wenn unsere Zellen Sauerstoff nutzen. In passenden Mengen helfen sie weißen Blutkörperchen, Mikroben zu töten, und dienen als Signale, die normales Zellverhalten steuern. Erhöhen sich ihre Konzentrationen jedoch zu stark, greifen sie DNA, Proteine und Fette an und tragen zu Erkrankungen von Neurodegeneration bis Herzkrankheiten bei. Hypochlorit ist eine solche reaktive Spezies, die von Immunzellen produziert wird und in lebendem Gewebe ungewöhnlich stabil ist. Weil sie zugleich nützlich und potenziell schädlich ist, benötigen Wissenschaftler Werkzeuge, die genau zeigen, wann, wo und in welcher Menge Hypochlorit in Zellen vorkommt.
Entwurf eines kleinen, intelligenten Lichtschaltermoleküls
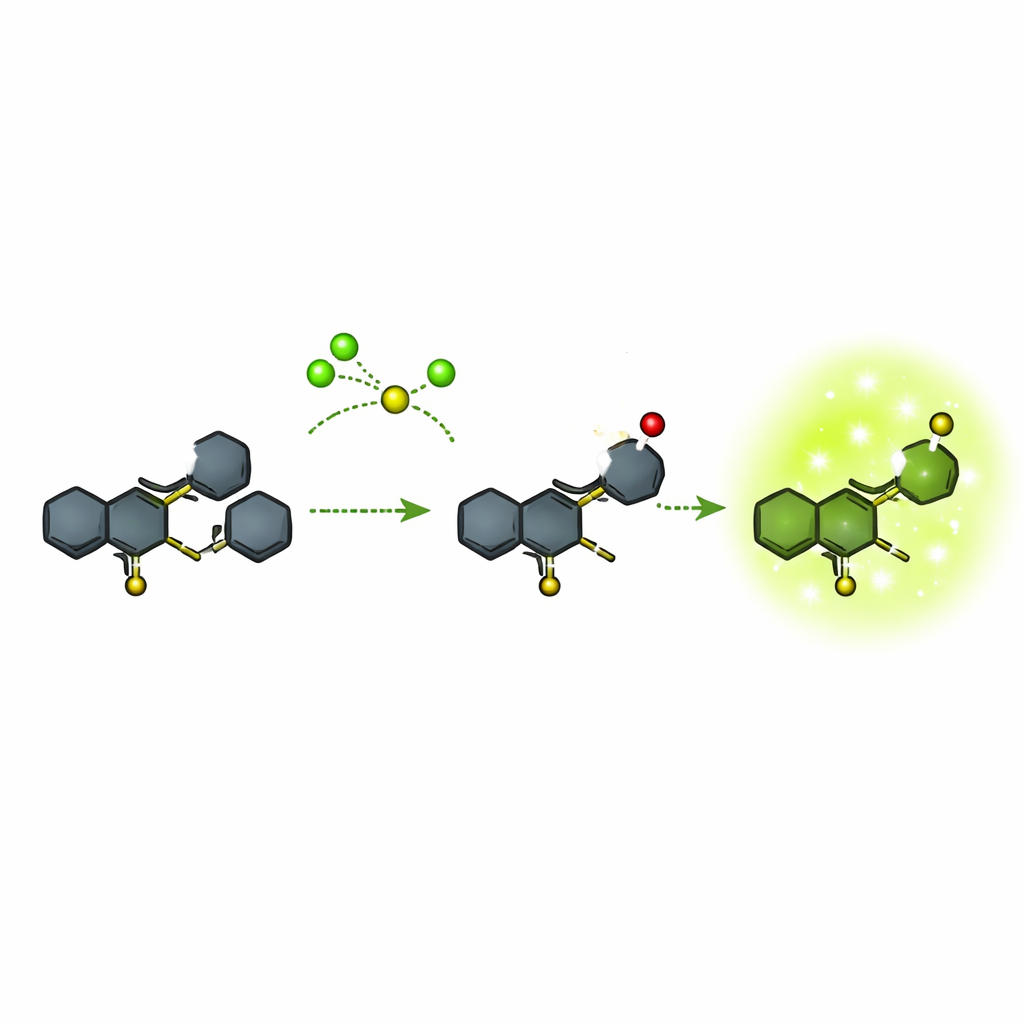
Viele existierende fluoreszierende Sonden für Hypochlorit sind vergleichsweise sperrig oder erfordern komplizierte Farbwechsel, die präzise Messungen erschweren. Die Autoren konzentrierten sich auf ein kompaktes chemisches Gerüst, das auf einem Ringsystem namens Quinolin basiert und mit einem weiteren Ringsystem, Phenothiazin, verbunden ist. Sie bauten diese Struktur in wenigen Schritten aus kommerziell erhältlichen Ausgangsstoffen auf und prüften jede Stufe sorgfältig mit Kernspinresonanz, Massenspektrometrie und optischen Messungen. Die finale Sonde, bezeichnet als Verbindung 5, ist von sich aus nahezu nicht leuchtend, wurde aber so gestaltet, dass ein bestimmtes Schwefelatom selektiv von Hypochlorit angegriffen werden kann. Diese Reaktion verwandelt das Molekül in eine neue Form (Verbindung 6), die stark im grünen Bereich des Spektrums leuchtet.
Von dunkel zu hell in Sekunden — und nur beim richtigen Ziel
Das Team untersuchte, wie spezifisch und wie schnell die Sonde auf verschiedene Chemikalien reagiert. In Lösung zeigte Verbindung 5 in einer breiten Palette von Lösungsmitteln praktisch keine Fluoreszenz. Beim Kontakt mit vielen häufigen Ionen, kleinen schwefelhaltigen Molekülen und anderen reaktiven Sauerstoffspezies blieb sie dunkel. Nur Hypochlorit verursachte eine starke, scharfe grüne Emission bei etwa 523 Nanometern, und die Helligkeit stieg in Abhängigkeit von der Hypochlorit-Konzentration über einen nützlichen Bereich an. Die Reaktion war schnell: messbares Licht erschien innerhalb von etwa 10 Sekunden und nahm über Minuten weiter zu. Bei sehr hohen Hypochlorit-Spiegeln konnte die Sonde noch einen Schritt weiter zu einer überoxidierten Form (Sulfona) getrieben werden, die weniger hell war, doch dies trat außerhalb des Hauptarbeitsbereichs auf. Insgesamt lag die Nachweisgrenze sehr niedrig, deutlich unter einem Mikromolar, und das Signal war so intensiv, dass es mit bloßem Auge sichtbar war.
Beobachtung von Hypochlorit in lebenden Zellen
Um zu prüfen, ob diese Chemie in einem biologischen Umfeld funktioniert, testeten die Forscher die Sonde in frisch isolierten Knochenmarkzellen von Mäusen. Bei einer niedrigen Sondendosis, die den Zellen nicht schadete, verfolgten sie das Verhalten mittels Durchflusszytometrie und Fluoreszenzmikroskopie. Zellen, die nur mit der Sonde behandelt wurden, zeigten nur einen leichten Anstieg des grünen Lichts, was darauf hindeutet, dass normale interne Hypochlorit-Spiegel niedrig, aber nachweisbar sind. Wurden dieselben Zellen dann mit steigenden Mengen zugefügten Hypochlorits exponiert, leuchtete ein großer Teil der Zellen hell auf, wobei das Signal mit der Dosis skalierte. Folgetests zeigten, dass das leuchtende Produkt unter kontinuierlicher Beleuchtung sowohl in Lösung als auch in Zellen stabil war und dass seine optischen Eigenschaften insbesondere in wässrigen, biologisch relevanten Bedingungen günstig waren.
Was das für das Studium von Gesundheit und Krankheit bedeutet
Zusammengefasst stellen diese Ergebnisse eine kompakte, schnell reagierende und selektive "Turn-on"-Sonde für Hypochlorit vor, die unter schonenden Bedingungen arbeitet und zuverlässig in lebenden Zellen einsetzbar ist. Anstatt sich auf subtile Farbverschiebungen oder sperrige Farbstoffstrukturen zu stützen, verwendet dieses Design einen einfachen Wechsel von dunkel zu hellem Grünlicht, der direkt mit einer spezifischen chemischen Änderung an einem Atom des Moleküls verknüpft ist. Da die Sonde Zellen mit erhöhtem Hypochlorit hervorheben kann, bietet sie ein praktisches Werkzeug, um zu erforschen, wie oxidativer Stress während Infektionen, Entzündungen und anderen Krankheitszuständen entsteht, und könnte die Entwicklung verfeinerter Sensoren für andere reaktive Chemikalien in der Zukunft leiten.
Zitation: Olubiyo, F.F., Klu, S.Y.S., Burgess, R.J. et al. Turn-on quinoline probe for selective sensing of hypochlorite in live cells. Sci Rep 16, 10715 (2026). https://doi.org/10.1038/s41598-026-45327-1
Schlüsselwörter: Hypochlorit-Erkennung, fluoreszierende Sonden, reaktive Sauerstoffspezies, Zellbildgebung, oxidativer Stress